Clear Sky Science · ar
تكوين خلايا عصبية جديدة في الحُصين البشري لدى البالغين والشيخوخة ومرض ألزهايمر
لماذا تهم الخلايا الدماغية الجديدة لدى البالغين
لعقود، اختلف العلماء حول سؤال بسيط لكنه عميق: هل يولّد البشر البالغون خلايا دماغية جديدة في مركز الذاكرة بالمخ، وإذا كان الأمر كذلك، فهل يساعد ذلك في حمايتنا من فقدان الذاكرة ومرض ألزهايمر؟ يتصدى هذا البحث لهذا الجدل مباشرة عبر دمج أدوات متقدمة على مستوى خلية مفردة وأنسجة دماغية بشرية بعد الوفاة ليبيّن كيف تتصرف الخلايا العصبية المولودة حديثاً في الحُصين لدى البالغين الأصحاء، والأشخاص في مسار التحول نحو ألزهايمر، ومرضى الألزهايمر، وكذلك كبار السن النادرين الذين يمتلكون ذاكرة استثنائية والمعروفين باسم SuperAgers.
حضانة الذاكرة في الدماغ
في عمق الحُصين يوجد التلم المسنن (dentate gyrus)، نوع من «الحضانة» للذاكرة حيث يمكن أن تنشأ خلايا عصبية جديدة من الخلايا الجذعية المحلية. قام الباحثون بتشريح هذه المنطقة من أدمغة 38 متبرعاً متوفىً، تراوحت أعمارهم من بالغين صغار إلى كبار في السن ذوي مستويات أداء ذاكرة وتغيرات مرتبطة بألزهايمر متفاوتة. باستخدام تسلسل متعدد الأومكس على مستوى خلية مفردة—الذي يقرأ كلّاً من نشاط الجينات وكيفية تغليف الحمض النووي—حللوا أكثر من 350,000 نواة خلوية فردية. أتاح ذلك تمييز الخلايا الجذعية العصبية، والخلايا الوليدة العصبية (الخلية الوليدة المبكرة) والخلايا الحُبيبية غير الناضجة بشكل موثوق، ورسم خريطة لكيفية تقدمها إلى خلايا عصبية ناضجة تنضم إلى دوائر الذاكرة. تدعم بياناتهم بشكل قاطع وجود مسار تطوري تدريجي للخلايا العصبية الجديدة في الحُصين البشري البالغ.
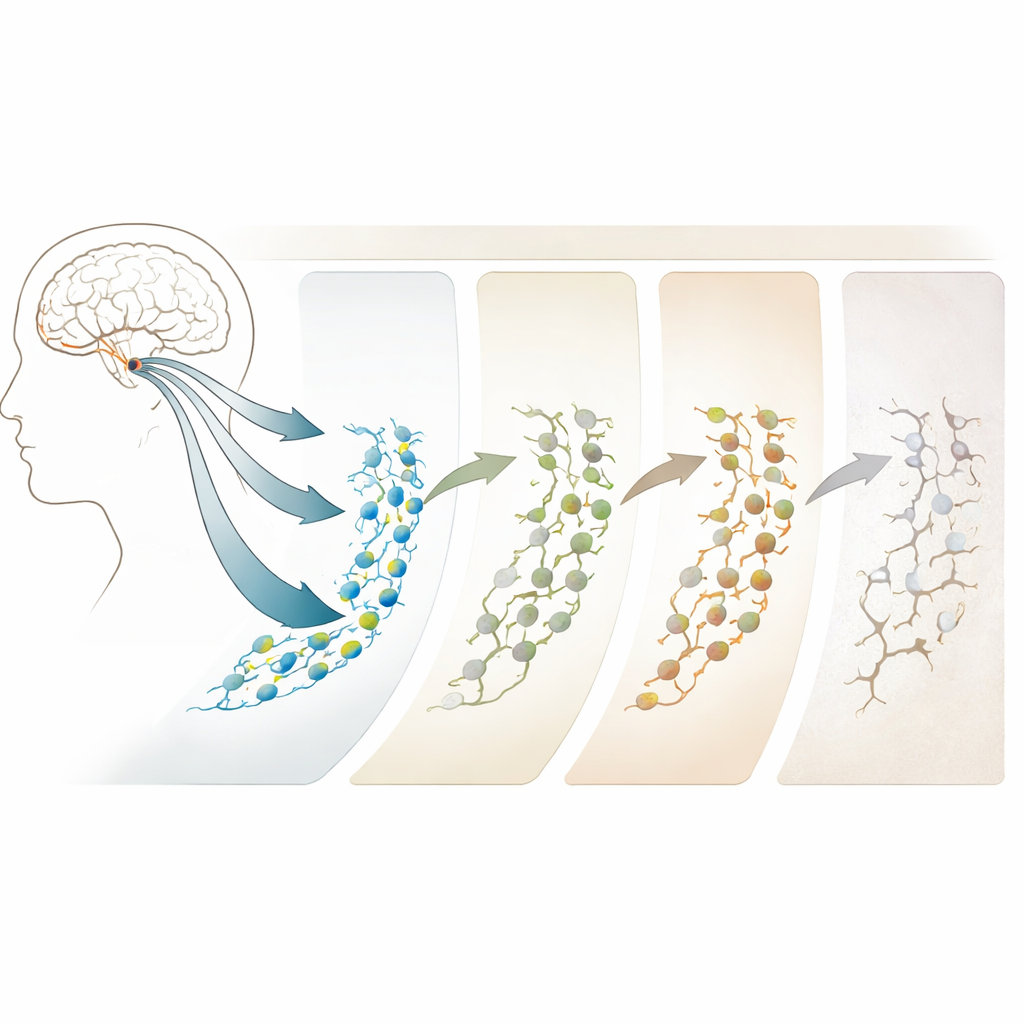
كيف يشوّه التقدّم في العمر ومرض ألزهايمر هذا المسار
أظهر المقارنة بين البالغين الشباب والمجموعات الأكبر سناً أن الشيخوخة وألزهايمر لا يقومان ببساطة بتشغيل أو إيقاف التكوين العصبي؛ بل يعيدان تشكيله. في الأفراد ذوي الآفات الوسيطة ما قبل السريرية—أشخاص يبدو أنهم في طور الانتقال من الشيخوخة الطبيعية نحو ألزهايمر—يزداد عدد الخلايا الجذعية فعلياً، لكن المراحل اللاحقة من التكوين العصبي تبدأ في التراجع. في مرض ألزهايمر الكامل، تقلّ الخلايا الوليدة والعصبونات غير الناضجة بشكل ملحوظ، رغم أن خلايا شبيهة بالخلايا الجذعية تكون أكثر وفرة. اللافت أن التغييرات الأكثر ثباتاً لا تكون دائماً في الجينات نفسها، بل في مناطق من الحمض النووي تصبح أكثر أو أقل قابلية للوصول، مثل بوابات تفتح أو تغلق للتحكم في أي الجينات يمكن استخدامها. تظهر هذه التحولات فوق الجينية، خصوصاً في مناطق مرتبطة بالتشابكات وبنية العص neuron، مبكراً وتتزايد مع تقدّم المرض، ما يجعلها إشارات تحذيرية مبكرة محتملة وهدافاً علاجياً.
البصمات الجزيئية للمرونة
قدّم المتفوّقون في العمر (SuperAgers)—الأشخاص في الثمانينيات وما بعدها الذين يتذكرون بمستوى يقارب البالغين الأصغر سناً—نافذة على المرونة المعرفية. احتوت أحماضهم الحُصينية على عدد أكبر بكثير من الخلايا الوليدة والعصبونات غير الناضجة مقارنة بمرضى ألزهايمر، وغالباً أكثر من كبار السن العاديين. بدلاً من تغييرات هائلة في الخلايا الجذعية، تكمن الفروقات الرئيسية في آلاف مناطق الحمض النووي التي كانت أكثر انفتاحاً في الخلايا الوليدة والعصبونات غير الناضجة، مما يدعم نموّاً قوياً ووظيفة تشابكية فعّالة. حدّد الفريق «درجة المرونة» التي تجمع الجينات ومناطق الحمض النووي التي تبقى مستقرة لدى البالغين الشباب والشيخوخة الصحية وSuperAgers لكنها تنهار في ألزهايمر. كثير منها مرتبط بالحفاظ على الاتصالات العصبية والتواصل الفعّال. كما أظهر المتفوّقون أنماطاً مميزة لشبكات التنظيم—تراكيب من بروتينات تحكم ومفاتيح حمض نووي—تشبه في بعض النواحي ما لدى البالغين الشباب لكنها تتضمن أيضاً منشّطات فريدة قد تدفع الخلايا العصبية المولودة نحو حالة قوية وطويلة الأمد.
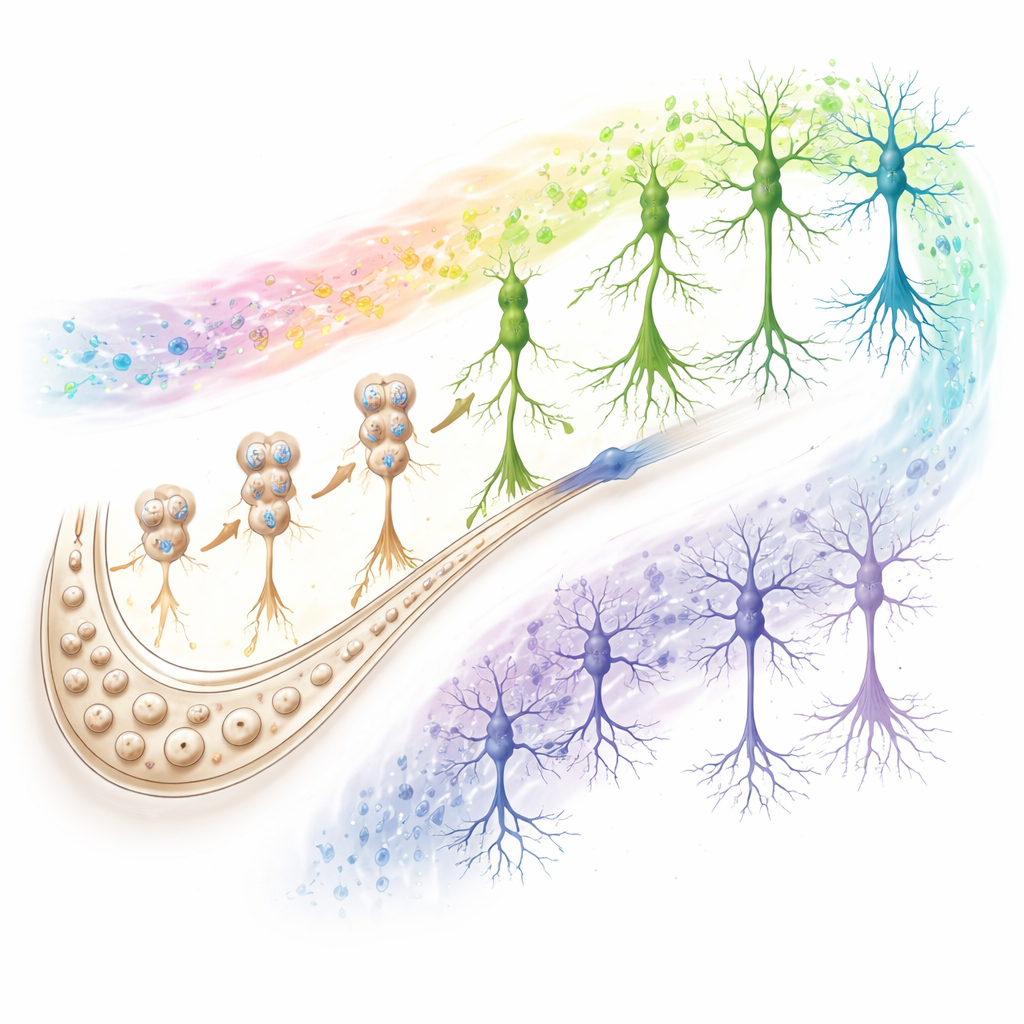
دوائر تميّز الشيخوخة الناجحة عن المتدهورة
لم يتوقف البحث عند الخلايا الوليدة. من خلال فحص جميع الأنواع الخلوية الرئيسية، وجد المؤلفون أن الإشارات التي تحفظ أو تقوّض الإدراك تتركّز في لاعبين رئيسيين: خلايا CA1 (محطة الإخراج الأساسية من الحُصين) والخلايا النجميّة (astrocytes) التي تدعم البيئة الكيميائية وتساعد في تنظيم التشابكات. في كبار السن الناجحين وSuperAgers، تدعم الجينات في خلايا CA1 نقل إشارات تشابكية قوي، وإنتاج طاقة ومسارات تنظيف خلوية، بينما تُظهر الخلايا النجمية أنماط كروماتين تفضّل الاستجابات الوقائية. في الأشخاص على طريق ألزهايمر، تنحرف هذه المسارات في الاتجاه المعاكس. أبرزت تحليلات التواصل بين الخلايا ضعف الالتصاق والإشارات المعتمدة على الغلوتامات بين خلايا CA1 والخلايا النجمية والخلايا المولّدة للعصبونات في المجموعات ما قبل السريرية والألزهايمر، مما يشير إلى أن تدهور التشابكات المثبطة هو سمة مشتركة للانخفاض المعرفي.
ماذا يعني ذلك لحماية الذاكرة
معاً، ترسم النتائج صورة مفصّلة: يولّد البشر البالغون خلايا عصبية جديدة في الحُصين، لكن هذه العملية حساسة للغاية تجاه العمر والمرض. تحدث أوضح وأبكر التغيرات على مستوى قابلية وصول الكروماتين—طريقة تغليف الحمض النووي—قبل أن تتغير الكثير من الجينات في نشاطها بشكل واضح. في الأدمغة المقاومة، مثل أدمغة SuperAgers، تبقي الشبكات الجزيئية التكوين العصبي والتواصل التشابكي في حالة «شبابية» رغم التقدم في العمر. في الأدمغة الضعيفة، تنقلب هذه الشبكات، مما يؤدي إلى توقف نمو الخلايا العصبية الجديدة وتآكل دوائر الحُصين. من خلال الكشف عن هذه البصمات فوق الجينية والخلوية، يشير البحث إلى استراتيجيات قد تساعد يوماً ما في الحفاظ على الذاكرة: علاجات لا تركز فقط على إزالة اللويحات، بل على إبقاء «حضانة الذاكرة» في الدماغ مفتوحة، ومفاتيح الحمض النووي مضبوطة بشكل صحيح، وتشابكاته مقاومة.
الاستشهاد: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
الكلمات المفتاحية: تكوين خلايا عصبية في الحُصين, المرونة المعرفية, المتفوّقون بالغ الأَمْر (SuperAgers), علم الوراثة فوق الجيني, مرض ألزهايمر