Clear Sky Science · de
Neurogenese im menschlichen Hippocampus im Erwachsenenalter, beim Altern und bei Alzheimer
Warum neue Gehirnzellen im Erwachsenenalter wichtig sind
Jahrzehntelang stritten Wissenschaftler über eine einfache, aber grundsätzliche Frage: Bilden erwachsene Menschen im Gedächtniszentrum des Gehirns neue Nervenzellen, und wenn ja, schützt das vor Gedächtnisverlust und Alzheimer? Diese Studie geht diese Debatte direkt an, indem sie hochmoderne Einzelzell‑Methoden mit postmortalem menschlichem Hirngewebe kombiniert, um zu zeigen, wie neugeborene Neuronen im Hippocampus bei gesunden Erwachsenen, bei Menschen auf dem Weg zu Alzheimer, bei Erkrankten und bei seltenen älteren Personen mit außergewöhnlichem Gedächtnis (sogenannten SuperAgers) verhalten.
Die Gedächtniskinderstube des Gehirns
Tief im Hippocampus liegt der Gyrus dentatus, eine Art Gedächtnis‑„Kinderstube“, in der aus örtlichen Stammzellen neue Neuronen entstehen können. Die Autoren entnahmen diesen Bereich aus den Gehirnen von 38 verstorbenen Spendern, von jungen Erwachsenen bis zu älteren Menschen mit unterschiedlichem Gedächtnisleistung und Alzheimer‑assoziierten Veränderungen. Mit multiomischer Einzelzell‑Sequenzierung—die sowohl Genaktivität als auch die DNA‑Verpackung liest—analysierten sie mehr als 350.000 einzelne Zellkerne. Das ermöglichte eine verlässliche Unterscheidung von neuralen Stammzellen, Neuroblasten (frühe Neuzellen) und unreifen Körnerneuronen sowie die Kartierung ihres Fortschreitens hin zu voll ausgereiften Nervenzellen, die sich in Gedächtnisnetzwerke einfügen. Ihre Daten stützen eindeutig die Existenz einer stufenweisen Entwicklungs‑Trajectory neuer Neuronen im erwachsenen menschlichen Hippocampus.
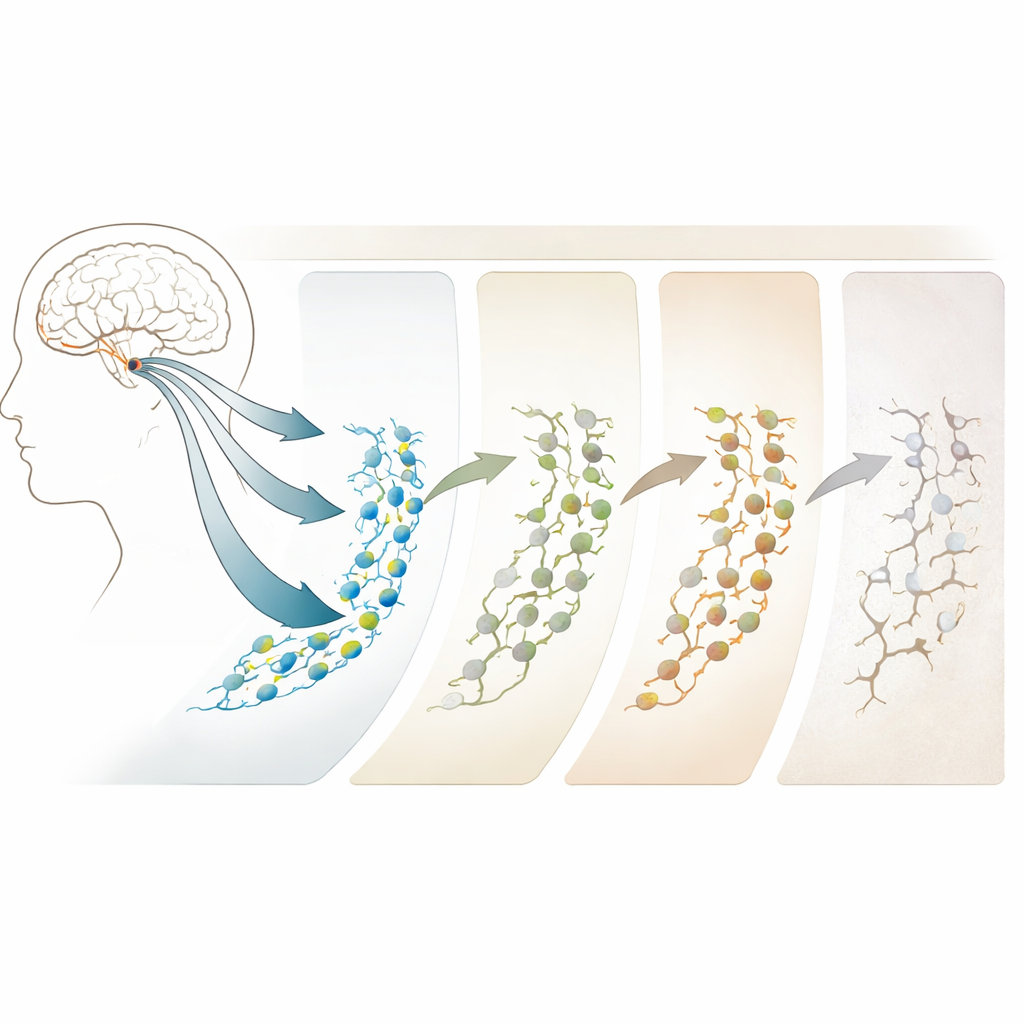
Wie Alter und Alzheimer die Entwicklung verbiegen
Der Vergleich von jungen Erwachsenen mit älteren Gruppen zeigte, dass Altern und Alzheimer Neurogenese nicht einfach an‑ oder ausschalten; sie verändern vielmehr deren Verlauf. Bei Menschen mit präklinischer intermediärer Pathologie—Personen, die offenbar vom normalen Altern in Richtung Alzheimer übergehen—nimmt die Zahl der Stammzellen sogar zu, doch die späteren Stadien der Neurogenese beginnen zu stocken. Bei manifestem Alzheimer sind Neuroblasten und unreife Neuronen deutlich reduziert, obwohl stammzellähnliche Zellen häufiger vorkommen. Auffällig ist, dass die beständigsten Veränderungen nicht in den Genen selbst liegen, sondern in DNA‑Bereichen, die mehr oder weniger zugänglich werden, wie Tore, die öffnen oder schließen und so steuern, welche Gene genutzt werden können. Diese epigenetischen Verschiebungen, insbesondere in Regionen, die mit Synapsen und neuronaler Struktur verknüpft sind, treten früh auf und verstärken sich mit der Krankheit, was sie zu potenziellen frühen Warnzeichen und therapeutischen Zielen macht.
Die molekularen Fingerabdrücke der Resilienz
SuperAgers—Menschen in ihren 80ern und älter, die sich so gut erinnern wie deutlich Jüngere—boten Einblicke in Resilienz. Ihre Hippocampi enthielten deutlich mehr Neuroblasten und unreife Neuronen als die von Alzheimer‑Patienten und oft auch mehr als typische ältere Erwachsene. Statt massiver Veränderungen in den Stammzellen lagen die entscheidenden Unterschiede in tausenden DNA‑Regionen, die in Neuroblasten und unreifen Neuronen offener waren und damit robustes Wachstum und synaptische Funktion unterstützten. Das Team definierte einen „Resilienz‑Score“, der Gene und DNA‑Regionen erfasst, die in jungen Erwachsenen, gesunden Alten und SuperAgers stabil bleiben, in Alzheimer aber zusammenbrechen. Viele davon stehen mit der Aufrechterhaltung neuronaler Verbindungen und effizienter Kommunikation in Zusammenhang. SuperAgers zeigten zudem ein charakteristisches Muster regulatorischer Netzwerke—Kombinationen aus Steuerproteinen und DNA‑Schaltern—das in mancher Hinsicht jungen Erwachsenen ähnelt, aber auch einzigartige Aktivatoren enthält, die neugeborene Neuronen in einen besonders robusten, langlebigen Zustand treiben könnten.
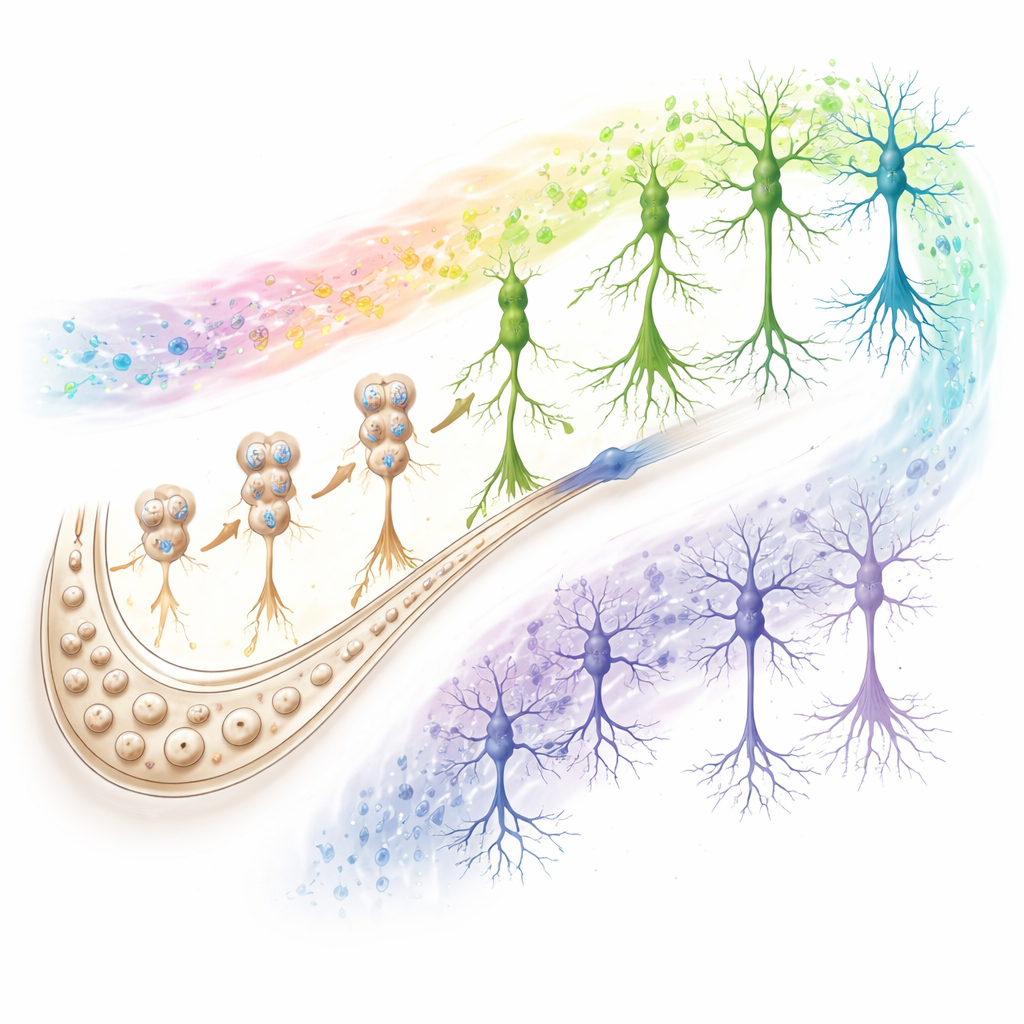
Netzwerke, die erfolgreiches gegen versagendes Altern markieren
Die Studie blieb nicht bei neugeborenen Neuronen stehen. Durch die Untersuchung aller wichtigen Zelltypen fanden die Autoren, dass Signale, die Kognition erhalten oder erodieren, sich auf zwei Hauptakteure konzentrieren: CA1‑Neuronen (eine zentrale Ausgangsstation des Hippocampus) und Astrozyten (Stützzellen, die das chemische Milieu steuern und Synapsen mitregulieren). Bei erfolgreichen Agenden und SuperAgers unterstützen Gene in CA1‑Neuronen starke synaptische Übertragung, Energieproduktion und zelluläre Reinigungswege, während Astrozyten Chromatinmuster zeigen, die protektive Reaktionen begünstigen. Bei Menschen auf dem Weg zu Alzheimer driften diese gleichen Pfade in die entgegengesetzte Richtung. Analysen der Zell‑zu‑Zell‑Kommunikation hoben geschwächte Adhäsion und glutamatbasierte Signalübertragung zwischen CA1‑Neuronen, Astrozyten und neurogenen Zellen in präklinischen und Alzheimer‑Gruppen hervor, was darauf hindeutet, dass der Zerfall exzitatorischer Synapsen ein gemeinsames Kennzeichen kognitiven Abbaus ist.
Was das für den Schutz des Gedächtnisses bedeutet
In der Summe zeichnen die Ergebnisse ein detailliertes Bild: Erwachsene Menschen bilden weiterhin neue hippokampale Neuronen, doch dieser Prozess ist äußerst empfindlich gegenüber Alter und Krankheit. Die frühesten und robustesten Veränderungen treten auf der Ebene der Chromatinzugänglichkeit auf—also wie DNA verpackt ist—lange bevor viele Gene sichtbar ihre Aktivität ändern. In resilienten Hirnen, wie denen von SuperAgers, halten molekulare Netzwerke Neurogenese und synaptische Kommunikation in einem „jugendlichen“ Modus trotz fortgeschrittenen Alters aufrecht. In anfälligen Hirnen verschieben sich diese Netzwerke, was zur Blockade der Entwicklung neuer Neuronen und zum Zerfasern hippokampaler Schaltkreise führt. Durch das Aufdecken dieser epigenetischen und zellulären Signaturen weist die Studie auf Strategien hin, die eines Tages das Gedächtnis bewahren könnten: Therapien, die nicht nur Plaques entfernen, sondern die Gedächtnis‑Kinderstube des Gehirns offenhalten, die DNA‑Tore richtig abstimmen und die Synapsen widerstandsfähig erhalten.
Zitation: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
Schlüsselwörter: hippokampale Neurogenese, kognitive Resilienz, SuperAgers, Epigenetik, Alzheimer‑Krankheit