Clear Sky Science · tr
Yetişkinlikte, yaşlanmada ve Alzheimer hastalığında insan hipokampal nörojenezi
Yetişkinlerde yeni beyin hücrelerinin önemi
On yıllardır, bilim insanları basit ama derin bir sorunun etrafında tartıştı: erişkin insanların beynin hafıza merkezinde yeni sinir hücreleri üretiyor mu ve eğer üretiyorsa bu hafıza kaybı ve Alzheimer’dan korunmamıza yardımcı oluyor mu? Bu çalışma, en yeni tek hücre teknolojileri ile otopsi sonrası insan beyin dokusunu birleştirerek bu tartışmayı doğrudan ele alıyor ve hipokampustaki yeni doğan nöronların sağlıklı yetişkinlerde, Alzheimer’a giden yolda olan insanlarda, hastalığı olanlarda ve olağanüstü hafızaya sahip nadir yaşlı yetişkinlerde (SuperAgers) nasıl davrandığını gösteriyor.
Beynindeki hafıza yuvası
Beynin derinliklerindeki hipokampusun dentat girusunda, kök hücrelerden yeni nöronların çıkabildiği bir tür hafıza “yuvası” bulunur. Yazarlar, genç yetişkinlerden hafıza performansı ve Alzheimer’a ilişkin değişiklikler bakımından farklı seviyelerde olan yaşlı yetişkinlere kadar uzanan 38 ölü donörün beyinlerinden bu bölgeyi çıkardı. Hem gen aktivitesini hem de DNA’nın ne kadar sıkı paketlendiğini okuyan çoklu-omik tek hücre dizilemesi kullanarak 350.000’den fazla bireysel hücre çekirdeğini analiz ettiler. Bu, nöral kök hücreleri, nöroblastları (erken yeni hücreler) ve olgunlaşmamış granüler nöronları güvenilir şekilde ayırt etmelerini ve bunların hafıza devrelerine katılan tam olgun nöronlara nasıl ilerlediğini haritalamalarını sağladı. Verileri, erişkin insan hipokampusunda yeni nöronların adım adım bir gelişim izleğine sahip olduğu yönünde güçlü destek sunuyor.
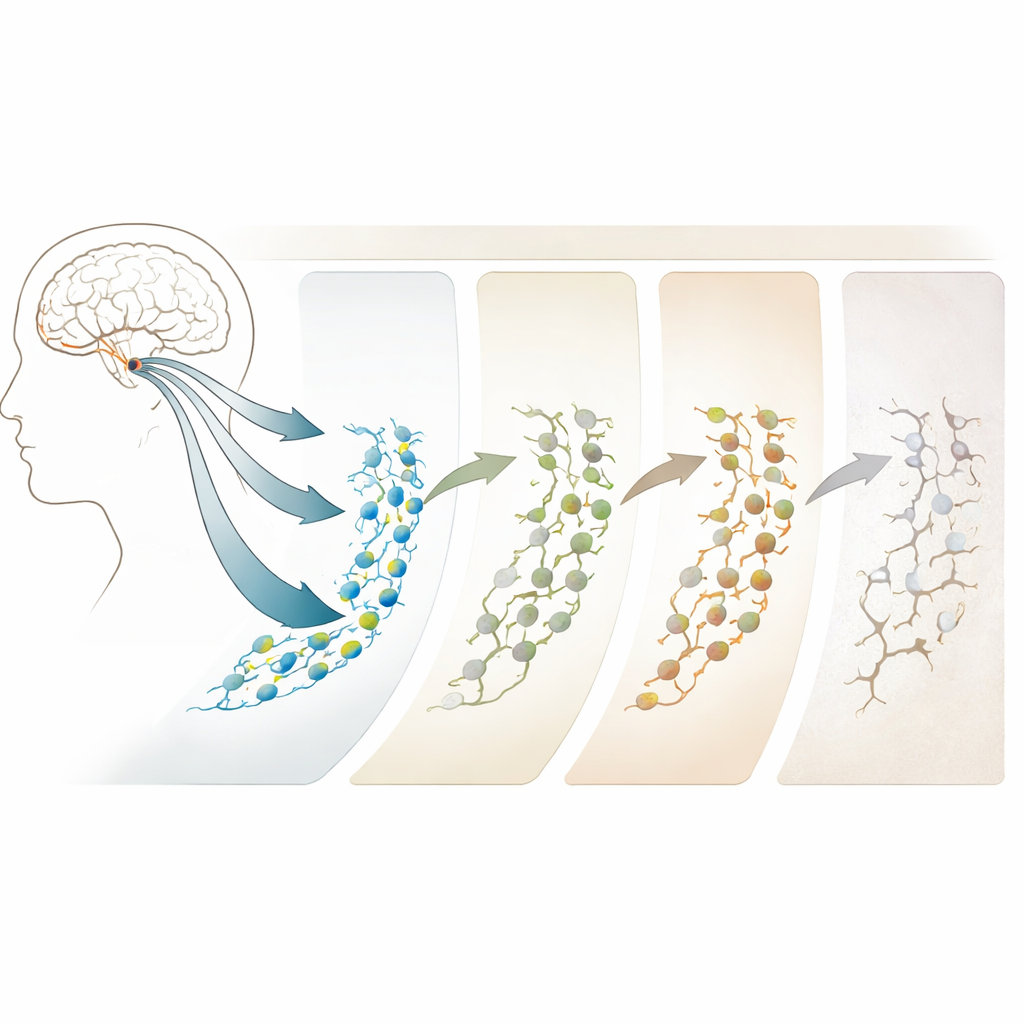
Yaşlanma ve Alzheimer yolunu nasıl büküyor
Genç yetişkinleri yaşlı gruplarla karşılaştırmak, yaşlanma ve Alzheimer’ın nörojenezi basitçe açıp kapatmadığını; bunun yerine onu yeniden şekillendirdiğini gösterdi. Klinik öncesi ara patolojiye sahip kişilerde—normal yaşlanmadan Alzheimer’a geçişte gibi görünen bireylerde—kök hücre sayısı aslında artarken nörojenezin sonraki aşamaları zayıflamaya başlıyor. Tam Alzheimer hastalığında ise nöroblastlar ve olgunlaşmamış nöronlar belirgin şekilde azalıyor, buna karşın kök hücre benzeri hücreler daha bol bulunuyor. Çarpıcı biçimde, en tutarlı değişiklikler genlerin kendisinde değil, hangi genlerin kullanılabileceğini kontrol eden kapılar gibi açılıp kapanan DNA bölgelerinin erişilebilirliğinde ortaya çıkıyor. Özellikle sinapslar ve nöronal yapı ile ilişkili bu epigenetik değişimler erken dönemde beliriyor ve hastalıkla yoğunlaşıyor; bu da onları potansiyel erken uyarı işaretleri ve tedavi hedefleri haline getiriyor.
Dirençlilik için moleküler parmak izleri
80’li yaşlarda ve üzerindeki, genç yetişkinler kadar iyi hatırlayan SuperAgers, dirençliliğe dair bir pencere sundu. Onların hipokampuslarında Alzheimer hastalarınınkinden ve sık sık tipik yaşlı yetişkinlerinkinden anlamlı derecede daha fazla nöroblast ve olgunlaşmamış nöron vardı. Kök hücrelerdeki büyük değişikliklerden ziyade kilit farklar, nöroblastlar ve olgunlaşmamış nöronlarda daha açık olan binlerce DNA bölgesinde yatıyordu; bu durum sağlam büyümeyi ve sinaptik işlevi destekliyordu. Ekip, genç yetişkinlerde, sağlıklı yaşlanmada ve SuperAgers’ta stabil kalan ancak Alzheimer’da çöken genleri ve DNA bölgelerini yakalayan bir “direnç puanı” tanımladı. Bunların birçoğu nöronal bağlantıları ve etkili iletişimi sürdürmeyle ilişkilidir. SuperAgers ayrıca düzenleyici ağlarda—kontrol proteinleri ve DNA anahtarlarının kombinasyonlarında—genç yetişkinlere benzer yönler taşıyan ancak yeni doğan nöronları özellikle dayanıklı, uzun ömürlü bir duruma itebilecek benzersiz aktivatörleri de içeren ayırt edici bir desen gösterdi.
Başarılı ile başarısız yaşlanmayı işaretleyen devreler
Çalışma sadece yeni doğan nöronlarla sınırlı kalmadı. Tüm ana hücre tiplerini inceleyerek, bilişsel korunmayı veya aşınmayı belirleyen sinyallerin iki kilit oyuncuda yoğunlaştığını buldular: CA1 nöronları (hipokampusun temel çıkış istasyonlarından biri) ve astroglia (kimyasal ortamı yöneten ve sinapsları düzenlemeye yardımcı olan destek hücreleri). Başarılı yaşlanma ve SuperAgers’ta CA1 nöronlarındaki genler güçlü sinaptik iletim, enerji üretimi ve hücresel temizlik yollarını desteklerken, astroglialar koruyucu yanıtlara elverişli kromatin desenleri gösteriyordu. Alzheimer’a doğru ilerleyen kişilerde bu aynı yollar ters yönde kayıyordu. Hücreler arası iletişim analizleri, preklinik ve Alzheimer gruplarında CA1 nöronları, astroglialar ve nörojenezik hücreler arasındaki adezyon ve glutamat temelli sinyalleşmenin zayıfladığını vurgulayarak, uyarıcı sinapsların bozulmasının bilişsel gerilemenin ortak bir işareti olduğunu düşündürüyor.
Hafızayı korumak için ne anlama geliyor
Bir araya getirildiğinde sonuçlar ayrıntılı bir tablo çiziyor: erişkin insanlarda hipokampal yeni nöron üretimi devam ediyor, ancak bu süreç yaşa ve hastalığa son derece duyarlı. En erken ve en güçlü değişiklikler, DNA’nın paketlenme biçimi olan kromatin erişilebilirliği düzeyinde gerçekleşiyor—birçok genin faaliyetinde belirgin değişiklikler ortaya çıkmadan çok önce. SuperAgers gibi dirençli beyinlerde moleküler ağlar, ileri yaşa rağmen nörojenezi ve sinaptik iletişimi “genç” bir modda tutuyor. Savunmasız beyinlerde ise aynı ağlar kayıyor, yeni nöronların gelişimi duruyor ve hipokampal devreler çözülüyor. Bu epigenetik ve hücresel imzaları ortaya koyarak çalışma, bir gün hafızayı koruyabilecek stratejilere işaret ediyor: sadece plakları temizlemeye yönelik değil, beynin hafıza yuvasını açık tutmayı, DNA kapılarını doğru şekilde ayarlamayı ve sinapsları dayanıklı kılmayı hedefleyen terapiler.
Atıf: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
Anahtar kelimeler: hipokampal nörojenez, bilişsel direnç, SuperAgers, epigenetik, Alzheimer hastalığı