Clear Sky Science · pt
Neurogênese hipocampal humana na idade adulta, no envelhecimento e na doença de Alzheimer
Por que novos neurônios em adultos importam
Por décadas, cientistas debateram uma questão simples, mas profunda: humanos adultos geram novos neurônios no centro da memória do cérebro e, em caso afirmativo, isso ajuda a nos proteger da perda de memória e da doença de Alzheimer? Este estudo enfrenta esse debate diretamente ao combinar ferramentas unicelulares de ponta e tecido cerebral humano pós‑morte para mostrar como os neurônios recém‑formados no hipocampo se comportam em adultos saudáveis, em pessoas no caminho para o Alzheimer, em pacientes com a doença e em raros idosos com memória excepcional conhecidos como SuperAgers.
O berçário de memórias do cérebro
No interior do hipocampo está o giro denteado, uma espécie de “berçário” de memória onde novos neurônios podem surgir a partir de células‑tronco residentes. Os autores dissecaram essa região dos cérebros de 38 doadores falecidos, com idades que vão de adultos jovens a idosos com diferentes níveis de desempenho de memória e alterações relacionadas ao Alzheimer. Usando sequenciamento unicelular multiômico — que lê tanto a atividade gênica quanto o grau de compactação do DNA — eles analisaram mais de 350.000 núcleos celulares individuais. Isso permitiu distinguir com confiança células‑tronco neurais, neuroblastos (células recém‑nascidas em estágio inicial) e neurônios granulosos imaturos, e mapear como esses progridem para neurônios totalmente maduros que integram circuitos de memória. Seus dados dão suporte sólido à existência de uma trajetória de desenvolvimento em etapas de novos neurônios no hipocampo humano adulto.
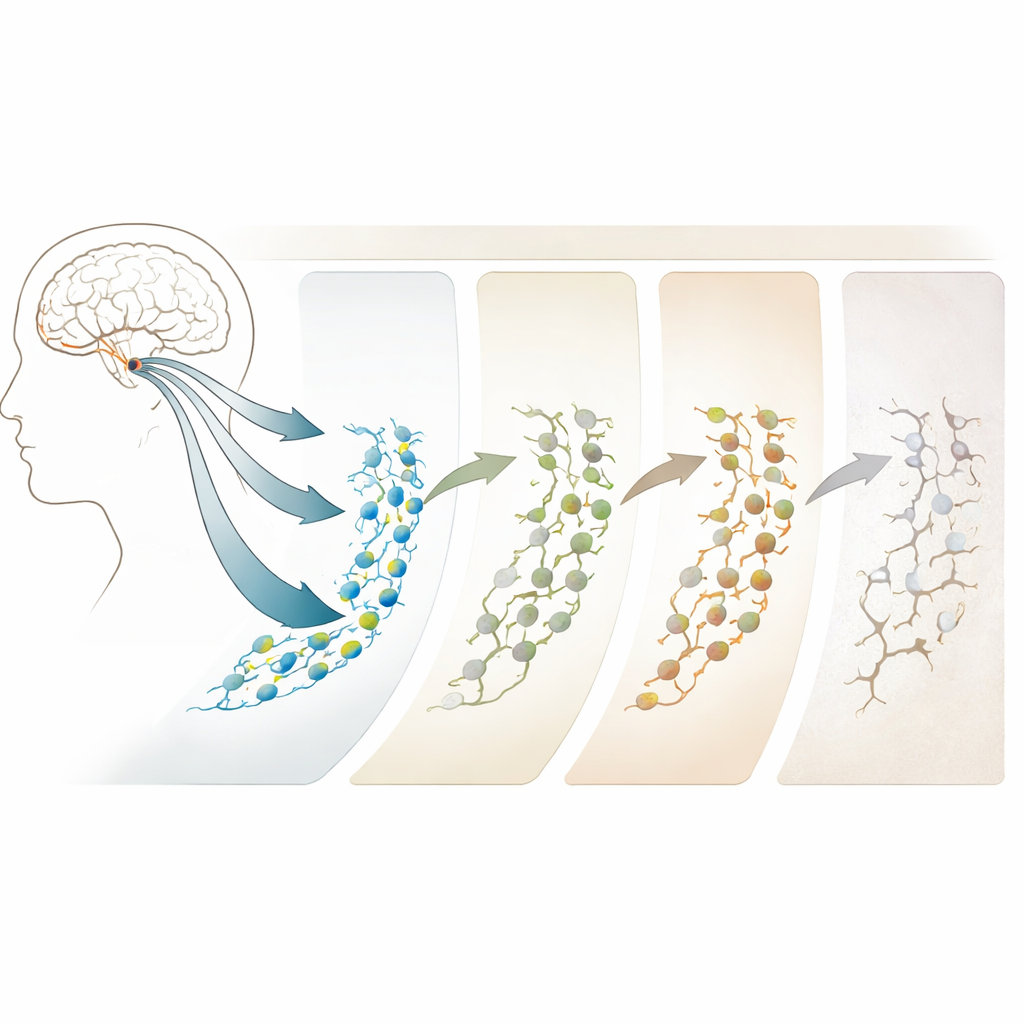
Como a idade e o Alzheimer moldam a trajetória
Ao comparar adultos jovens com grupos mais velhos, ficou claro que envelhecimento e Alzheimer não simplesmente ligam ou desligam a neurogênese; em vez disso, os modificam. Em pessoas com patologia intermediária pré‑clínica — indivíduos que parecem estar em transição do envelhecimento normal para o Alzheimer — o número de células‑tronco na verdade aumenta, mas as fases finais da neurogênese começam a falhar. Na doença de Alzheimer estabelecida, neuroblastos e neurônios imaturos estão marcadamente reduzidos, embora células com características de células‑tronco sejam mais abundantes. Notavelmente, as mudanças mais consistentes não acontecem nos genes em si, mas em regiões do DNA que se tornam mais ou menos acessíveis, como portões que se abrem ou fecham para controlar quais genes podem ser utilizados. Essas alterações epigenéticas, especialmente em regiões ligadas a sinapses e à estrutura neuronal, surgem cedo e se intensificam com a doença, tornando‑se potenciais sinais de alerta precoce e alvos terapêuticos.
As impressões moleculares da resiliência
SuperAgers — pessoas na faixa dos 80 anos ou mais que lembram tão bem quanto adultos muito mais jovens — ofereceram uma janela sobre a resiliência. Seus hipocampos continham significativamente mais neuroblastos e neurônios imaturos do que os de pacientes com Alzheimer, e frequentemente mais do que os de idosos típicos. Em vez de mudanças massivas nas células‑tronco, as diferenças-chave residiam em milhares de regiões do DNA que estavam mais abertas em neuroblastos e neurônios imaturos, sustentando crescimento robusto e função sináptica. A equipe definiu uma “pontuação de resiliência” que captura genes e regiões de DNA que permanecem estáveis em adultos jovens, envelhecedores saudáveis e SuperAgers, mas desmoronam no Alzheimer. Muitos desses elementos estão vinculados à manutenção de conexões neuronais e à comunicação eficiente. SuperAgers também exibiram um padrão distinto de redes regulatórias — combinações de proteínas de controle e interruptores de DNA — que em alguns aspectos se assemelham aos adultos jovens, mas que também incluem ativadores únicos que podem direcionar os neurônios recém‑formados a um estado particularmente robusto e duradouro.
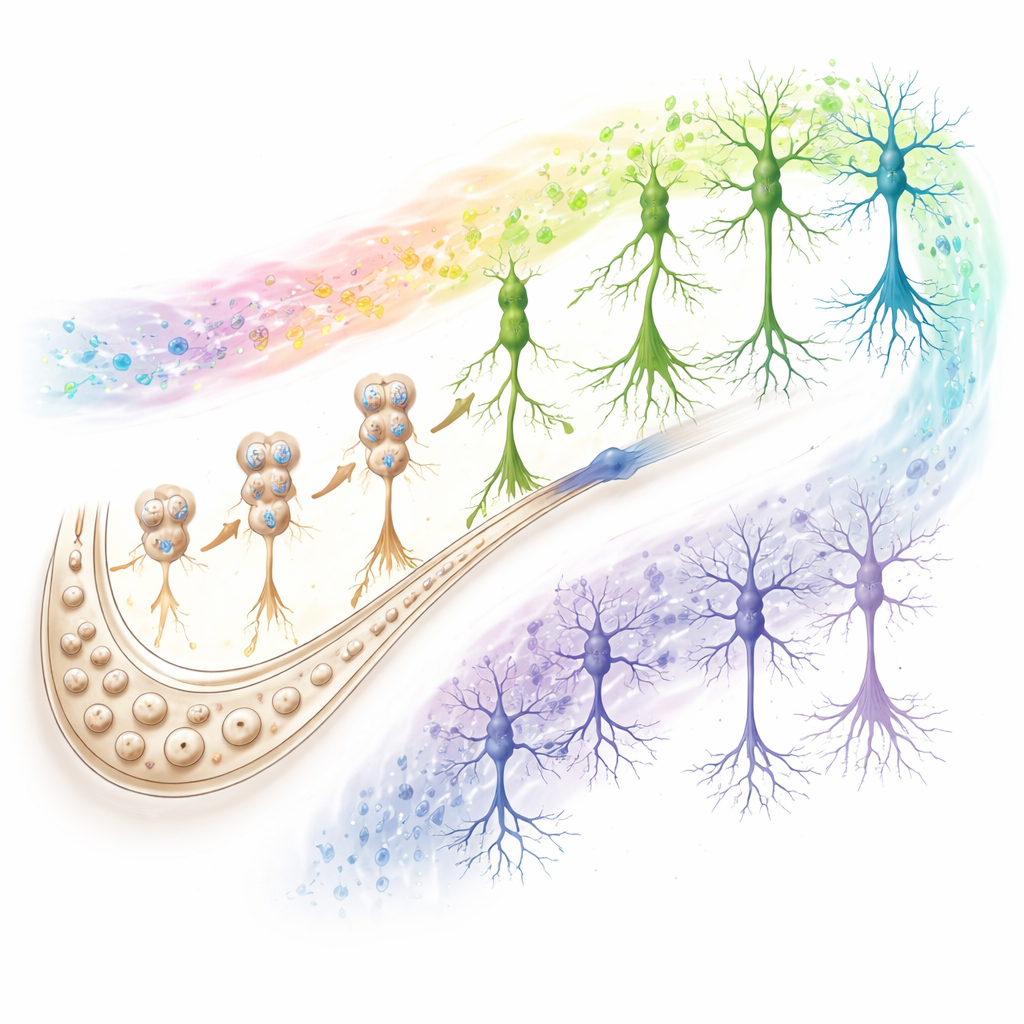
Circuitos que marcam envelhecimento bem‑sucedido versus em declínio
O estudo não se limitou aos neurônios recém‑formados. Ao examinar todos os principais tipos celulares, os autores descobriram que sinais que preservam ou erodem a cognição se concentram em dois protagonistas: neurônios CA1 (uma estação de saída central do hipocampo) e astrócitos (células de suporte que gerenciam o ambiente químico e ajudam a regular sinapses). Em envelhecedores bem‑sucedidos e SuperAgers, genes em neurônios CA1 sustentam forte transmissão sináptica, produção de energia e vias de limpeza celular, enquanto astrócitos mostram padrões de cromatina que favorecem respostas protetoras. Em pessoas no caminho para o Alzheimer, essas mesmas vias dérivam na direção oposta. Análises da comunicação célula a célula destacaram adesão enfraquecida e sinalização baseada em glutamato entre neurônios CA1, astrócitos e células neurogênicas em grupos pré‑clínicos e com Alzheimer, sugerindo que a ruptura de sinapses excitatórias é uma marca comum do declínio cognitivo.
O que isso significa para proteger a memória
Em conjunto, os resultados desenham um quadro detalhado: humanos adultos continuam a gerar novos neurônios hipocampais, mas esse processo é extremamente sensível à idade e à doença. As mudanças mais precoces e robustas ocorrem no nível da acessibilidade da cromatina — a forma como o DNA é empacotado — muito antes de muitos genes alterarem visivelmente sua atividade. Em cérebros resilientes, como os de SuperAgers, redes moleculares mantêm a neurogênese e a comunicação sináptica em um modo “juvenil” apesar da idade avançada. Em cérebros vulneráveis, essas mesmas redes mudam, levando ao desenvolvimento interrompido de novos neurônios e ao desgaste dos circuitos hipocampais. Ao revelar essas assinaturas epigenéticas e celulares, o estudo aponta para estratégias que talvez um dia preservem a memória: terapias voltadas não apenas para remover placas, mas para manter o berçário de memória do cérebro aberto, seus portões de DNA corretamente ajustados e suas sinapses resilientes.
Citação: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
Palavras-chave: neurogênese hipocampal, resiliência cognitiva, SuperAgers, epigenética, doença de Alzheimer