Clear Sky Science · es
Neurogénesis hipocampal humana en la edad adulta, el envejecimiento y la enfermedad de Alzheimer
Por qué importan las nuevas neuronas en adultos
Durante décadas, los científicos han debatido una pregunta sencilla pero profunda: ¿los humanos adultos generan nuevas neuronas en el centro de la memoria del cerebro y, de ser así, esto ayuda a protegernos de la pérdida de memoria y de la enfermedad de Alzheimer? Este estudio aborda ese debate de frente combinando herramientas de vanguardia a nivel de una sola célula y tejido cerebral humano post mortem para mostrar cómo se comportan las neuronas recién formadas en el hipocampo de adultos sanos, de personas en la trayectoria hacia el Alzheimer, de pacientes con la enfermedad y de unos pocos adultos mayores con memoria excepcional conocidos como SuperAgers.
La guardería de la memoria del cerebro
En lo profundo del hipocampo se encuentra el giro dentado, una especie de “guardería” de la memoria donde nuevas neuronas pueden surgir a partir de células madre residentes. Los autores diseccionaron esta región de los cerebros de 38 donantes fallecidos, que iban desde adultos jóvenes hasta adultos mayores con distintos niveles de rendimiento de la memoria y cambios asociados al Alzheimer. Utilizando secuenciación multiómica de una sola célula—que lee tanto la actividad génica como el grado de empaquetamiento del ADN—analizaron más de 350.000 núcleos celulares individuales. Esto les permitió distinguir con fiabilidad células madre neuronales, neuroblastos (células recién nacidas en etapas tempranas) y neuronas granulares inmaduras, y cartografiar cómo progresan hacia neuronas plenamente maduras que se integran en los circuitos de la memoria. Sus datos respaldan de forma contundente la existencia de una trayectoria de desarrollo por etapas de nuevas neuronas en el hipocampo humano adulto.
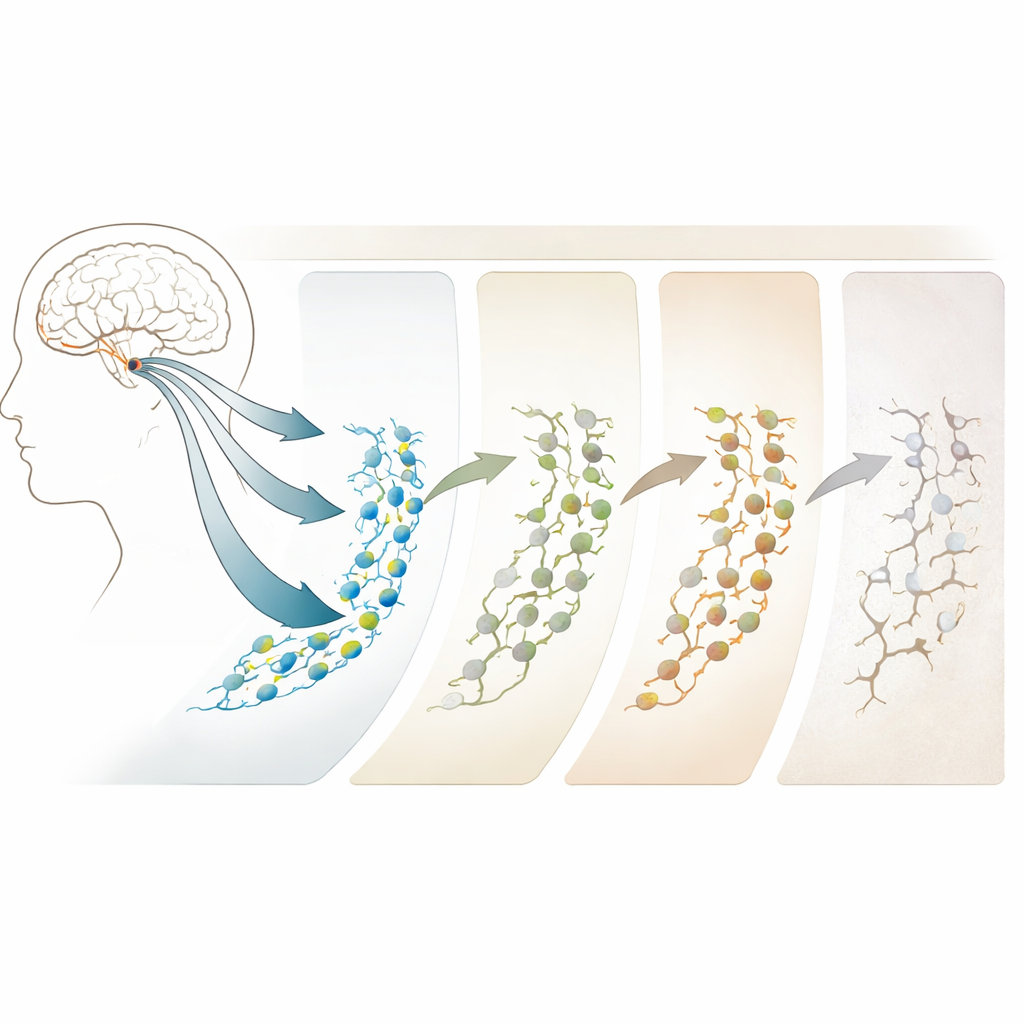
Cómo la edad y el Alzheimer moldean la trayectoria
Al comparar adultos jóvenes con grupos de mayor edad se observó que el envejecimiento y el Alzheimer no simplemente activan o desactivan la neurogénesis; en cambio, la remodelan. En personas con patología intermedia preclínica—individuos que parecen estar en transición del envejecimiento normal hacia el Alzheimer—el número de células madre aumenta en realidad, pero las etapas posteriores de la neurogénesis comienzan a fallar. En la enfermedad de Alzheimer plena, los neuroblastos y las neuronas inmaduras están marcadamente reducidos, aunque las células con aspecto de células madre son más abundantes. De forma llamativa, los cambios más consistentes no se encuentran tanto en los genes en sí, sino en regiones del ADN que se vuelven más o menos accesibles, como puertas que se abren o cierran para controlar qué genes pueden utilizarse. Estos cambios epigenéticos, especialmente en regiones vinculadas a las sinapsis y la estructura neuronal, emergen temprano y se intensifican con la enfermedad, lo que los señala como posibles indicadores tempranos y dianas terapéuticas.
Las huellas moleculares de la resiliencia
Los SuperAgers—personas de 80 años o más que recuerdan tan bien como adultos mucho más jóvenes—ofrecieron una ventana hacia la resiliencia. Sus hipocampos contenían significativamente más neuroblastos y neuronas inmaduras que los de pacientes con Alzheimer, y a menudo más que los de adultos mayores típicos. En lugar de cambios masivos en las células madre, las diferencias clave residían en miles de regiones del ADN que estaban más abiertas en neuroblastos y neuronas inmaduras, favoreciendo un crecimiento robusto y la función sináptica. El equipo definió una «puntuación de resiliencia» que captura genes y regiones del ADN que permanecen estables en adultos jóvenes, en envejecimiento saludable y en SuperAgers, pero que colapsan en el Alzheimer. Muchos de estos están vinculados al mantenimiento de las conexiones neuronales y a una comunicación eficiente. Los SuperAgers también mostraron un patrón distintivo de redes regulatorias—combinaciones de proteínas reguladoras y interruptores del ADN—que en ciertos aspectos se asemeja al de los adultos jóvenes, pero que además incluye activadores únicos que podrían empujar a las neuronas recién formadas hacia un estado especialmente robusto y duradero.
Circuitos que marcan envejecimiento exitoso frente al que falla
El estudio no se detuvo en las neuronas recién nacidas. Al examinar todos los tipos celulares principales, los autores encontraron que las señales que preservan o erosionan la cognición se concentran en dos actores clave: las neuronas CA1 (una estación de salida central del hipocampo) y los astrocitos (células de soporte que gestionan el entorno químico y ayudan a regular las sinapsis). En las personas que envejecen con éxito y en los SuperAgers, los genes en las neuronas CA1 apoyan una transmisión sináptica fuerte, producción de energía y vías de limpieza celular, mientras que los astrocitos muestran patrones de cromatina que favorecen respuestas protectoras. En personas en la vía hacia el Alzheimer, esas mismas vías derivan en la dirección opuesta. Los análisis de la comunicación célula a célula destacaron una adhesión debilitada y una señalización basada en glutamato entre neuronas CA1, astrocitos y células neurogénicas en los grupos preclínicos y con Alzheimer, lo que sugiere que el deterioro de las sinapsis excitatorias es una característica compartida del declive cognitivo.
Qué significa esto para proteger la memoria
En conjunto, los resultados dibujan un retrato detallado: los humanos adultos continúan generando nuevas neuronas hipocampales, pero este proceso es exquisitamente sensible a la edad y a la enfermedad. Los cambios más tempranos y robustos ocurren a nivel de la accesibilidad de la cromatina—la forma en que se empaqueta el ADN—mucho antes de que muchos genes cambien visiblemente su actividad. En cerebros resilientes, como los de los SuperAgers, las redes moleculares mantienen la neurogénesis y la comunicación sináptica en un modo «juvenil» pese a la avanzada edad. En cerebros vulnerables, esas mismas redes se desplazan, lo que lleva al estancamiento del desarrollo de nuevas neuronas y al deshilachamiento de los circuitos hipocampales. Al revelar estas firmas epigenéticas y celulares, el estudio apunta hacia estrategias que podrían algún día preservar la memoria: terapias dirigidas no solo a eliminar placas, sino a mantener abierta la guardería de la memoria del cerebro, a afinar las puertas del ADN y a fortalecer la resistencia de las sinapsis.
Cita: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
Palabras clave: neurogénesis hipocampal, resiliencia cognitiva, SuperAgers, epigenética, enfermedad de Alzheimer