Clear Sky Science · it
Neurogenesi ippocampale umana in età adulta, invecchiamento e malattia di Alzheimer
Perché i nuovi neuroni negli adulti sono importanti
Per decenni gli scienziati si sono confrontati su una domanda semplice ma profonda: gli esseri umani adulti generano nuovi neuroni nel centro della memoria del cervello e, in tal caso, questo aiuta a proteggerci dalla perdita di memoria e dalla malattia di Alzheimer? Questo studio affronta direttamente il dibattito combinando strumenti single‑cell all’avanguardia e tessuto cerebrale umano post‑mortem per mostrare come si comportano i neuroni neonati nell’ippocampo di adulti sani, di persone in cammino verso l’Alzheimer, di pazienti con la malattia e di rari anziani con memoria eccezionale noti come SuperAgers.
La “nursery” della memoria nel cervello
In profondità nell’ippocampo si trova la giro dentato, una sorta di “nursery” della memoria dove nuovi neuroni possono originare da cellule staminali residenti. Gli autori hanno dissezionato questa regione dai cervelli di 38 donatori deceduti, da giovani adulti fino ad anziani con differenti livelli di prestazione mnemonica e cambiamenti legati all’Alzheimer. Utilizzando sequenziamento multiomico single‑cell—che legge sia l’attività genica sia il grado di impacchettamento del DNA—hanno analizzato oltre 350.000 nuclei cellulari individuali. Questo ha permesso di distinguere in modo affidabile le cellule staminali neurali, i neuroblasti (prime cellule neonate) e i neuroni granulari immaturi, e di mappare come progrediscono verso neuroni pienamente maturi che si integrano nei circuiti della memoria. I loro dati supportano con forza l’esistenza di una traiettoria di sviluppo graduale dei nuovi neuroni nell’ippocampo umano adulto.
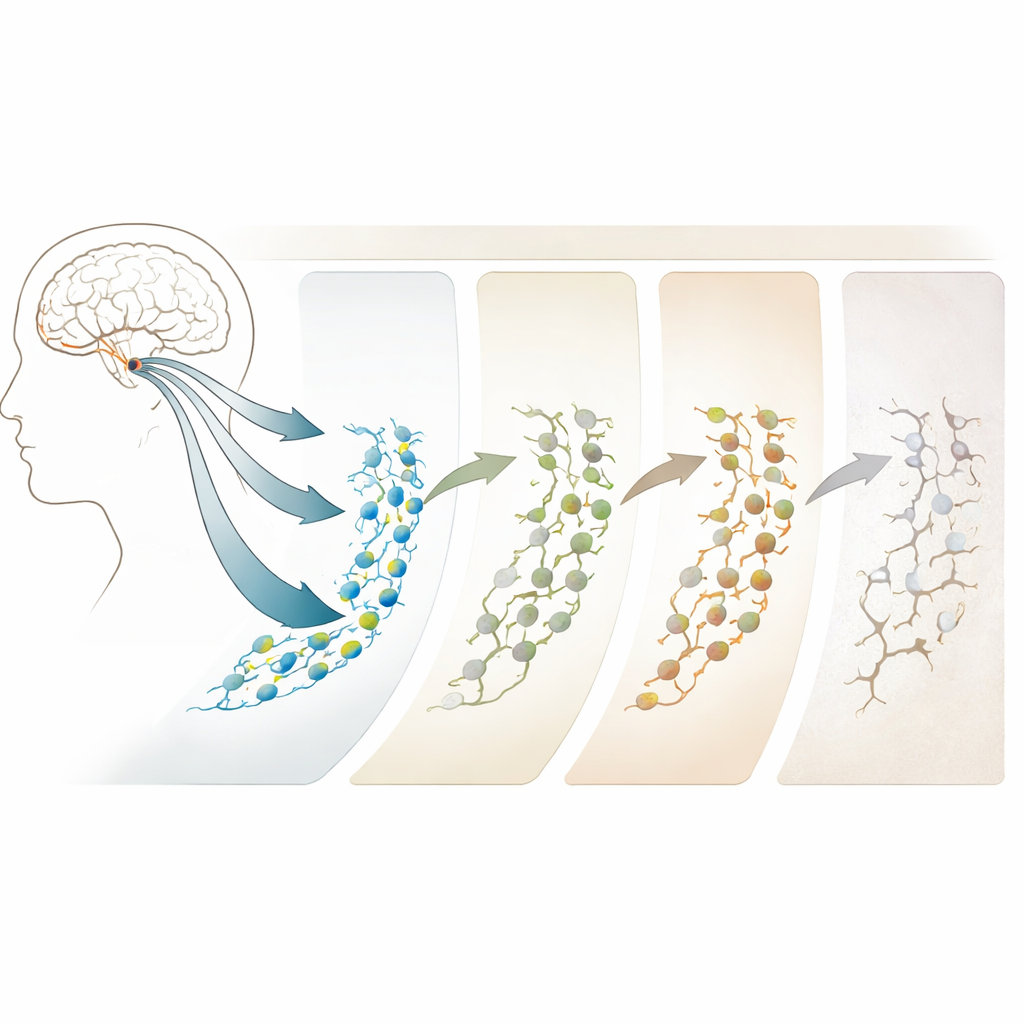
Come età e Alzheimer rimodellano la traiettoria
Il confronto tra giovani adulti e gruppi più anziani ha rivelato che invecchiamento e Alzheimer non semplicemente accendono o spengono la neurogenesi; piuttosto, la rimodellano. Nelle persone con patologia intermedia preclinica—individui che sembrano transitare dall’invecchiamento normale verso l’Alzheimer—il numero di cellule staminali aumenta in realtà, ma le fasi successive della neurogenesi cominciano a vacillare. Nella malattia di Alzheimer conclamata, i neuroblasti e i neuroni immaturi risultano fortemente ridotti, nonostante le cellule di tipo staminale siano più abbondanti. È sorprendente che i cambiamenti più coerenti non avvengano nei geni stessi, ma in regioni del DNA che diventano più o meno accessibili, come cancelli che si aprono o chiudono per controllare quali geni possono essere utilizzati. Questi spostamenti epigenetici, in particolare nelle regioni legate alle sinapsi e alla struttura neuronale, emergono precocemente e si intensificano con la malattia, candidandosi come potenziali segnali d’allarme precoci e bersagli terapeutici.
Le impronte molecolari della resilienza
I SuperAgers—persone dagli ottanta anni in su che ricordano altrettanto bene quanto adulti molto più giovani—offrono una finestra sulla resilienza. I loro ippocampi contenevano un numero significativamente maggiore di neuroblasti e neuroni immaturi rispetto ai pazienti con Alzheimer, e spesso più dei normali anziani. Piuttosto che cambiamenti massicci nelle cellule staminali, le differenze chiave risiedevano in migliaia di regioni di DNA più aperte nei neuroblasti e nei neuroni immaturi, a supporto di una crescita robusta e della funzione sinaptica. Il team ha definito un “punteggio di resilienza” che cattura geni e regioni di DNA stabili nei giovani adulti, negli anziani sani e nei SuperAgers ma che collassano nell’Alzheimer. Molti di questi sono legati al mantenimento delle connessioni neuronali e alla comunicazione efficiente. I SuperAgers hanno inoltre mostrato un modello distinto di reti regolatorie—combinazioni di proteine di controllo e interruttori del DNA—that in alcuni aspetti ricorda i giovani adulti ma include anche attivatori unici che potrebbero spingere i neuroni neonati verso uno stato particolarmente robusto e duraturo.
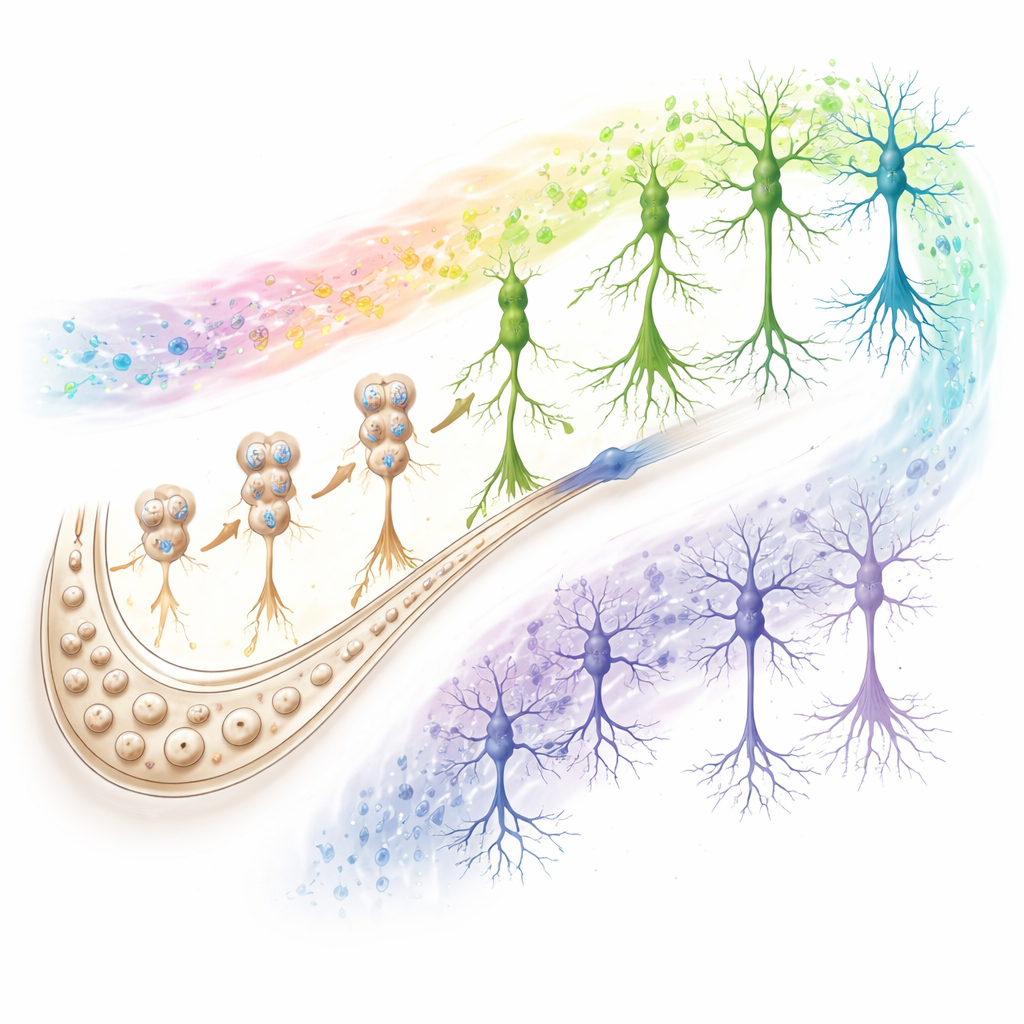
Circuiti che distinguono invecchiamento riuscito da quello fallimentare
Lo studio non si è fermato ai neuroni neonati. Esaminando tutti i principali tipi cellulari, gli autori hanno scoperto che i segnali che preservano o erodono la cognizione si concentrano in due protagonisti chiave: i neuroni CA1 (una stazione di uscita centrale dell’ippocampo) e gli astrociti (cellule di supporto che gestiscono l’ambiente chimico e aiutano a regolare le sinapsi). Negli anziani con invecchiamento riuscito e nei SuperAgers, i geni nei neuroni CA1 supportano una forte trasmissione sinaptica, la produzione di energia e i percorsi di pulizia cellulare, mentre gli astrociti mostrano pattern di cromatina che favoriscono risposte protettive. Nelle persone sulla strada verso l’Alzheimer, questi stessi percorsi virano nella direzione opposta. Le analisi della comunicazione cellula‑cellula hanno evidenziato un indebolimento dell’adesione e della segnalazione basata sul glutammato tra neuroni CA1, astrociti e cellule neurogene nei gruppi preclinici e Alzheimer, suggerendo che il collasso delle sinapsi eccitatorie sia un tratto comune del declino cognitivo.
Cosa significa per la protezione della memoria
Complessivamente, i risultati dipingono un quadro dettagliato: gli esseri umani adulti continuano a generare nuovi neuroni ippocampali, ma questo processo è estremamente sensibile all’età e alla malattia. I cambiamenti più precoci e robusti avvengono a livello dell’accessibilità della cromatina—il modo in cui il DNA è impacchettato—molto prima che molti geni modifichino visibilmente la loro attività. Nei cervelli resilienti, come quelli dei SuperAgers, reti molecolari mantengono la neurogenesi e la comunicazione sinaptica in uno stato “giovanile” nonostante l’età avanzata. Nei cervelli vulnerabili, queste stesse reti si spostano, portando a uno stallo nello sviluppo dei nuovi neuroni e all’usura dei circuiti ippocampali. Rivelando queste firme epigenetiche e cellulari, lo studio indica strategie che un giorno potrebbero preservare la memoria: terapie mirate non solo a rimuovere le placche, ma a mantenere aperta la nursery della memoria del cervello, a regolare correttamente i cancelli del DNA e a rendere le sinapsi più resilienti.
Citazione: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
Parole chiave: neurogenesi ippocampale, resilienza cognitiva, SuperAgers, epigenetica, malattia di Alzheimer