Clear Sky Science · nl
Hippocampale neurogenese bij volwassenen, veroudering en de ziekte van Alzheimer
Waarom nieuwe hersencellen bij volwassenen ertoe doen
Decennialang hebben wetenschappers gedebatteerd over een eenvoudige maar ingrijpende vraag: maken volwassenen nieuwe hersencellen in het geheugencentrum van de hersenen, en zo ja, helpt dat ons beschermen tegen geheugenverlies en de ziekte van Alzheimer? Deze studie pakt dat debat frontaal aan door geavanceerde enkelceltechnieken te combineren met post‑mortem menselijk hersenweefsel om te laten zien hoe pasgeboren neuronen in de hippocampus zich gedragen bij gezonde volwassenen, bij mensen die op weg zijn naar Alzheimer, bij patiënten met de ziekte en bij zeldzame oudere volwassenen met uitzonderlijk geheugen, de zogeheten SuperAgers.
De geheugenkwekerij van de hersenen
Diep in de hippocampus ligt de gyrus dentatus, een soort geheugen "kwekerij" waaruit nieuwe neuronen kunnen ontstaan uit residentiële stamcellen. De auteurs dissecteerden deze regio uit de hersenen van 38 overleden donors, variërend van jongvolwassenen tot oudere volwassenen met uiteenlopende geheugenprestaties en Alzheimer‑gerelateerde veranderingen. Met multiomische enkelcelsequencing—die zowel genactiviteit als de mate van DNA‑oppakking leest—analyseeerden ze meer dan 350.000 individuele celnuclei. Dit stelde hen in staat betrouwbaar neurale stamcellen, neuroblasten (vroegste pasgeboren cellen) en immature korrelcellen te onderscheiden, en te karten hoe deze uitgroeien tot volledig rijpe neuronen die zich aansluiten bij geheugencircuits. Hun gegevens ondersteunen duidelijk het bestaan van een stapsgewijze ontwikkelingsbaan van nieuwe neuronen in de volwassen menselijke hippocampus.
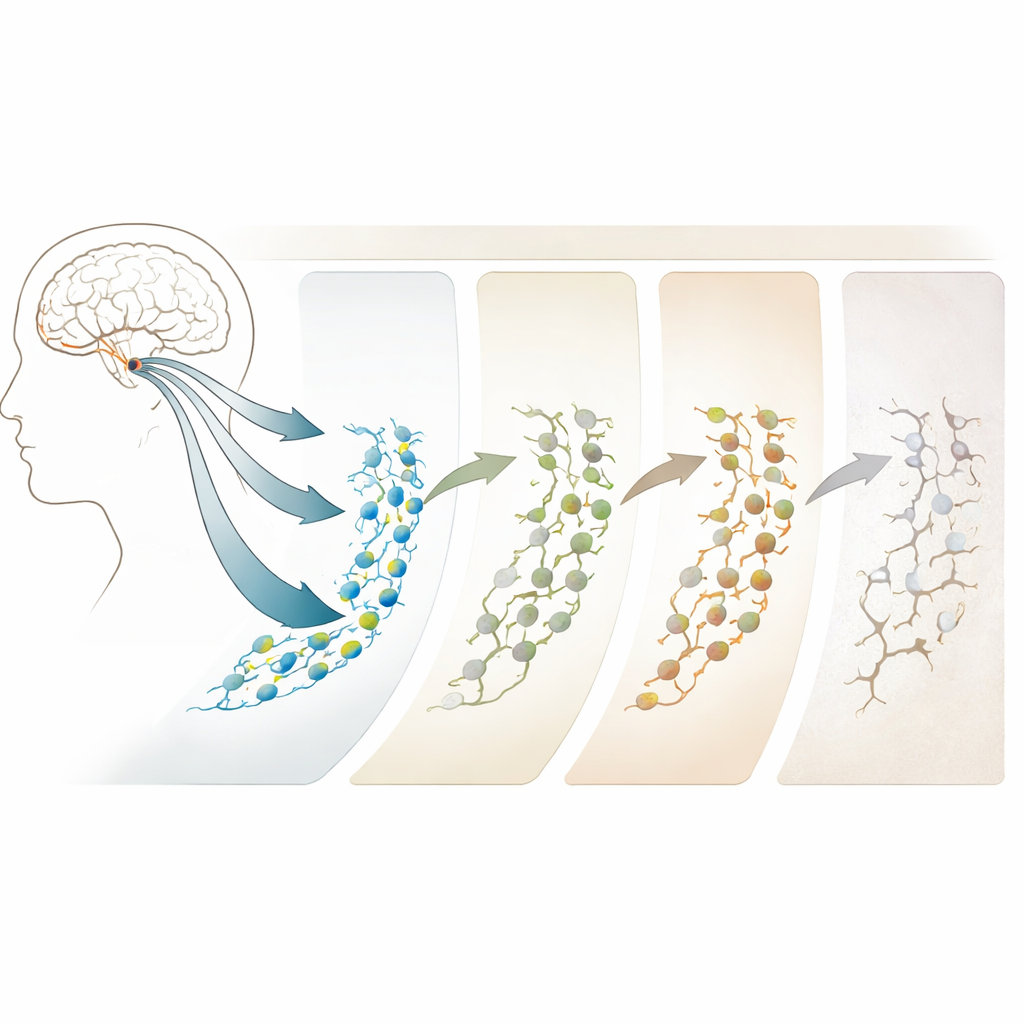
Hoe leeftijd en Alzheimer de baan buigen
Vergelijking van jongvolwassenen met oudere groepen toonde aan dat veroudering en Alzheimer neurogenese niet simpelweg aan of uit zetten; ze herschikken het proces. Bij mensen met preklinische intermediaire pathologie—individuen die lijken over te gaan van normaal ouder worden naar Alzheimer—neemt het aantal stamcellen juist toe, maar de latere stadia van neurogenese beginnen te haperen. Bij manifeste Alzheimer zijn neuroblasten en immature neuronen opvallend verminderd, zelfs wanneer stamcelachtige cellen overvloediger zijn. Opvallend is dat de meest consistente veranderingen niet in de genen zelf zitten, maar in DNA‑regio's die meer of minder toegankelijk worden, als poorten die openen of sluiten om te bepalen welke genen gebruikt kunnen worden. Deze epigenetische verschuivingen, vooral in regio's die gekoppeld zijn aan synapsen en neuronale structuur, doen zich vroeg voor en verergeren met de ziekte, waardoor ze mogelijke vroege waarschuwingstekens en therapeutische doelen vormen.
De moleculaire vingerafdrukken van veerkracht
SuperAgers—mensen van in de tachtig en ouder die onthouden net zo goed als veel jongere volwassenen—boden zicht op veerkracht. Hun hippocampi bevatten aanzienlijk meer neuroblasten en immature neuronen dan die van Alzheimerpatiënten, en vaak meer dan typische ouderen. In plaats van ingrijpende veranderingen in stamcellen lagen de belangrijkste verschillen in duizenden DNA‑regio's die bij neuroblasten en immature neuronen meer open waren, wat robuuste groei en synaptische functie ondersteunt. Het team definieerde een "veerkrachtscore" die genen en DNA‑regio's vangt die stabiel blijven bij jongvolwassenen, gezonde ouderen en SuperAgers maar instorten bij Alzheimerpatiënten. Veel daarvan zijn verbonden met het behouden van neuronale verbindingen en efficiënte communicatie. SuperAgers toonden ook een onderscheidend patroon van regelnetwerken—combinaties van controleproteïnen en DNA‑schakelaars—dat in sommige opzichten op jongvolwassenen lijkt maar ook unieke activatoren bevat die pasgeboren neuronen naar een bijzonder robuuste, langdurige staat kunnen duwen.
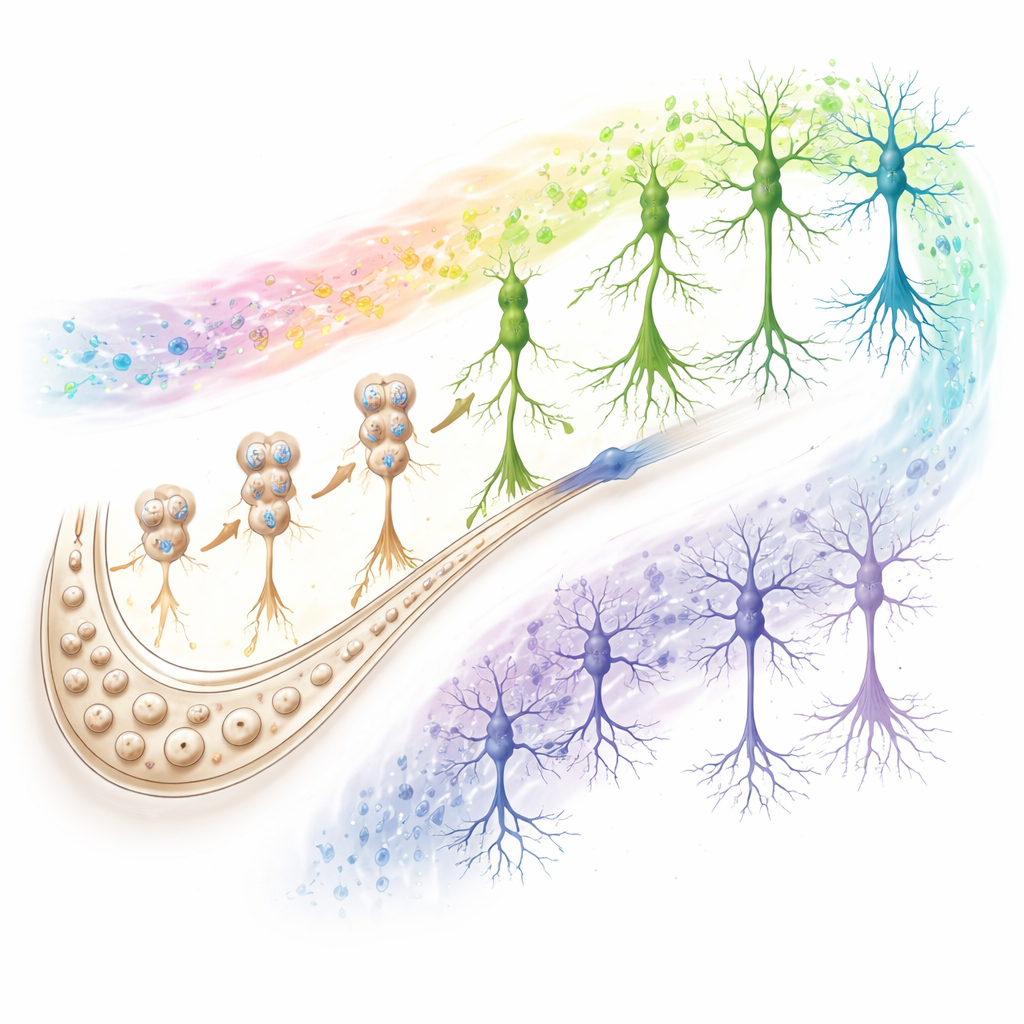
Circuits die succesvol tegenover falend ouder worden markeren
De studie stopte niet bij pasgeboren neuronen. Door alle belangrijke celtypen te onderzoeken, vonden de auteurs dat signalen die cognitie behouden of ondermijnen geconcentreerd zijn in twee sleutelspelers: CA1‑neuronen (een kernuitgangsstation van de hippocampus) en astrocyten (ondersteunende cellen die de chemische omgeving beheren en helpen synapsen te reguleren). Bij succesvolle oudworders en SuperAgers ondersteunen genen in CA1‑neuronen sterke synaptische transmissie, energieproductie en cellulaire opruimroutes, terwijl astrocyten chromatinepatronen vertonen die beschermende reacties bevorderen. Bij mensen op weg naar Alzheimer kantelen dezezelfde routes in de tegenovergestelde richting. Analyses van cel‑tot‑celcommunicatie benadrukten verzwakte adhesie en glutamaatgebaseerde signalering tussen CA1‑neuronen, astrocyten en neurogene cellen in preklinische en Alzheimergroepen, wat suggereert dat het afbreken van exciterende synapsen een gemeenschappelijk kenmerk van cognitieve achteruitgang is.
Wat dit betekent voor het beschermen van geheugen
Samengevoegd schetsen de resultaten een gedetailleerd beeld: volwassen mensen blijven nieuwe hippocampale neuronen aanmaken, maar dit proces is uitermate gevoelig voor leeftijd en ziekte. De vroegste en meest robuuste veranderingen vinden plaats op het niveau van chromatine‑toegankelijkheid—de manier waarop DNA is verpakt—lang voordat veel genen zichtbaar hun activiteit veranderen. In veerkrachtige hersenen, zoals die van SuperAgers, houden moleculaire netwerken neurogenese en synaptische communicatie in een "jeugdig" modus ondanks gevorderde leeftijd. In kwetsbare hersenen verschuiven deze netwerken, wat leidt tot vastlopen in de ontwikkeling van nieuwe neuronen en het rafelen van hippocampale circuits. Door deze epigenetische en cellulaire signaturen te onthullen, wijst de studie op strategieën die mogelijk op een dag geheugen kunnen behouden: therapieën die niet alleen plaques verwijderen, maar ook de geheugen‑kwekerij van de hersenen openhouden, de DNA‑poorten goed afstemmen en synapsen veerkrachtig houden.
Bronvermelding: Disouky, A., Sanborn, M.A., Sabitha, K.R. et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 652, 1264–1273 (2026). https://doi.org/10.1038/s41586-026-10169-4
Trefwoorden: hippocampale neurogenese, cognitieve veerkracht, SuperAgers, epigenetica, ziekte van Alzheimer