Clear Sky Science · zh
蛋白质信号阵列中的自发开关揭示近临界合作性
细菌如何做出瞬间决策
细菌虽然微小,但不断在生死攸关的情境中做出决策:朝食物游动、远离毒素或保持直线前进。本研究探究了让肠道细菌大肠埃希菌感知化学物质并转向的分子“天线”的内部机制。作者表明,这些天线运行在有序与无序之间的刀锋上——一种称为临界性的物理状态——使细菌能够对微弱信号作出强烈反应而不致变得迟缓。
细胞表面的分子控制室
大肠埃希菌并非依赖单个孤立的受体,而是将成千上万的感受蛋白集合成细胞表面的一片平面晶体状结构。这些被称为化学感受阵列的补片检测环境分子并控制驱动细菌鞭毛旋转的电机。当趋化物分子与受体结合时,内部酶网络会降低一种通常促进翻滚的激酶活性,从而促使细胞更长时间、更直线地朝更有利的条件移动。一个重大问题是,如此庞大的装配体如何协调其众多部件,以产生精确可靠的信号。
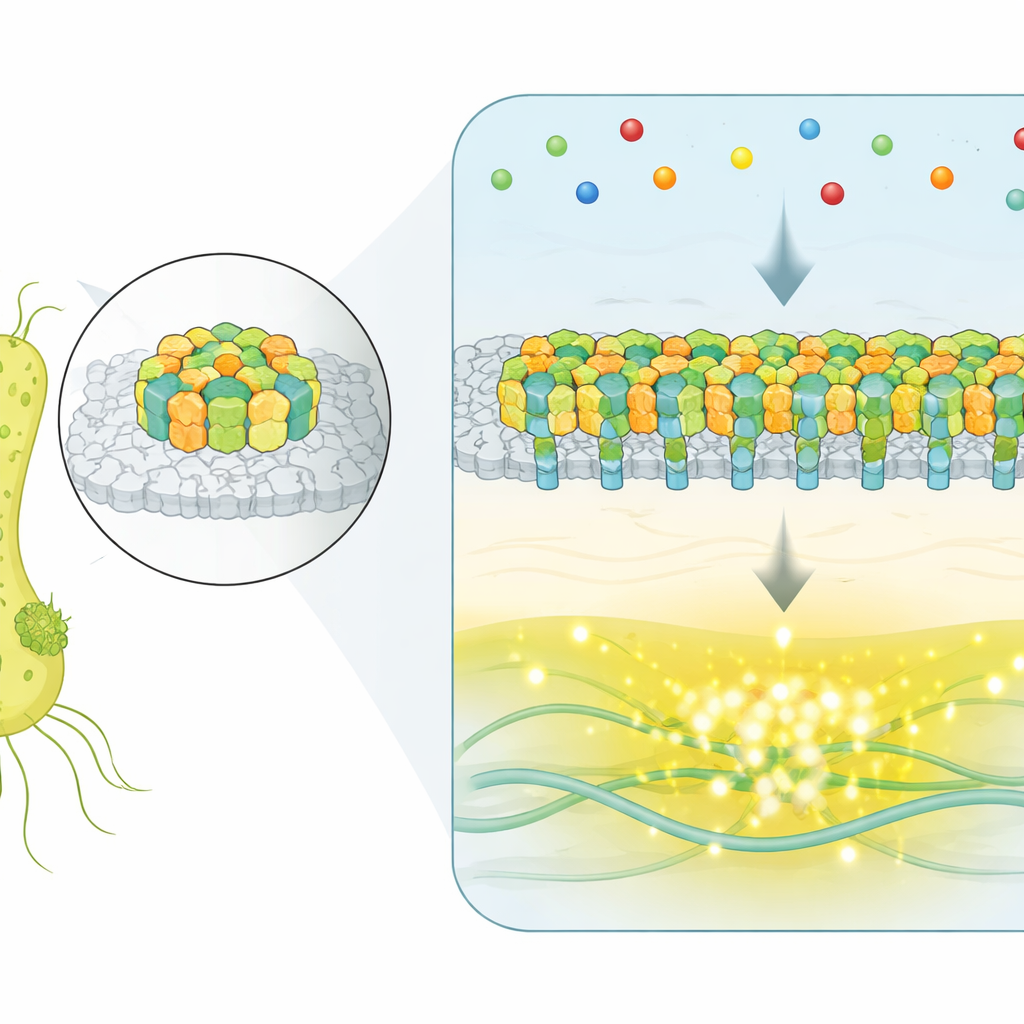
实时捕捉整个阵列的翻转
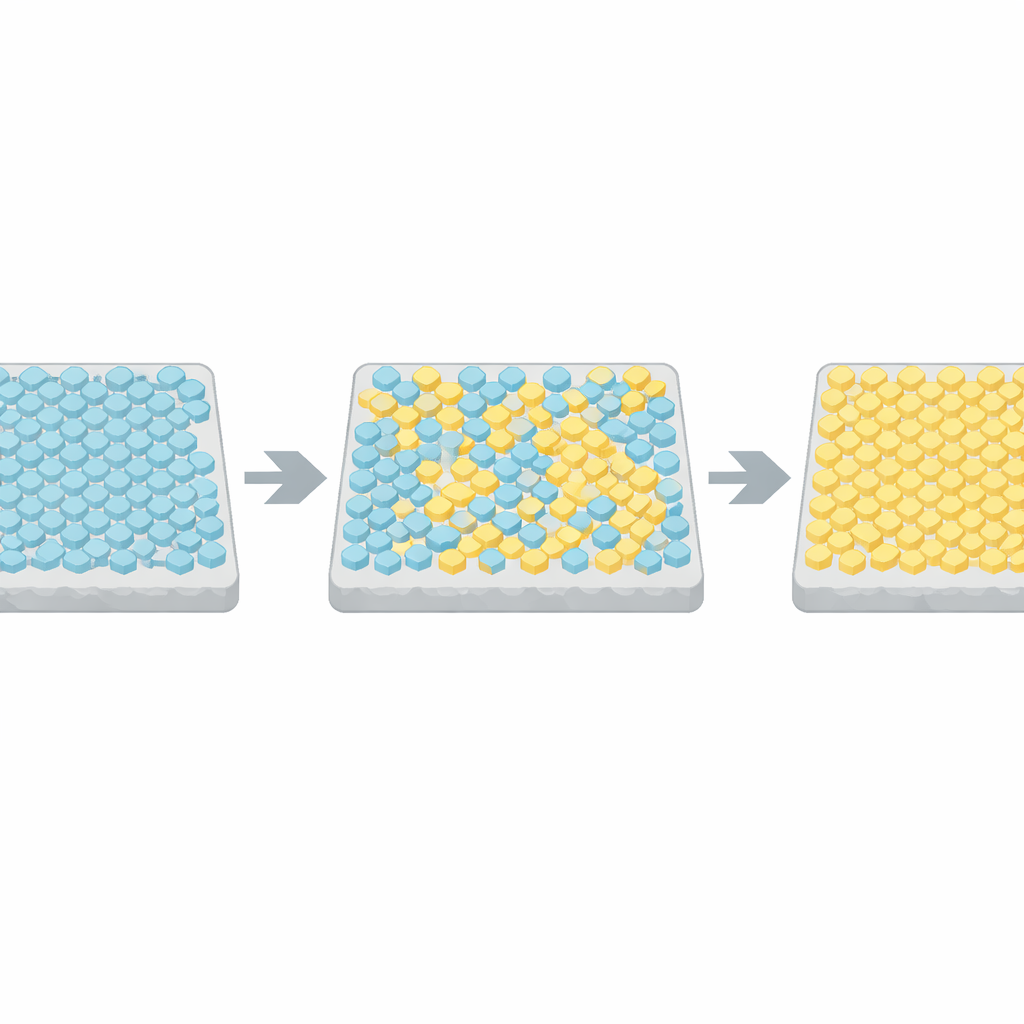
为了在活细胞内观察阵列的工作状态,研究者使用了一种报告关键信号酶活性的荧光技术。他们构建了由单个主导阵列控制整个细胞的菌株,并在外部化学环境保持恒定时监测了数千个个体细菌的随时间变化。在相当一部分细胞中,输出并非仅仅随机波动——而是在两个明确的水平之间来回切换:全开与全关状态。这种自发的两级开关是合作系统的特征,表明许多组件协同作用而非各自为政。
用于蛋白质决策的物理模型
为了解释这些突发翻转,作者求助于物理学的经典模型——伊辛模型,该模型最初用于描述磁体中自旋如何对齐。在他们的改编中,阵列中的每个受体单元可以处于活跃或不活跃状态,邻近单元倾向于匹配对方。计算机模拟表明,当邻居之间的耦合较弱时,活性仅在中间值附近抖动。但当耦合被调节到非常接近临界阈值时,整个晶格偶尔会在几乎全活跃和几乎全不活跃的状态之间跳变,其统计特性与实验数据高度一致。通过将许多细胞的切换时间和持续时间与这些模拟比较,研究小组推断出真实的细菌阵列位于该临界点的几百分点范围内。
在响应速度与强度之间权衡
在临界附近运行有代价。受体之间强耦合会极大地放大小信号,但也会减慢系统改变状态的能力——这一现象称为临界减速。模拟预测,近临界的阵列对新刺激的响应可能需要数十秒,这对大约每秒重新定向一次的细菌来说过于缓慢。作者通过使用微流控装置施加快速的化学阶跃直接检验了这一点。那些被工程化为具有高度均一阵列且缺乏正常适应机制的细胞确实反应很慢,证实了响应幅度与响应速度之间的权衡。
将无序作为一种设计特征
然而,野生型细菌并不被迫承受如此迟缓的行为。它们的阵列通常混合不同的受体物种,并且持续受到通过化学标记调节敏感性的酶的修饰。这两种效应在原本有序的晶格中引入了一种空间和时间上的“无序”。研究的模拟和实验表明,这种无序有效地适度削弱了合作性,足以防止严重的迟滞,同时仍保留强大的放大作用和信号输出中的显著自然波动。这些波动或噪声被认为有助于大肠埃希菌通过改变游动模式更有效地探索环境。
生活在有序与混沌的边缘
作者总结道,近临界合作性是细菌化学感受阵列的核心设计原则。阵列被调节到靠近一个物理临界点,在这里微小的化学线索可以触发大规模协调的反应,但又通过内建的无序加以缓和,从而使决策保持快速且灵活。这项工作将统计物理中的抽象概念与活细胞的可观行为联系起来,提示许多蛋白质装配体——以及未来的合成分子器件——可能被设计为在敏感性与速度之间的这一微妙平衡点上运行。
引用: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
关键词: 细菌趋化性, 蛋白质信号阵列, 生物学中的临界性, 协作受体, 细胞决策