Clear Sky Science · fr
Commutation spontanée dans un réseau de signalisation protéique révèle une coopération proche de la criticité
Comment les bactéries prennent des décisions en une fraction de seconde
Les bactéries sont minuscules, mais elles prennent constamment des décisions vitales : nager vers la nourriture, fuir des toxines ou continuer tout droit. Cette étude examine l’« antenne » moléculaire qui permet à la bactérie intestinale Escherichia coli de détecter des produits chimiques et de s’orienter. Les auteurs montrent que ces antennes fonctionnent exactement sur le fil entre ordre et désordre — un régime physique appelé criticité — permettant aux bactéries de réagir fortement à des signaux faibles sans devenir lentes.
Une salle de contrôle moléculaire à la surface cellulaire
Au lieu d’utiliser des récepteurs isolés, E. coli rassemble des milliers de protéines détectrices en une nappe plane et cristalline à sa surface. Ces agrégats, appelés réseaux chémosensoriels, détectent les molécules de l’environnement et contrôlent les moteurs qui font tourner les flagelles de la bactérie. Lorsque des molécules attractantes se lient aux récepteurs, un réseau enzymatique interne réduit l’activité d’une kinase qui favorise normalement les vrilles, poussant la cellule vers des courses plus longues et plus rectilignes vers de meilleures conditions. La grande question était de savoir comment de telles assemblées massives coordonnent leurs nombreuses parties pour produire des signaux précis et fiables.
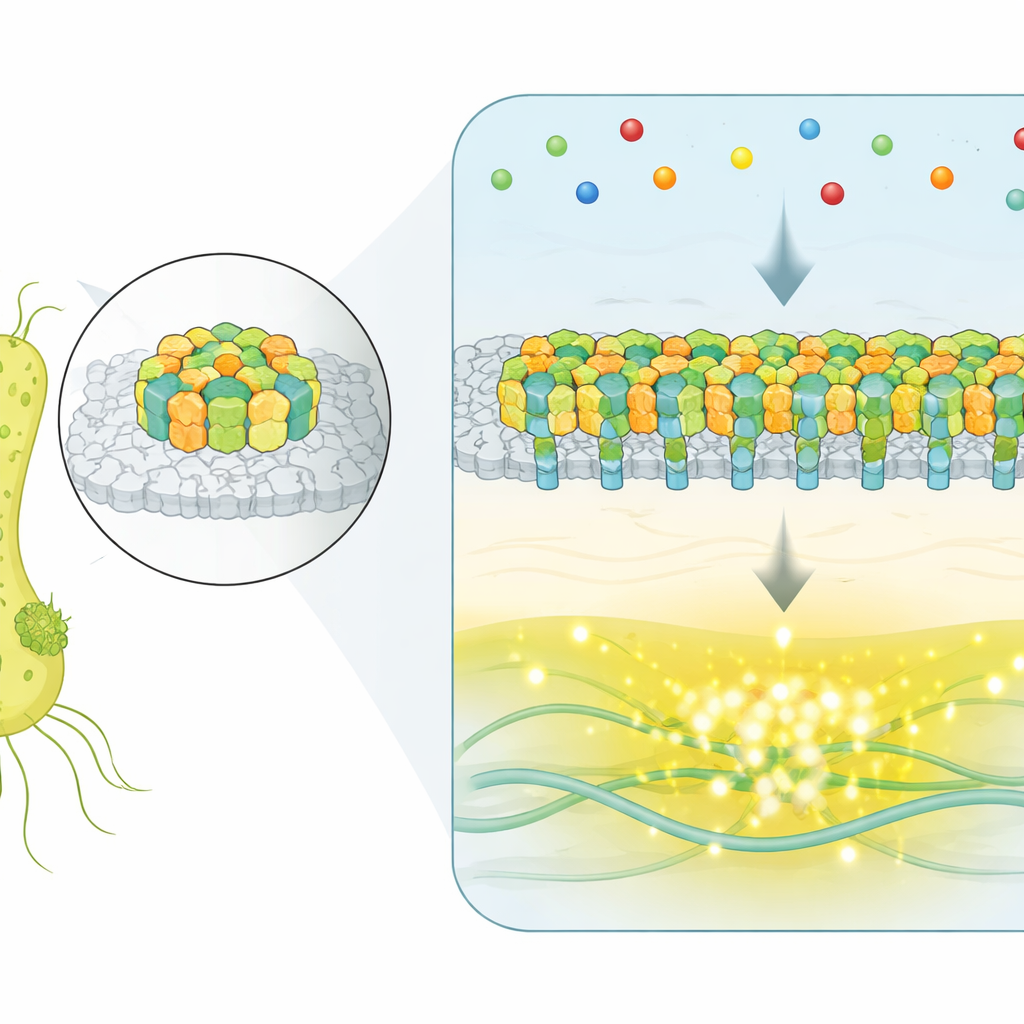
Observer en temps réel les basculements de l’ensemble du réseau
Pour regarder les réseaux en action dans des cellules vivantes, les chercheurs ont utilisé une technique de fluorescence qui renseigne sur l’activité d’une enzyme de signalisation clé. Ils ont conçu des souches où un seul réseau dominant contrôle toute la cellule, puis ont surveillé des milliers de bactéries individuelles au fil du temps, même lorsque l’environnement chimique externe était maintenu constant. Dans une fraction notable des cellules, la sortie ne se contentait pas de trembler au hasard — elle basculait entre deux niveaux bien définis : tout-ON et tout-OFF. Ce basculement spontané à deux niveaux est la marque des systèmes coopératifs, où de nombreux composants agissent ensemble plutôt qu’indépendamment.
Un modèle physique pour les décisions protéiques
Pour comprendre ces basculements abrupts, les auteurs se sont tournés vers un modèle classique de la physique, le modèle d’Ising, développé à l’origine pour décrire l’alignement des spins dans un aimant. Dans leur adaptation, chaque unité réceptrice du réseau peut être active ou inactive, et les unités voisines préfèrent se ressembler. Des simulations informatiques ont montré que lorsque le couplage entre voisins est faible, l’activité ne fait que fluctuer autour d’une valeur moyenne. Mais lorsque le couplage est réglé très près d’un seuil critique, l’ensemble du réseau saute occasionnellement entre des états presque entièrement actifs et presque entièrement inactifs, avec des statistiques qui correspondent étroitement aux données expérimentales. En comparant les temps de basculement et les durées observées dans de nombreuses cellules à ces simulations, l’équipe a déduit que les réseaux bactériens réels se situent à quelques pourcents de ce point critique.
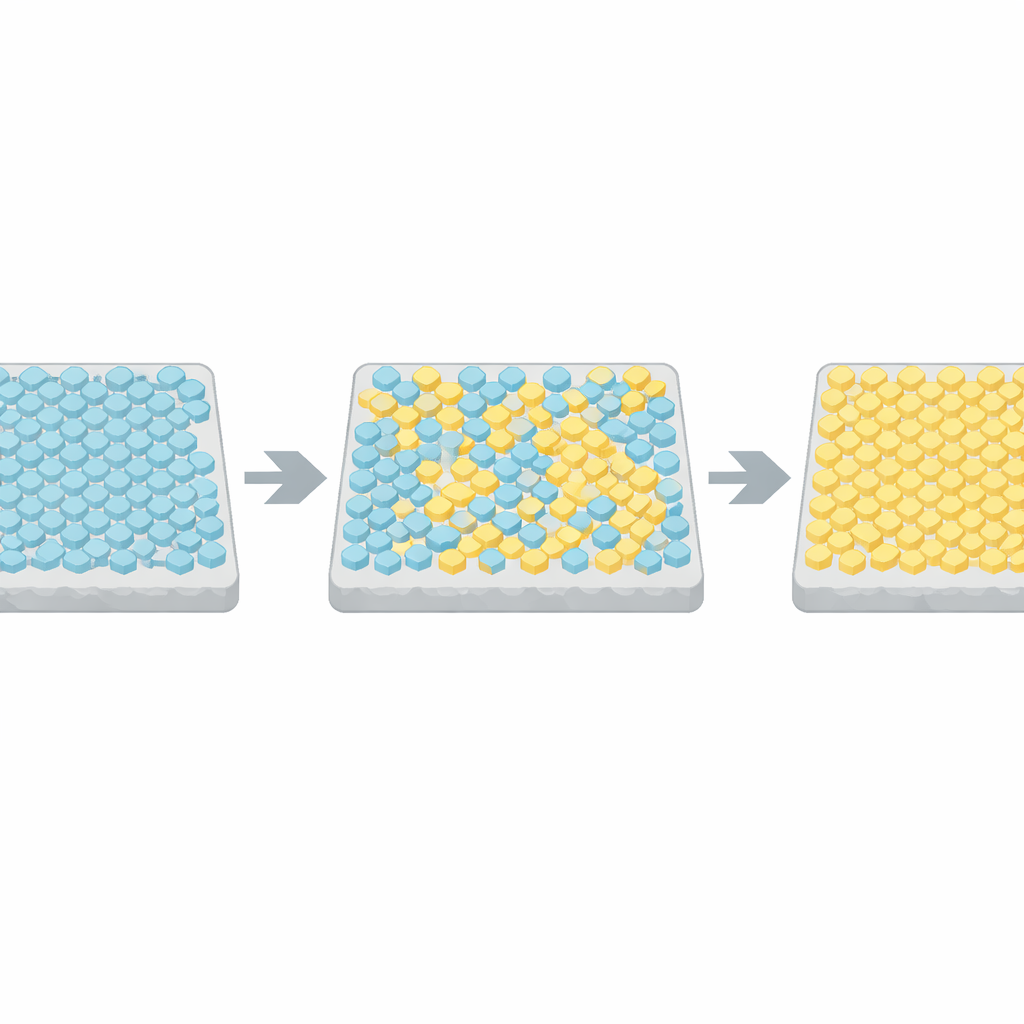
Équilibrer rapidité et amplitude de la réponse
Opérer près de la criticité a un coût. Un fort couplage entre récepteurs amplifie grandement de petites entrées, mais ralentit aussi la capacité du système à changer d’état — un phénomène connu sous le nom de ralentissement critique. Les simulations prédisaient que des réseaux proches de la criticité pourraient mettre des dizaines de secondes à répondre à un nouveau stimulus, trop lent pour des bactéries qui se réorientent en moyenne une fois par seconde. Les auteurs ont testé cela directement en imposant des variations chimiques rapides à l’aide de dispositifs microfluidiques. Les cellules modifiées pour posséder des réseaux très uniformes, dépourvus de leur machinerie d’adaptation habituelle, ont en effet répondu très lentement, confirmant le compromis entre amplitude et vitesse de réponse.
Utiliser le désordre comme caractéristique de conception
Les bactéries sauvages, cependant, ne sont pas condamnées à un comportement aussi lent. Leurs réseaux mélangent généralement différentes espèces de récepteurs, et ils sont constamment modifiés par des enzymes qui ajustent la sensibilité via des marques chimiques. Ces deux effets introduisent une forme de « désordre » spatial et temporel dans la nappe autrement ordonnée. Les simulations et expériences de l’étude ont montré que ce désordre adoucit efficacement la coopération juste ce qu’il faut pour éviter un ralentissement sévère, tout en préservant une forte amplification et des fluctuations naturelles importantes dans la sortie de signalisation. On pense que ces fluctuations, ou bruit, aident E. coli à explorer son environnement plus efficacement en variant ses modes de nage.
Vivre à la frontière entre ordre et chaos
Les auteurs concluent que la coopération proche de la criticité est un principe de conception central du réseau chémosensoriel bactérien. Le réseau est réglé pour se tenir près d’un point de bascule physique où de faibles indices chimiques peuvent déclencher des réponses larges et coordonnées, mais il est tempéré par un désordre intégré afin que les décisions restent rapides et flexibles. Ce travail relie des idées abstraites de la physique statistique à un comportement tangible dans des cellules vivantes, et suggère que de nombreux assemblages protéiques — et peut-être des dispositifs moléculaires synthétiques futurs — pourraient être conçus pour fonctionner à cet équilibre délicat entre sensibilité et vitesse.
Citation: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
Mots-clés: chemotaxie bactérienne, réseaux de signalisation protéique, criticité en biologie, récepteurs coopératifs, prise de décision cellulaire