Clear Sky Science · ar
التبدّل التلقائي في مصفوفة إشارات بروتينية يكشف عن تعاونية قريبة من الحرجة
كيف تتخذ البكتيريا قرارات في جزء من الثانية
قد تكون البكتيريا صغيرة، لكنها تتخذ باستمرار قرارات مصيرية: السباحة نحو الغذاء، الفرار من السموم، أو الاستمرار في السباحة في خط مستقيم. تبحث هذه الدراسة داخل "الهوائي" الجزيئي الذي يتيح لبكتيريا الأمعاء Escherichia coli استشعار المواد الكيميائية وتوجيه حركتها. يبين المؤلفون أن هذه الهوائيات تعمل على حافة بين النظام والاضطراب—نطاق فيزيائي يُعرف بالحرجية—مما يمكّن البكتيريا من الاستجابة بقوة لإشارات ضعيفة دون أن تصبح بطيئة الحركة.
غرفة تحكم جزيئية على سطح الخلية
بدلاً من استخدام مستقبلات مفردة معزولة، تجمع E. coli آلاف بروتينات الاستشعار في رقعة مسطحة بلورية على سطح الخلية. تكشف هذه الرقع، المسماة مصفوفات استشعار الكيميائيات، عن جزيئات في البيئة وتتحكم بالمحركات التي تدير الأسواط البكتيرية. عندما ترتبط جزيئات الجذب بالمستقبلات، يخفض نظام إنزيمي داخلي نشاط كيناز كان يعزز عادة التناوب، مما يدفع الخلية إلى قفلات أطول وأكثر استقامة نحو ظروف أفضل. السؤال الكبير كان كيف تنسق مثل هذه التجمعات الكبيرة أجزائها المتعددة لإنتاج إشارات دقيقة وموثوقة.
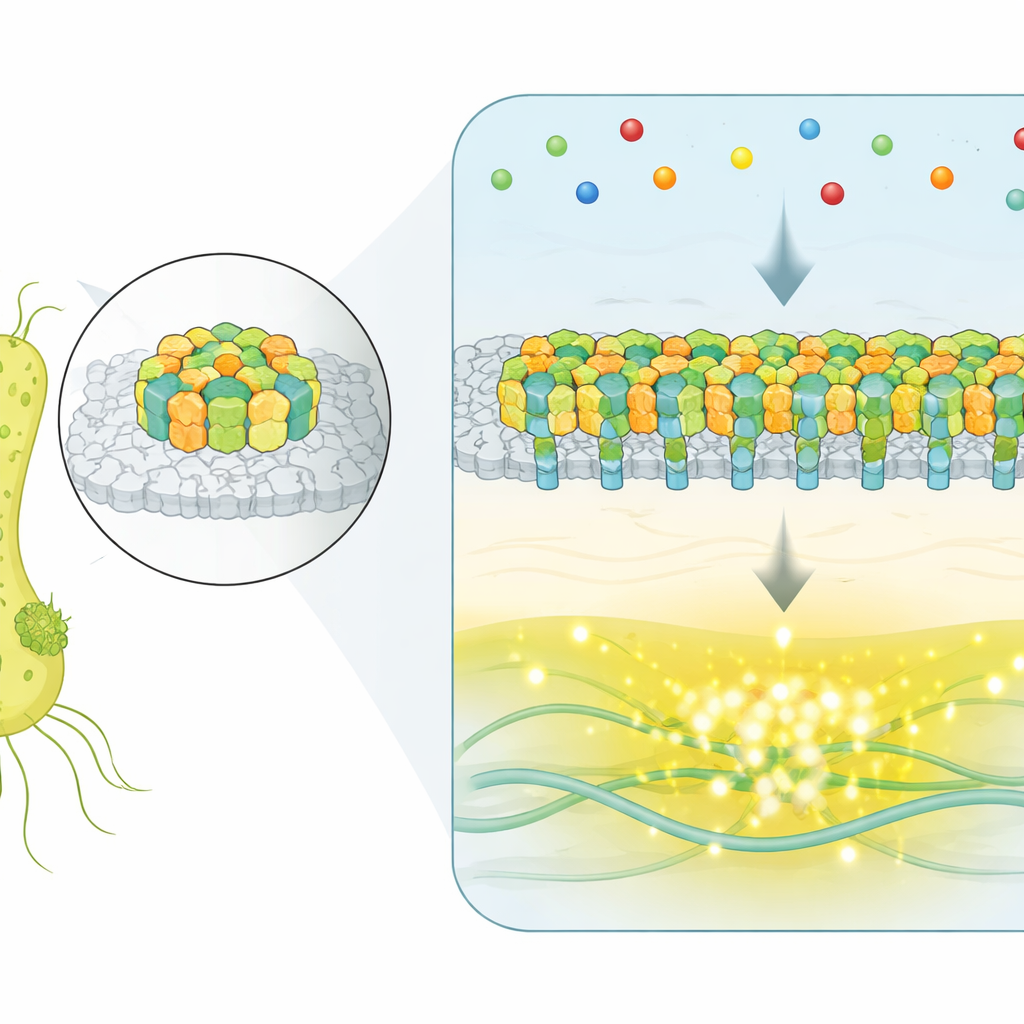
رصد تقلبات المصفوفة الكاملة في الزمن الحقيقي
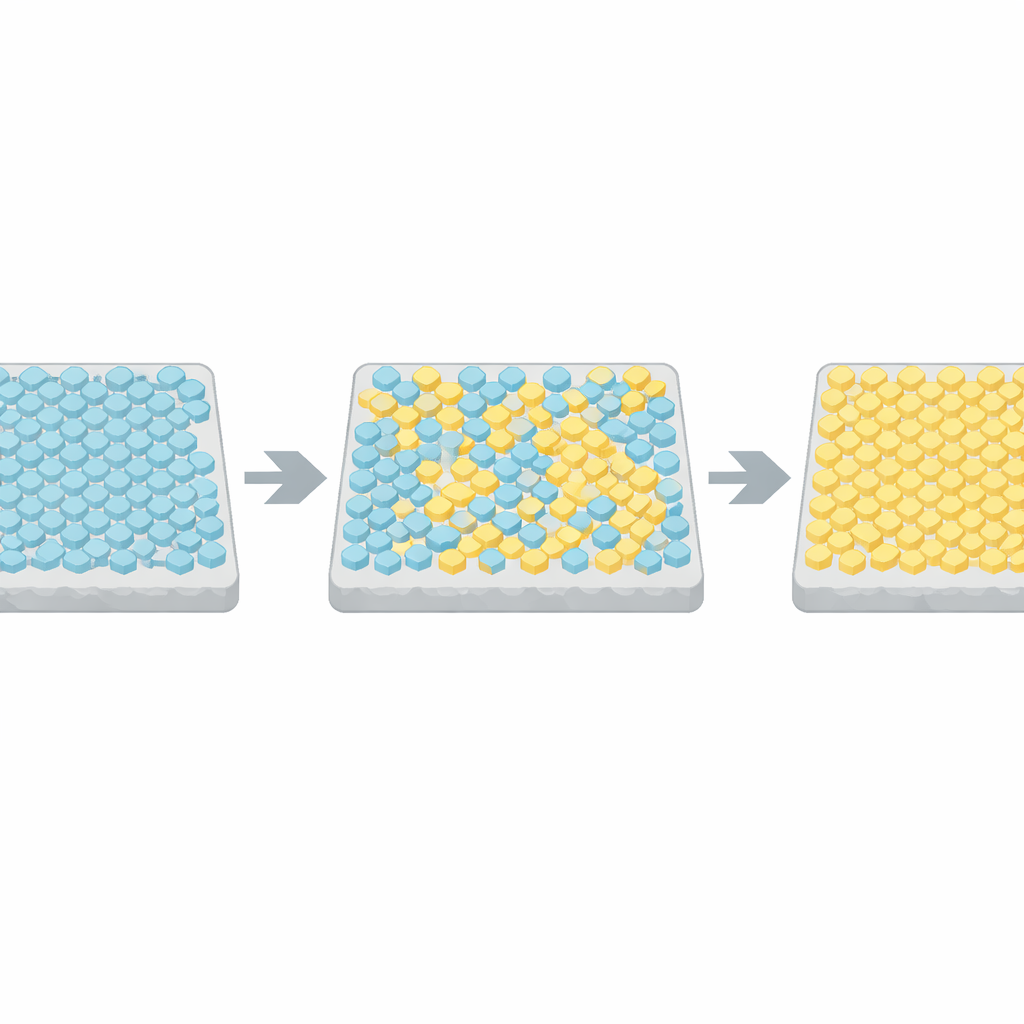
لمراقبة المصفوفات أثناء عملها داخل خلايا حية، استخدم الباحثون تقنية فلورية تُبلغ عن نشاط إنزيم إشاري رئيسي. قاموا بتعديل سلالات بحيث تتحكم مصفوفة واحدة مهيمنة في الخلية بأكملها، ثم رصدوا آلاف البكتيريا الفردية عبر الزمن، حتى عندما كانت البيئة الكيميائية الخارجية ثابتة. في جزء كبير من الخلايا، لم يكن المخرج مجرد ارتعاش عشوائي—بل تقلب فجأة بين مستويين محددين جيداً: حالة تشغيل كاملة وحالة إيقاف كاملة. إن هذا التبدل التلقائي ذو المستويين سمة مميزة للأنظمة التعاونية، حيث تتصرف العديد من المكونات معاً بدلاً من العمل بشكل مستقل.
نموذج فيزيائي لقرارات البروتين
لفهم هذه القفزات الحادة، لجأ المؤلفون إلى نموذج كلاسيكي من الفيزياء، نموذج إيزينغ، الذي طور أصلاً لوصف كيفية محاذاة الدورات في مغناطيس. في تكييفهم، يمكن لكل وحدة مستقبل في المصفوفة أن تكون نشطة أو غير نشطة، وتفضل الوحدات المجاورة أن تتطابق مع بعضها. أظهرت المحاكاة الحاسوبية أنه عندما يكون الترابط بين الجيران ضعيفاً، تتذبذب الفعالية حول قيمة وسطية. ولكن عندما يتم ضبط الترابط ليكون قريباً جداً من عتبة حرجة، تقفز الشبكة بأكملها أحياناً بين حالات شبه جميعها نشطة وحالات شبه جميعها غير نشطة، مع إحصاءات تطابقت عن كثب مع البيانات التجريبية. بمقارنة أوقات وتوابع التبديل عبر العديد من الخلايا مع هذه المحاكاة، استنتج الفريق أن المصفوفات البكتيرية الحقيقية تقع ضمن بضعة بالمئة من هذه النقطة الحرجة.
موازنة سرعة وقوة الاستجابة
العمل قرب الحرجة له ثمن. الترابط القوي بين المستقبلات يضخم المدخلات الصغيرة بشكل كبير، لكنه يبطئ أيضاً قدرة النظام على تغيير الحالة—وهي ظاهرة معروفة باسم التباطؤ الحرج. توقعت المحاكاة أن المصفوفات القريبة من الحرجة قد تستغرق عشرات الثواني للاستجابة لمحفز جديد، وهذا بطيء للغاية للبكتيريا التي تعيد توجيه نفسها تقريباً مرة كل ثانية. اختبر المؤلفون هذا مباشرة بفرض خطوات كيميائية سريعة باستخدام أجهزة ميكروفلويديك. استجابت الخلايا المعدلة لتحتوي على مصفوفات شديدة الاتساق، وبدون آليتها الطبيعية للتكيف، فعلاً ببطء شديد، مؤكدة المقايضة بين حجم الاستجابة وسرعتها.
استخدام الاضطراب كميزة تصميم
ومع ذلك، لا تكون البكتيريا البرية محكومة بهذه السلوكيات البطيئة. عادةً ما تخلط مصفوفاتها بين أنواع مستقبلات مختلفة، كما تُعدَّل باستمرار بواسطة إنزيمات تضبط الحساسية عبر علامات كيميائية. كلا التأثيرين يُدخِلان نوعاً من "الاضطراب" المكاني والزمني في الشبكة المنظمة. أظهرت محاكيات الدراسة وتجاربها أن هذا الاضطراب يلين التعاونية بما يكفي لمنع تباطؤ شديد، مع المحافظة على تضخيم قوي وتقلبات طبيعية كبيرة في خرج الإشارة. وتعتقد أن هذه التقلبات، أو الضوضاء، تساعد E. coli في استكشاف محيطها بفاعلية أكبر عن طريق تغيير أنماط السباحة.
الحياة على حافة النظام والفوضى
يخلص المؤلفون إلى أن التعاون القريب من الحرجة هو مبدأ تصميم أساسي في مصفوفة الاستشعار الكيميائي البكتيرية. تُضبط المصفوفة لتقع قريبة من نقطة انقلاب فيزيائية حيث يمكن لإشارات كيميائية صغيرة أن تثير استجابات كبيرة ومنسقة، لكنها تُهدأ بواسطة اضطراب مدمج بحيث تبقى القرارات سريعة ومرنة. يربط هذا العمل أفكاراً مجردة من الفيزياء الإحصائية بسلوك ملموس في خلايا حية، ويقترح أن العديد من تجمعات البروتين—وربما الأجهزة الجزيئية الاصطناعية في المستقبل—قد تُصمم لتعمل عند هذا التوازن الدقيق بين الحساسية والسرعة.
الاستشهاد: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
الكلمات المفتاحية: الكيمياء الحركية البكتيرية, مصفوفات إشارة البروتين, الحرجية في الأحياء, المستقبلات التعاونية, اتخاذ القرار الخلوي