Clear Sky Science · pl
Spontaniczne przełączanie w białkowej macierzy sygnalizacyjnej ujawnia bliską-krytyczną kooperatywność
Jak bakterie podejmują decyzje w ułamkach sekundy
Bakterie są małe, ale nieustannie podejmują decyzje o życiu i śmierci: płynąć ku pożywieniu, uciekać przed toksynami albo płynąć prosto. To badanie zagląda do molekularnej „anteny”, która pozwala jelitowej bakterii Escherichia coli wyczuwać chemikalia i sterować ruchem. Autorzy pokazują, że te anteny działają dokładnie na krawędzi porządku i nieładu — w fizycznym reżimie znanym jako krytyczność — co pozwala bakteriom silnie reagować na słabe sygnały, nie stając się przy tym ospałymi.
Molekularna centrala na powierzchni komórki
Zamiast używać pojedynczych, izolowanych receptorów, E. coli gromadzi tysiące białek sensorycznych w płaskiej, krystalicznej płytce na powierzchni komórki. Te struktury, zwane tablicami chemosensorycznymi, wykrywają cząsteczki w otoczeniu i kontrolują silniki obracające wici bakterii. Gdy cząsteczki przyciągające wiążą się z receptorami, wewnętrzna sieć enzymatyczna obniża aktywność kinazy, która zwykle sprzyja obracaniu się (tumblingowi), skłaniając komórkę do dłuższych, prostszych biegów ku lepszym warunkom. Kluczowe pytanie brzmiało, jak tak duże zespoły koordynują swoje części, by generować precyzyjne i wiarygodne sygnały.
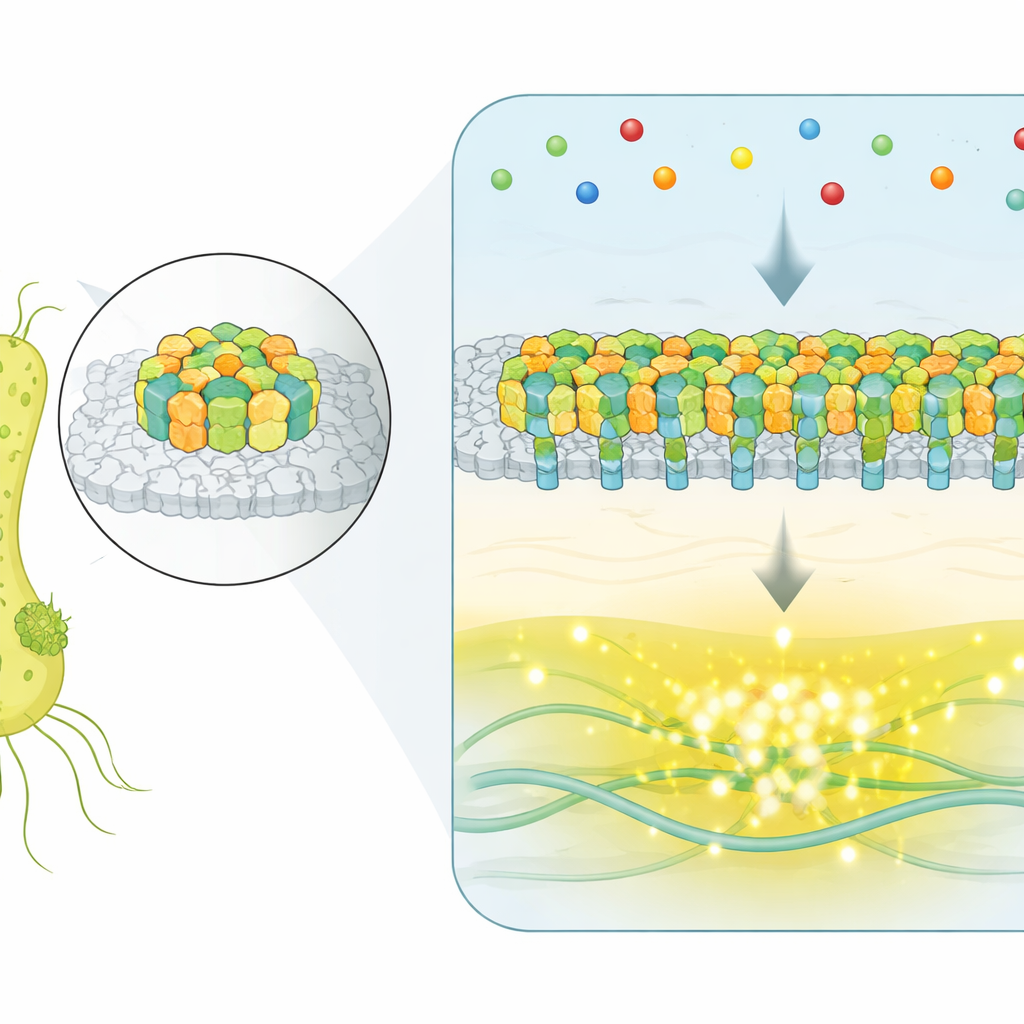
Obserwowanie przełączeń całej tablicy w czasie rzeczywistym
Aby zobaczyć tablice w działaniu wewnątrz żywych komórek, badacze użyli techniki fluorescencyjnej raportującej aktywność kluczowego enzymu sygnalizacyjnego. Opracowali szczepy, w których pojedyncza dominująca tablica kontroluje całą komórkę, a następnie monitorowali tysiące pojedynczych bakterii w czasie, nawet gdy zewnętrzne środowisko chemiczne pozostawało niezmienne. U znacznej części komórek sygnał nie tylko drgał losowo — przełączał się wyraźnie między dwoma dobrze zdefiniowanymi poziomami: stanem całkowicie WŁĄCZONYM i całkowicie WYŁĄCZONYM. To spontaniczne, dwupoziomowe przełączanie jest znakiem rozpoznawczym systemów kooperatywnych, w których wiele składników działa razem, a nie niezależnie.
Fizyczny model decyzji białkowych
Aby zrozumieć te nagłe skoki, autorzy sięgnęli po klasyczny model fizyczny — model Isinga — pierwotnie opracowany do opisu wyrównywania spinów w magnesie. W ich adaptacji każda jednostka receptorowa w tablicy może być aktywna lub nieaktywna, a sąsiadujące jednostki wolą być zgodne. Symulacje komputerowe wykazały, że gdy sprzężenie między sąsiadami jest słabe, aktywność jedynie drga wokół wartości środkowej. Jednak gdy sprzężenie jest ustawione bardzo blisko krytycznego progu, cała kratownica od czasu do czasu przeskakuje między niemal całkowicie aktywnym a niemal całkowicie nieaktywnym stanem, z statystykami ściśle odpowiadającymi danym eksperymentalnym. Porównując czasy przełączeń i ich trwania w wielu komórkach z wynikami symulacji, zespół wywnioskował, że prawdziwe bakteryjne tablice znajdują się w odległości kilku procent od tego punktu krytycznego.
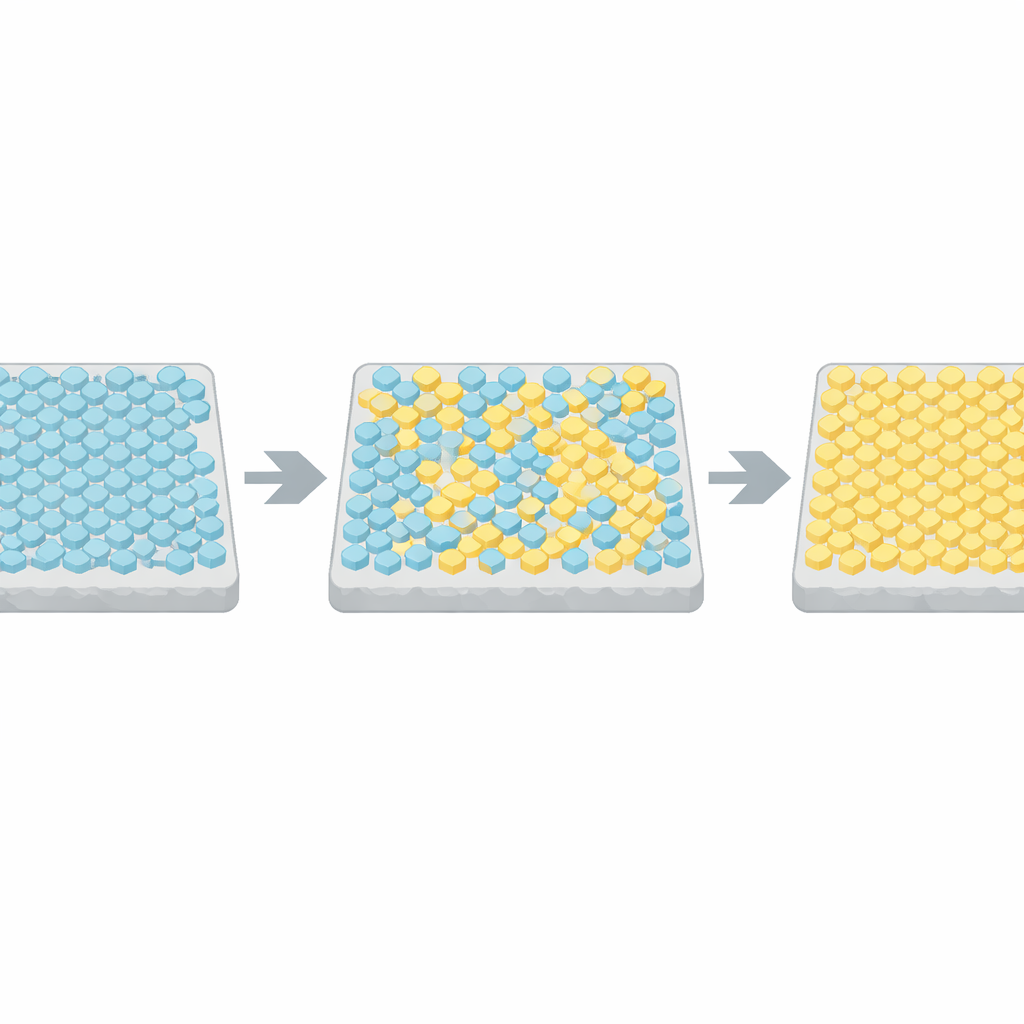
Równoważenie szybkości i siły odpowiedzi
Praca blisko krytyczności ma swoją cenę. Silne sprzężenie między receptorami znacznie wzmacnia drobne sygnały, ale jednocześnie spowalnia zdolność systemu do zmiany stanu — zjawisko znane jako krytyczne spowolnienie. Symulacje przewidziały, że tablice bliskie krytyczności mogą potrzebować dziesiątek sekund na reakcję na nowy bodziec, zbyt wolno dla bakterii, które zmieniają orientację około raz na sekundę. Autorzy sprawdzili to bezpośrednio, narzucając szybkie skoki chemiczne za pomocą urządzeń mikroprzepływowych. Komórki zaprojektowane tak, by miały bardzo jednorodne tablice, pozbawione normalnego mechanizmu adaptacji, rzeczywiście reagowały bardzo wolno, potwierdzając kompromis między wielkością odpowiedzi a jej szybkością.
Wykorzystywanie nieporządku jako cechy projektowej
Dziko żyjące bakterie jednak nie są skazane na takie ospałe zachowanie. Ich tablice zwykle mieszą różne gatunki receptorów i są stale modyfikowane przez enzymy, które regulują czułość przez chemiczne znaczniki. Oba te efekty wprowadzają rodzaj przestrzennego i czasowego „nieporządku” do w przeciwnym razie uporządkowanej kratownicy. Symulacje i eksperymenty z badania wykazały, że ten nieporządek skutecznie zmiękcza kooperatywność na tyle, by zapobiec poważnemu spowolnieniu, zachowując jednocześnie silne wzmocnienie i istotne naturalne fluktuacje sygnału. Te fluktuacje, czyli szum, uważa się za pomocne dla E. coli w efektywniejszym eksplorowaniu otoczenia poprzez zróżnicowanie wzorców pływania.
Życie na krawędzi porządku i chaosu
Autorzy wnioskują, że bliska-krytyczna kooperatywność jest podstawową zasadą projektową bakteryjnej tablicy chemosensorycznej. Tablica jest dostrojona do położenia blisko fizycznego punktu przechyłu, w którym drobne sygnały chemiczne mogą wywołać duże, skoordynowane odpowiedzi, lecz jest złagodzona wbudowanym nieporządkiem, dzięki czemu decyzje pozostają szybkie i elastyczne. Praca ta łączy abstrakcyjne idee z fizyki statystycznej z namacalnym zachowaniem żywych komórek, sugerując, że wiele zespołów białkowych — a być może także syntetycznych urządzeń molekularnych przyszłości — może być zaprojektowanych do działania w tej delikatnej równowadze między czułością a szybkością.
Cytowanie: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
Słowa kluczowe: chemotaksja bakteryjna, białkowe tablice sygnalizacyjne, krytyczność w biologii, receptory kooperatywne, decyzje komórkowe