Clear Sky Science · ja
タンパク質シグナル配列における自発的スイッチングが示す臨界近傍の協同性
細菌はどうやって一瞬のうちに決断するか
細菌は小さいが、生死を左右する決断を常に行っている:餌に向かって泳ぐ、毒から逃げる、あるいは直進を続ける。この研究は、腸内細菌Escherichia coliが化学物質を感知して進路を制御する分子「アンテナ」の内部を調べる。著者らは、これらのアンテナが秩序と無秩序の境界、すなわち臨界性として知られる物理的領域のまさに縁にあり、ごく弱い信号に対して鋭く応答しつつも鈍くなりすぎないようになっていることを示す。
細胞表面にある分子制御室
個々の孤立した受容体を用いる代わりに、E. coliは数千の感知タンパク質を細胞表面の平坦で結晶様のパッチに集める。これらは化学感受アレイと呼ばれ、環境中の分子を検出して鞭毛を回すモーターを制御する。誘引分子が受容体に結合すると、内部の酵素ネットワークが通常は「くねり(タンブル)」を促進するキナーゼの活性を下げ、細胞をより長くまっすぐ進む方向に傾ける。多くの構成要素を持つこうした大規模集合体が、どうやって精密で信頼できる信号を生み出すために協調するのかが大きな疑問だった。
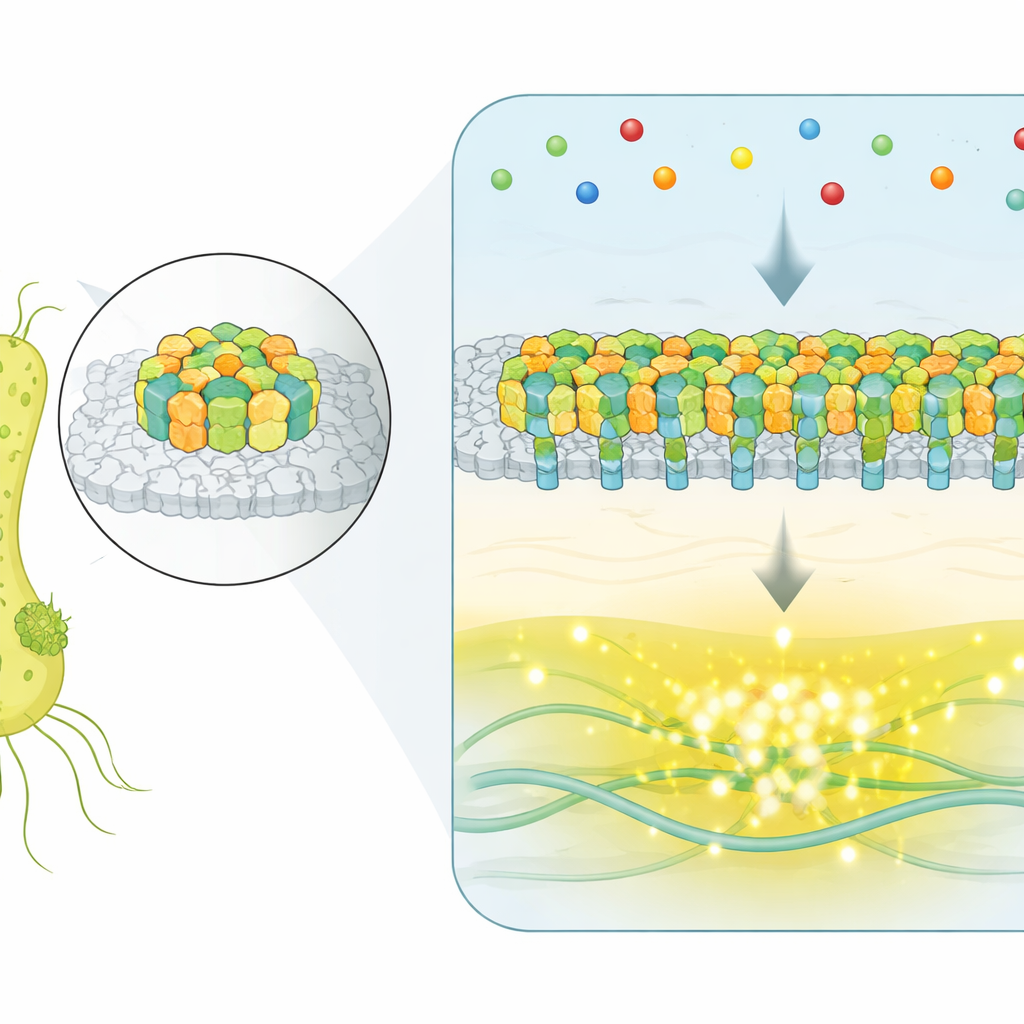
全アレイの反転をリアルタイムで捉える
生きた細胞内でアレイの動作を観察するために、研究者らは主要なシグナル酵素の活性を報告する蛍光手法を用いた。単一の優勢なアレイが細胞全体を支配するように改変した株を作成し、外部化学環境を一定に保ったまま何千もの個々の細菌を時間経過で追跡した。かなりの割合の細胞で、出力は単にランダムに揺らぐだけではなく、二つの明瞭なレベルの間をパチッと往復した:全ONと全OFFの状態。この自発的な二レベルのスイッチングは、多くの構成要素が独立してではなく協同して動く系の特徴である。
タンパク質の決定を説明する物理モデル
これらの急激な反転を理解するために、著者らは磁性体中でスピンが整列する様子を記述するために古くから使われるイジングモデルという物理モデルに立ち返った。彼らの適用では、アレイの各受容体単位は活性か非活性のいずれかであり、隣接する単位同士は一致することを好む。コンピュータシミュレーションは、隣接間の結合が弱いときは活動が中央付近でただ揺らぐだけであることを示した。しかし結合が臨界閾値に非常に近く調整されると、格子全体が時折ほぼ全活性とほぼ全非活性の状態の間をジャンプし、その統計は実験データと密接に一致した。多数の細胞にわたるスイッチング時間と持続時間をこれらのシミュレーションと比較することで、実際の細菌アレイはこの臨界点から数パーセント以内の範囲に位置していると推定された。
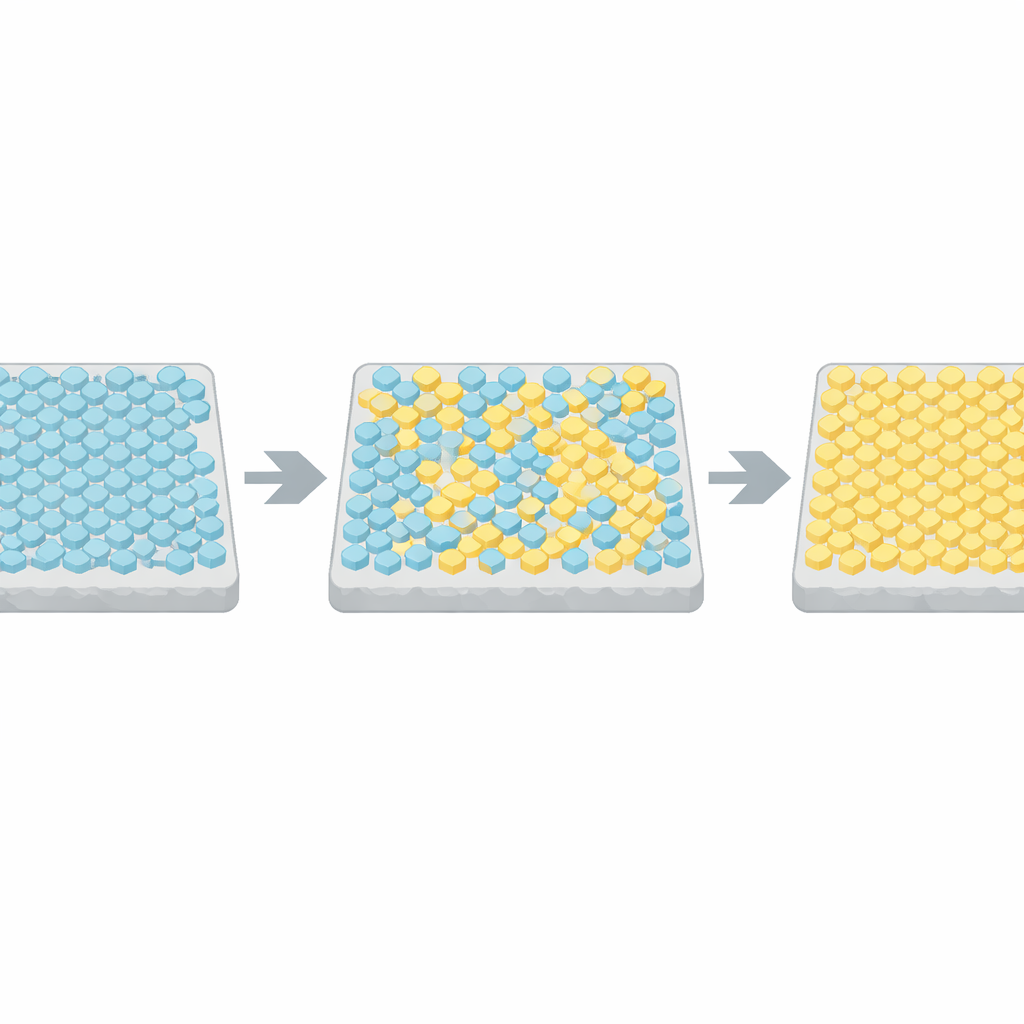
応答の速さと強さのバランス
臨界近傍で動作することには代償がある。受容体間の強い結合は小さな入力を大きく増幅するが、系が状態を変える能力も遅くしてしまう—これは臨界減速として知られる現象である。シミュレーションは、臨界近傍のアレイが新しい刺激に応答するのに数十秒かかる可能性があり、1秒程度で再配向する細菌には遅すぎると予測した。著者らはマイクロフルイディクス装置を使って急速な化学的ステップを与えることでこれを直接検証した。通常の適応機構を持たない非常に均一なアレイを持つように設計した細胞は、確かに非常に遅く応答し、応答の大きさと速度のトレードオフを裏付けた。
不規則性を設計上の特徴として利用する
しかし野生型の細菌はそのような鈍い振る舞いに囚われてはいない。彼らのアレイは通常、異なる受容体種を混ぜ合わせ、感度を化学的修飾で調整する酵素群によって常に変更されている。これらの効果はいずれも、秩序だった格子に対して空間的かつ時間的な「不規則性」を導入する。本研究のシミュレーションと実験は、この不規則性が協同性を適度に和らげ、深刻な減速を防ぎつつも強い増幅とかなりの自然揺らぎをシグナル出力に保持することを示した。これらの揺らぎ(ノイズ)は、泳ぎ方を変えることでE. coliが周囲をより効果的に探索するのを助けると考えられている。
秩序と混沌の境界で生きる
著者らは、臨界近傍の協同性が細菌化学感受アレイの中核的設計原理であると結論づける。アレイは小さな化学的手がかりが大きく協調した応答を引き起こす物理的な転換点に近づくように調整されており、同時に組み込まれた不規則性によって決断が速く柔軟に保たれている。この研究は統計物理学の抽象的な概念を生きた細胞の具体的行動に結びつけ、多くのタンパク質集合体や将来の合成分子デバイスが感度と速度の微妙なバランスで動作するよう設計され得ることを示唆している。
引用: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
キーワード: 細菌走化性, タンパク質シグナル配列, 生物学における臨界性, 協同受容体, 細胞の意思決定