Clear Sky Science · it
Commutazione spontanea in un array proteico di segnalazione rivela cooperatività quasi critica
Come i batteri prendono decisioni in un istante
I batteri possono essere minuscoli, ma prendono costantemente decisioni di vita o di morte: nuotare verso il cibo, fuggire dalle tossine o continuare dritti. Questo studio indaga l’interno dell’“antenna” molecolare che permette al batterio intestinale Escherichia coli di percepire sostanze chimiche e orientarsi. Gli autori mostrano che queste antenne operano proprio sul filo del rasoio tra ordine e disordine—un regime fisico noto come criticità—consentendo ai batteri di rispondere con forza a segnali deboli senza diventare lenti.
Una sala di controllo molecolare sulla superficie cellulare
Invece di usare recettori singoli e isolati, E. coli raggruppa migliaia di proteine sensoriali in una patch piatta e cristallina sulla superficie cellulare. Queste patch, chiamate array chemosensoriali, rilevano molecole nell’ambiente e controllano i motori che fanno girare i flagelli del batterio. Quando le molecole attrattive si legano ai recettori, una rete enzimatica interna riduce l’attività di una chinasi che normalmente favorisce il movimento a caso (tumbling), inducendo la cellula a percorsi più lunghi e più diretti verso condizioni migliori. La grande domanda è stata come tali grandi assemblaggi coordinino le loro molte parti per produrre segnali precisi e affidabili.
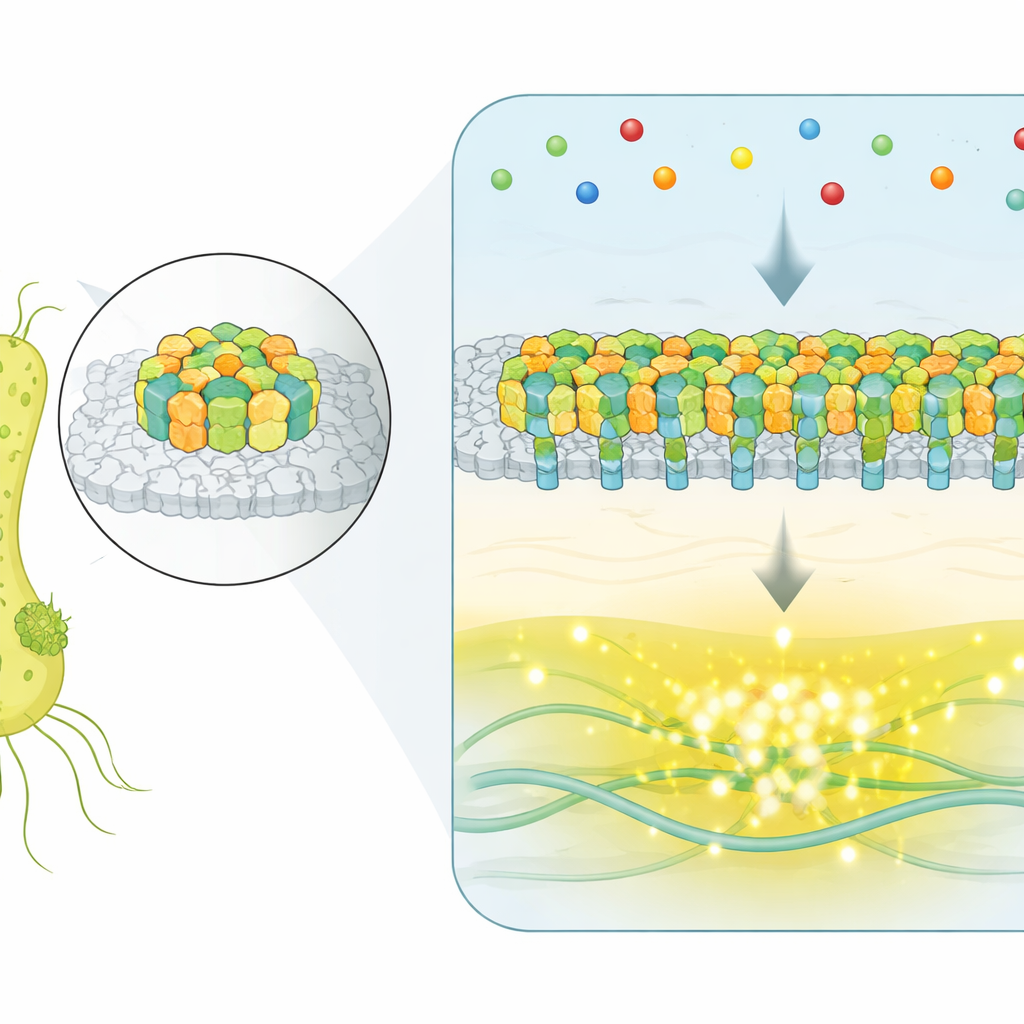
Catturare i ribaltamenti dell’intero array in tempo reale
Per osservare gli array in azione all’interno di cellule vive, i ricercatori hanno usato una tecnica fluorescente che segnala l’attività di un enzima chiave nella segnalazione. Hanno ingegnerizzato ceppi in cui un singolo array dominante controlla l’intera cellula, quindi hanno monitorato migliaia di batteri individuali nel tempo, anche quando l’ambiente chimico esterno rimaneva costante. In una frazione significativa delle cellule, l’uscita non si limitava a sfarfallare casualmente—passava bruscamente tra due livelli ben distinti: uno stato tutto-ON e uno tutto-OFF. Questo switching spontaneo a due livelli è una firma dei sistemi cooperativi, in cui molti componenti agiscono insieme piuttosto che indipendentemente.
Un modello fisico per le decisioni proteiche
Per comprendere questi ribaltamenti improvvisi, gli autori si sono rivolti a un modello classico della fisica, il modello di Ising, sviluppato originariamente per descrivere come si allineano gli spin in un magnete. Nella loro adattazione, ogni unità recettoriale dell’array può essere attiva o inattiva, e le unità vicine preferiscono essere uguali. Le simulazioni al computer hanno mostrato che quando l’accoppiamento tra vicini è debole, l’attività oscilla attorno a un valore medio. Ma quando l’accoppiamento è sintonizzato molto vicino a una soglia critica, l’intero reticolo salta occasionalmente tra stati quasi tutti-attivi e quasi tutti-inattivi, con statistiche che corrispondevano strettamente ai dati sperimentali. Confrontando i tempi di switching e le durate in molte cellule con queste simulazioni, il gruppo ha dedotto che i veri array batterici si trovano a pochi percentuali da questo punto critico.
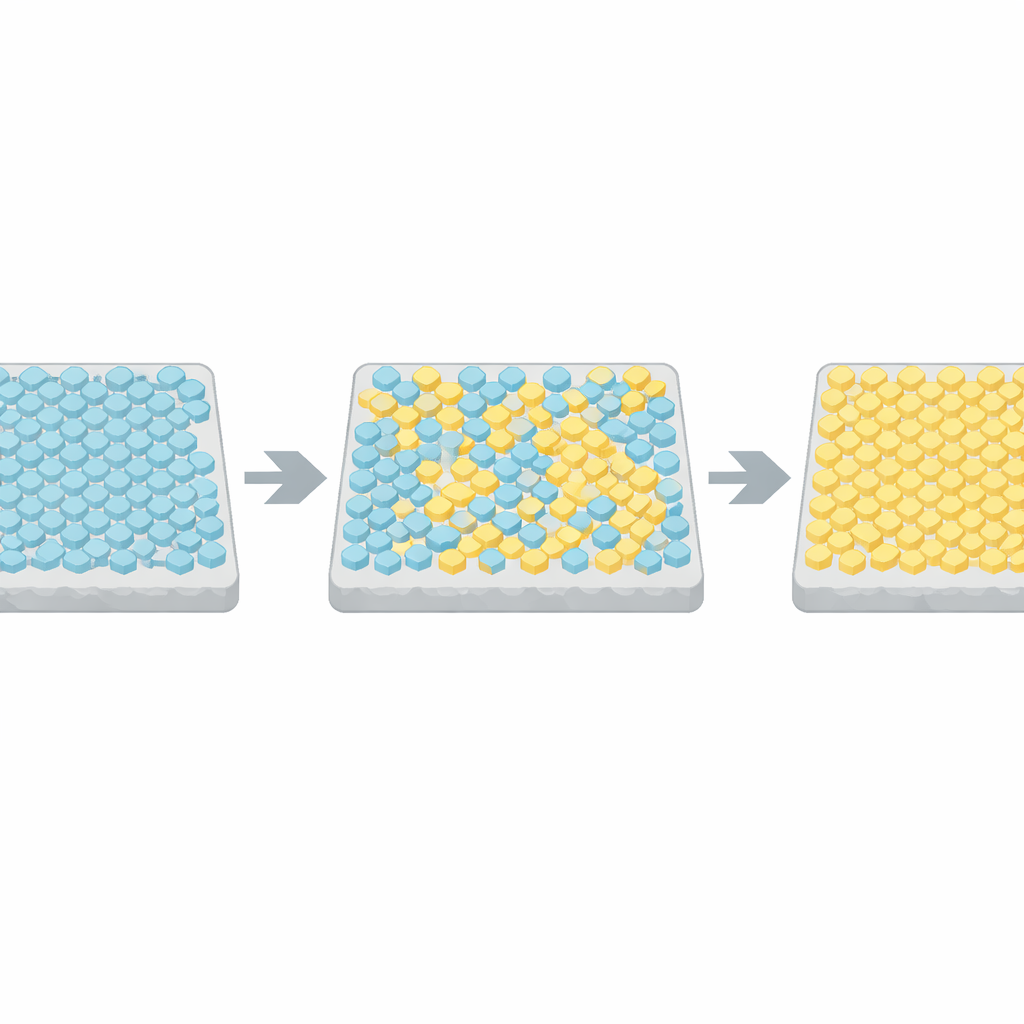
Bilanciare velocità e intensità della risposta
Operare vicino alla criticità comporta un prezzo. Un forte accoppiamento tra recettori amplifica molto gli input piccoli, ma rallenta anche la capacità del sistema di cambiare stato—un fenomeno noto come rallentamento critico. Le simulazioni prevedevano che gli array quasi critici potessero impiegare decine di secondi per rispondere a un nuovo stimolo, troppo lenti per batteri che si riorientano grosso modo una volta al secondo. Gli autori hanno testato questo direttamente imponendo passi chimici rapidi mediante dispositivi microfluidici. Le cellule ingegnerizzate per avere array molto uniformi, privi della loro normale macchina di adattamento, hanno infatti risposto molto lentamente, confermando il compromesso tra ampiezza e velocità della risposta.
Usare il disordine come caratteristica progettuale
I batteri selvatici, tuttavia, non sono condannati a un comportamento così pigro. I loro array di solito mescolano diverse specie di recettori e sono costantemente modificati da enzimi che regolano la sensibilità tramite marcatori chimici. Entrambi gli effetti introducono una sorta di “disordine” spaziale e temporale nel reticolo altrimenti ordinato. Le simulazioni e gli esperimenti dello studio hanno mostrato che questo disordine ammorbidisce efficacemente la cooperatività quel tanto che basta per prevenire un rallentamento severo, pur preservando una forte amplificazione e fluttuazioni naturali sostanziali nell’output di segnalazione. Si pensa che queste fluttuazioni, o rumore, aiutino E. coli a esplorare l’ambiente in modo più efficace variando i suoi schemi di nuoto.
Vita al confine tra ordine e caos
Gli autori concludono che la cooperatività quasi critica è un principio progettuale fondamentale dell’array chemosensoriale batterico. L’array è sintonizzato per stare vicino a un punto di svolta fisico dove piccoli segnali chimici possono scatenare risposte ampie e coordinate, ma è temperato da un disordine incorporato in modo che le decisioni restino rapide e flessibili. Questo lavoro collega idee astratte della fisica statistica a comportamenti concreti nelle cellule viventi, suggerendo che molti assemblaggi proteici—e forse dispositivi molecolari sintetici del futuro—potrebbero essere progettati per operare in questo delicato equilibrio tra sensibilità e velocità.
Citazione: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
Parole chiave: chemotassi batterica, array di segnalazione proteica, criticità in biologia, recettori cooperativi, processi decisionali cellulari