Clear Sky Science · pt
Troca espontânea em um arranjo de sinalização proteica revela cooperatividade quase-crítica
Como bactérias tomam decisões em frações de segundo
Bactérias podem ser minúsculas, mas tomam constantemente decisões de vida ou morte: nadar em direção ao alimento, fugir de toxinas ou seguir em frente. Este estudo examina o interior da “antena” molecular que permite à bactéria intestinal Escherichia coli detectar químicos e se orientar. Os autores mostram que essas antenas operam exatamente na fronteira entre ordem e desordem — um regime físico conhecido como criticidade — permitindo que as bactérias respondam fortemente a sinais fracos sem se tornarem lentas.
Uma sala de controle molecular na superfície celular
Em vez de usar receptores isolados, E. coli reúne milhares de proteínas sensoriais em um mosaico plano e cristalino na superfície celular. Esses aglomerados, chamados de arranjos quimiossensoriais, detectam moléculas no ambiente e controlam os motores que giram os flagelos da bactéria. Quando moléculas atrativas se ligam aos receptores, uma rede enzimática interna reduz a atividade de uma quinase que normalmente promove o “tumbling” (rodopios), inclinando a célula para corridas mais longas e retilíneas em direção a condições melhores. A grande questão tem sido como montagens tão grandes coordenam suas muitas partes para produzir sinais precisos e confiáveis.
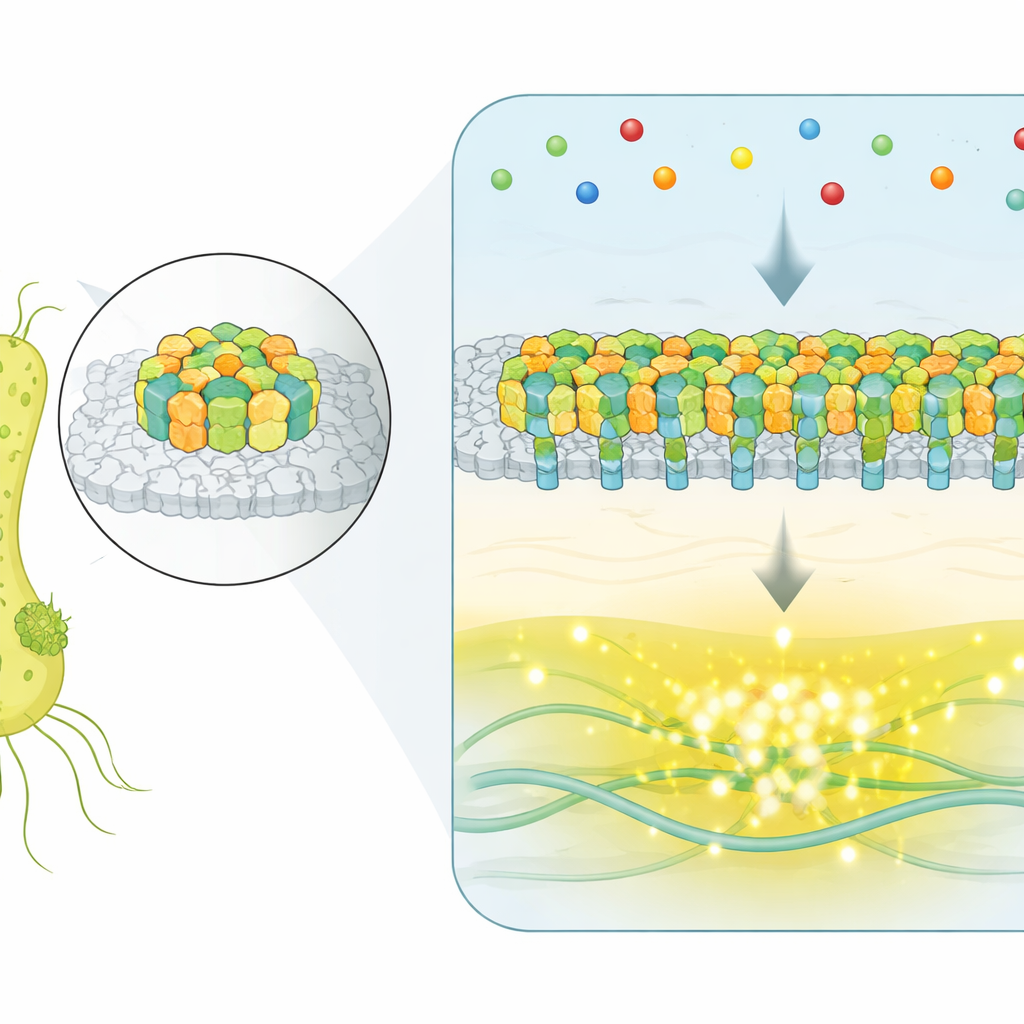
Capturando inversões de todo o arranjo em tempo real
Para observar os arranjos em ação dentro de células vivas, os pesquisadores usaram uma técnica de fluorescência que reporta a atividade de uma enzima de sinalização chave. Eles construíram cepas nas quais um único arranjo dominante controla a célula inteira e então monitoraram milhares de bactérias individuais ao longo do tempo, mesmo quando o ambiente químico externo era mantido constante. Em uma fração substancial de células, a saída não apenas tremeluzia aleatoriamente — ela alternava de forma nítida entre dois níveis bem definidos: um estado totalmente LIGADO e um totalmente DESLIGADO. Essa comutação espontânea em dois níveis é uma marca de sistemas cooperativos, nos quais muitos componentes atuam juntos em vez de independentemente.
Um modelo físico para decisões proteicas
Para entender essas inversões abruptas, os autores recorreram a um modelo clássico da física, o modelo de Ising, originalmente desenvolvido para descrever como spins se alinham em um ímã. Na adaptação deles, cada unidade receptora no arranjo pode estar ativa ou inativa, e unidades vizinhas preferem coincidir entre si. Simulações por computador mostraram que, quando o acoplamento entre vizinhos é fraco, a atividade apenas oscila em torno de um valor médio. Mas quando o acoplamento é ajustado muito próximo a um limiar crítico, toda a rede ocasionalmente salta entre estados quase todos-ativos e quase todos-inativos, com estatísticas que coincidem de perto com os dados experimentais. Ao comparar tempos de comutação e durações em muitas células com essas simulações, a equipe inferiu que arranjos bacterianos reais se situam a poucos por cento desse ponto crítico.
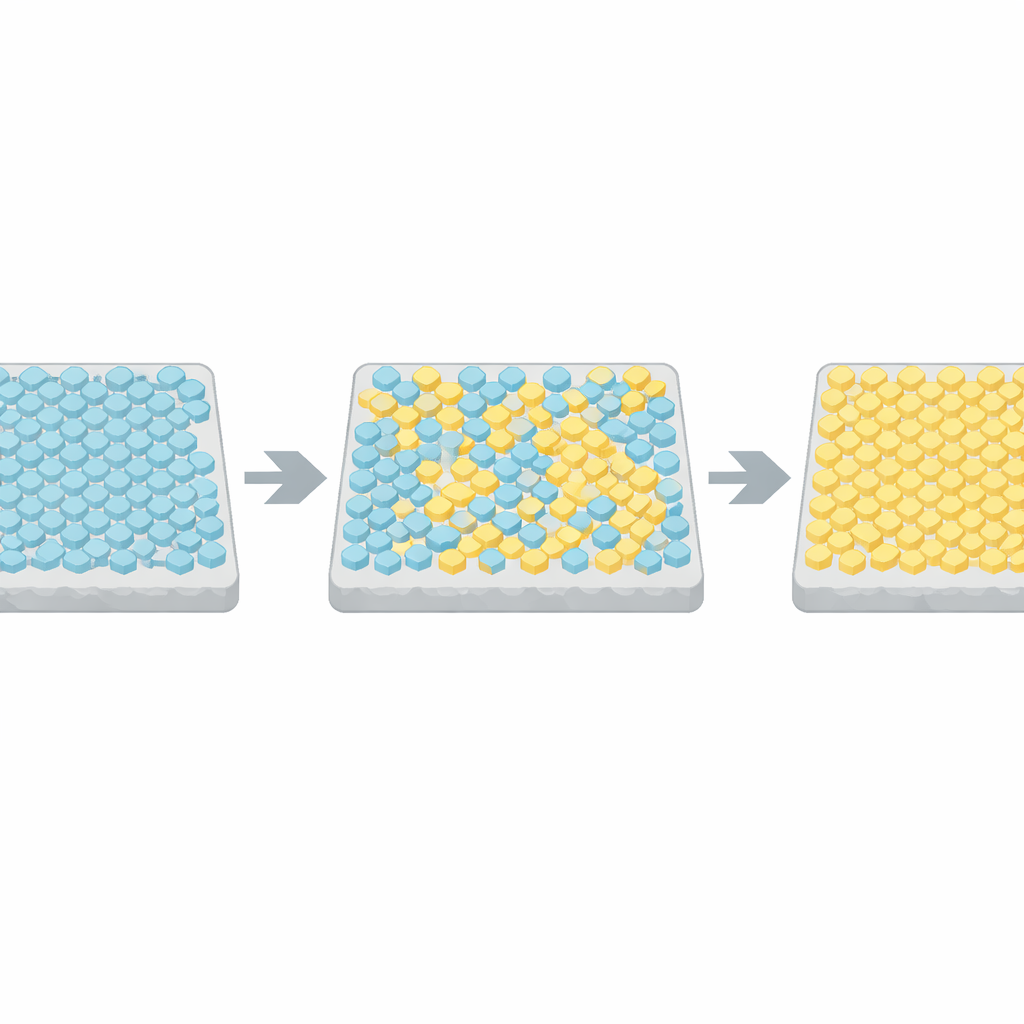
Equilibrando velocidade e intensidade da resposta
Operar perto da criticidade tem um custo. O forte acoplamento entre receptores amplifica muito entradas pequenas, mas também retarda a capacidade do sistema de mudar de estado — um fenômeno conhecido como desaceleração crítica. As simulações previram que arranjos quase-críticos poderiam levar dezenas de segundos para responder a um novo estímulo, tempo excessivo para bactérias que se reorientam aproximadamente uma vez por segundo. Os autores testaram isso diretamente impondo passos químicos rápidos usando dispositivos microfluídicos. Células projetadas para ter arranjos altamente uniformes, sem sua maquinaria normal de adaptação, de fato responderam muito lentamente, confirmando o trade-off entre tamanho da resposta e velocidade de resposta.
Usando a desordem como um recurso de projeto
As bactérias selvagens, porém, não ficam presas a esse comportamento lento. Seus arranjos geralmente misturam diferentes espécies de receptores e são constantemente modificados por enzimas que ajustam a sensibilidade por meio de marcas químicas. Ambos os efeitos introduzem uma espécie de “desordem” espacial e temporal na rede por outro modo ordenada. As simulações e experimentos do estudo mostraram que essa desordem suaviza efetivamente a cooperatividade o suficiente para evitar uma desaceleração severa, preservando ainda uma forte amplificação e flutuações naturais substanciais na saída de sinalização. Acredita-se que essas flutuações, ou ruído, ajudem E. coli a explorar melhor o ambiente ao variar seus padrões de natação.
Vida na borda entre ordem e caos
Os autores concluem que a cooperatividade quase-crítica é um princípio central de projeto do arranjo quimiossensorial bacteriano. O arranjo é ajustado para ficar próximo a um ponto de inflexão físico onde pequenas pistas químicas podem desencadear respostas grandes e coordenadas, mas é temperado por desordem incorporada de modo que as decisões permaneçam rápidas e flexíveis. Este trabalho conecta ideias abstratas da física estatística a comportamentos concretos em células vivas, sugerindo que muitas montagens proteicas — e talvez dispositivos moleculares sintéticos do futuro — possam ser projetados para operar nesse delicado equilíbrio entre sensibilidade e velocidade.
Citação: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
Palavras-chave: quimiotaxia bacteriana, arranjos de sinalização proteica, criticidade na biologia, receptores cooperativos, tomada de decisão celular