Clear Sky Science · es
Cambios espontáneos en una matriz de señalización proteica revelan cooperatividad casi crítica
Cómo toman decisiones en fracciones de segundo las bacterias
Las bacterias pueden ser diminutas, pero constantemente toman decisiones de vida o muerte: nadar hacia el alimento, huir de toxinas o seguir en línea recta. Este estudio examina el interior de la “antena” molecular que permite a la bacteria intestinal Escherichia coli detectar químicos y orientarse. Los autores muestran que estas antenas operan justo en el filo entre el orden y el desorden —un régimen físico conocido como criticidad—, lo que permite a las bacterias responder con fuerza a señales débiles sin volverse lentas.
Una sala de control molecular en la superficie celular
En lugar de usar receptores individuales y aislados, E. coli agrupa miles de proteínas sensoras en un parche plano y cristalino en su superficie celular. Estos parches, llamados matrices quimiosensoras, detectan moléculas del entorno y controlan los motores que hacen girar los flagelos de la bacteria. Cuando moléculas atrayentes se unen a los receptores, una red interna de enzimas reduce la actividad de una quinasa que normalmente promueve el “tumbling” (giros), inclinando a la célula hacia carreras más largas y rectas hacia condiciones mejores. La gran pregunta ha sido cómo asambleas tan grandes coordinan sus muchas piezas para producir señales precisas y fiables.
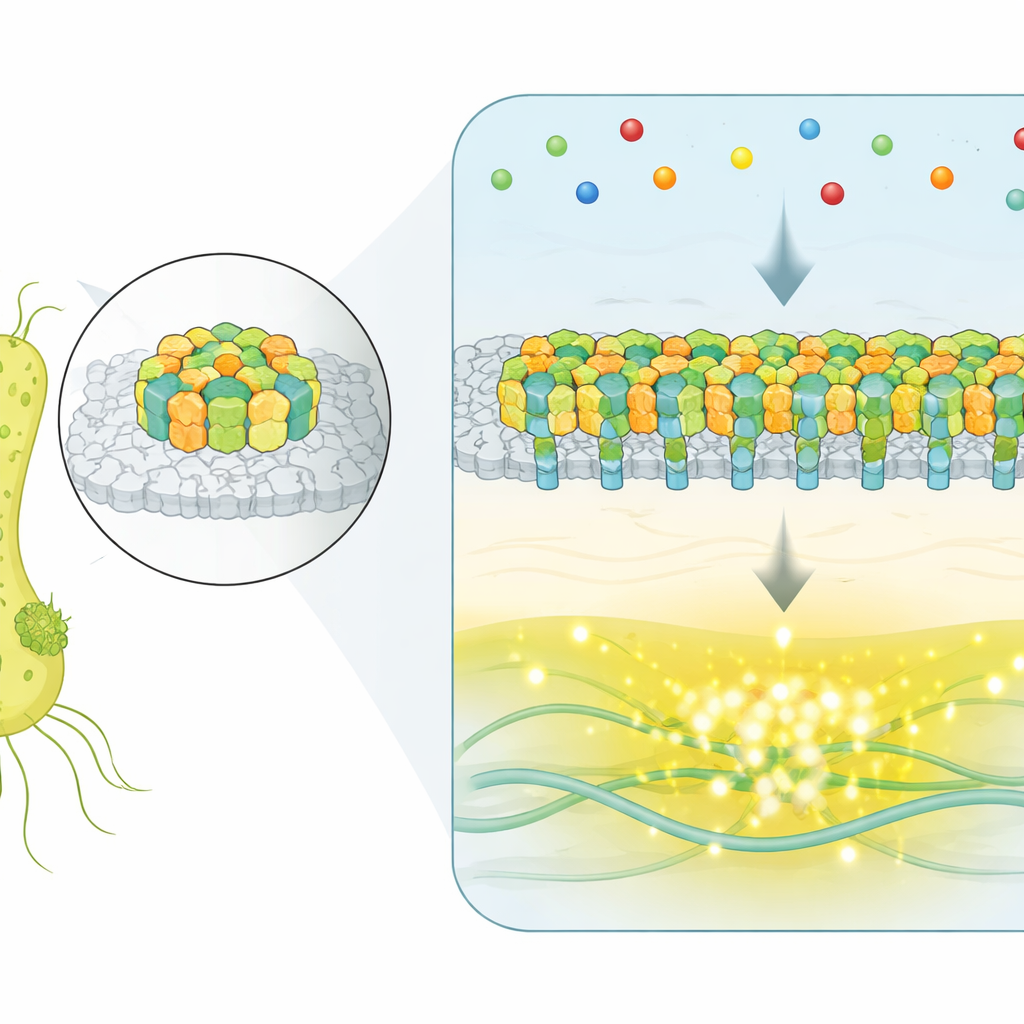
Capturar los volteos de la matriz completa en tiempo real
Para observar las matrices en acción dentro de células vivas, los investigadores emplearon una técnica de fluorescencia que informa sobre la actividad de una enzima clave de señalización. Diseñaron cepas en las que una única matriz dominante controla toda la célula y luego monitorizaron miles de bacterias individuales a lo largo del tiempo, incluso cuando el entorno químico externo se mantenía constante. En una fracción considerable de células, la salida no se limitó a parpadear de forma aleatoria: cambiaba bruscamente entre dos niveles bien definidos: un estado TODO-ENCENDIDO y un estado TODO-APAGADO. Este cambio espontáneo de dos niveles es una marca de los sistemas cooperativos, donde muchos componentes actúan juntos en lugar de independientemente.
Un modelo físico para decisiones proteicas
Para entender estos volteos abruptos, los autores recurrieron a un modelo clásico de la física, el modelo de Ising, desarrollado originalmente para describir cómo se alinean los espines en un imán. En su adaptación, cada unidad receptora en la matriz puede estar activa o inactiva, y las unidades vecinas prefieren coincidir entre sí. Las simulaciones por ordenador mostraron que cuando el acoplamiento entre vecinos es débil, la actividad simplemente titubea alrededor de un valor intermedio. Pero cuando el acoplamiento se ajusta muy cerca de un umbral crítico, toda la red salta ocasionalmente entre estados casi totalmente activos y casi totalmente inactivos, con estadísticas que coincidían estrechamente con los datos experimentales. Comparando los tiempos y las duraciones de los cambios en muchas células con estas simulaciones, el equipo dedujo que las matrices bacterianas reales se sitúan a pocos porcentajes de ese punto crítico.
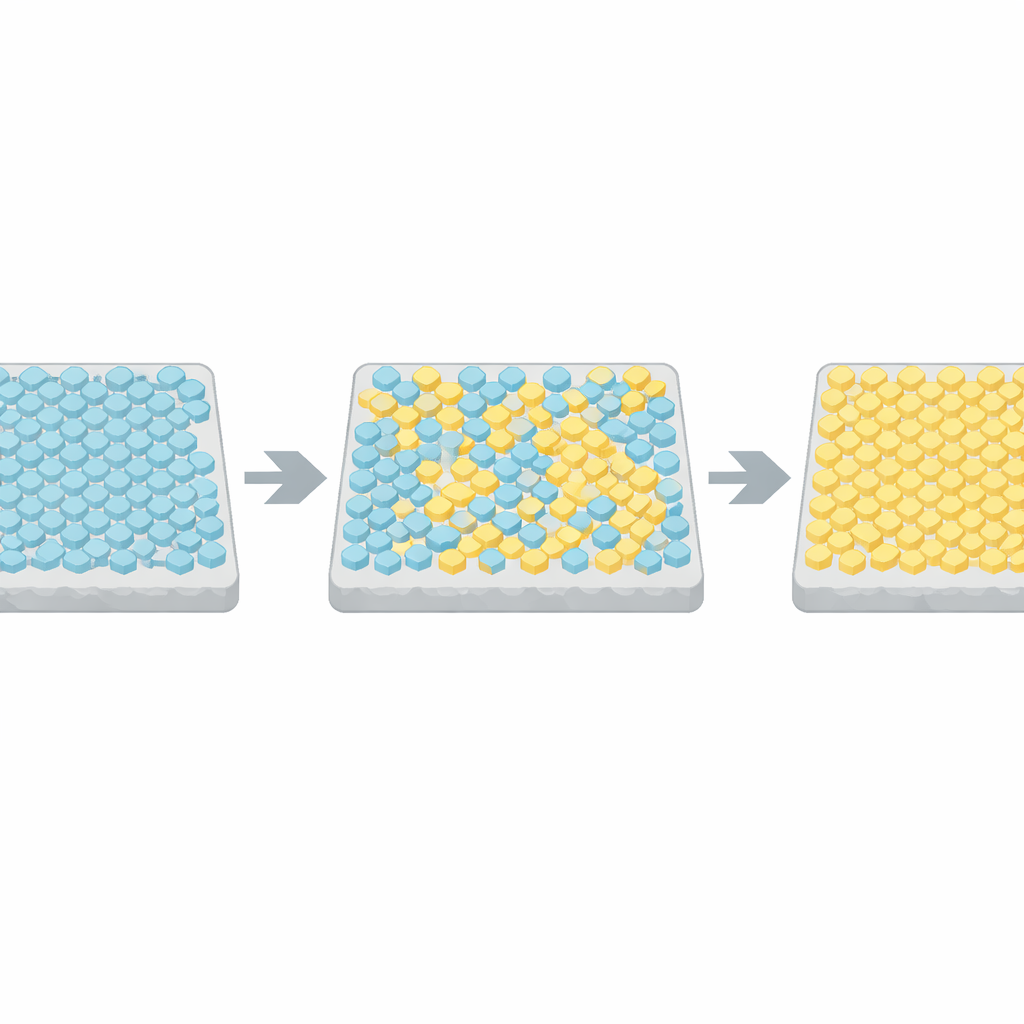
Equilibrar la rapidez y la intensidad de la respuesta
Operar cerca de la criticidad tiene un precio. Un acoplamiento fuerte entre receptores amplifica mucho las entradas pequeñas, pero también ralentiza la capacidad del sistema para cambiar de estado —un fenómeno conocido como desaceleración crítica. Las simulaciones predijeron que las matrices cercanas al crítico podrían tardar decenas de segundos en responder a un nuevo estímulo, demasiado lento para bacterias que se reorientan aproximadamente una vez por segundo. Los autores probaron esto directamente imponiendo cambios químicos rápidos mediante dispositivos microfluídicos. Las células diseñadas para tener matrices muy uniformes, sin su maquinaria normal de adaptación, respondieron efectivamente de forma muy lenta, confirmando el equilibrio entre tamaño de la respuesta y velocidad de respuesta.
Usar el desorden como una característica de diseño
Sin embargo, las bacterias silvestres no están condenadas a un comportamiento tan lento. Sus matrices suelen mezclar distintas especies de receptores y están constantemente modificadas por enzimas que ajustan la sensibilidad mediante marcas químicas. Ambos efectos introducen una especie de “desorden” espacial y temporal en la retícula por lo demás ordenada. Las simulaciones y experimentos del estudio mostraron que ese desorden ablanda eficazmente la cooperatividad lo suficiente como para evitar una desaceleración severa, manteniendo al mismo tiempo una fuerte amplificación y fluctuaciones naturales sustanciales en la señal. Se piensa que estas fluctuaciones, o ruido, ayudan a E. coli a explorar su entorno con más eficacia variando sus patrones de nado.
Vivir en el borde entre el orden y el caos
Los autores concluyen que la cooperatividad casi crítica es un principio de diseño central de la matriz quimiosensora bacteriana. La matriz está afinada para situarse cerca de un punto de inflexión físico donde pequeñas señales químicas pueden desencadenar respuestas grandes y coordinadas, pero está atemperada por un desorden incorporado para que las decisiones sigan siendo rápidas y flexibles. Este trabajo enlaza ideas abstractas de la física estadística con comportamientos tangibles en células vivas, y sugiere que muchos ensamblajes proteicos —y quizá dispositivos moleculares sintéticos del futuro— podrían diseñarse para operar en este delicado equilibrio entre sensibilidad y rapidez.
Cita: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
Palabras clave: quimiotaxis bacteriana, matrices de señalización proteica, criticidad en biología, receptores cooperativos, toma de decisiones celular