Clear Sky Science · tr
Bir protein sinyalizasyon dizisindeki kendiliğinden geçişler kritik eşiğe yakın işbirliğini ortaya koyuyor
Bakteriler Nasıl Ani Kararlar Alır?
Bakteriler küçük olabilir, ama sürekli yaşamı belirleyen kararlar alırlar: yiyeceğe doğru yüzmek, toksinlerden kaçmak veya düz gitmeye devam etmek. Bu çalışma, bağırsak bakterisi Escherichia coli’nin kimyasalları algılayıp yönlendirmesini sağlayan moleküler “anten”in içini inceliyor. Yazarlar, bu antenlerin düzen ile düzensizlik arasındaki keskin eşikte—fizikte kritiklik olarak bilinen bir rejimde—işlediğini gösteriyor; bu da bakterilerin zayıf sinyallere güçlü yanıt vermesini, fakat yavaşlamadan kaçınmasını sağlıyor.
Hücre Yüzeyinde Bir Moleküler Kontrol Odası
Tek, izole reseptörler kullanmak yerine E. coli binlerce algılayıcı proteini hücre yüzeyinde düz, kristalin bir yamada toplar. Bu yamalar, kemosezgisel diziler olarak adlandırılır; çevredeki molekülleri algılar ve bakterinin kamçılarını döndüren motorları kontrol eder. Cezbedici moleküller reseptörlere bağlandığında, içsel bir enzim ağı normalde tumbling (dönmeyi) teşvik eden bir kinazı baskılar, böylece hücre daha iyi koşullara doğru daha uzun ve düz hareketlere yönelir. Büyük soru, bu kadar büyük bir montajın birçok parçasını nasıl koordine ederek kesin, güvenilir sinyaller ürettiğidir.
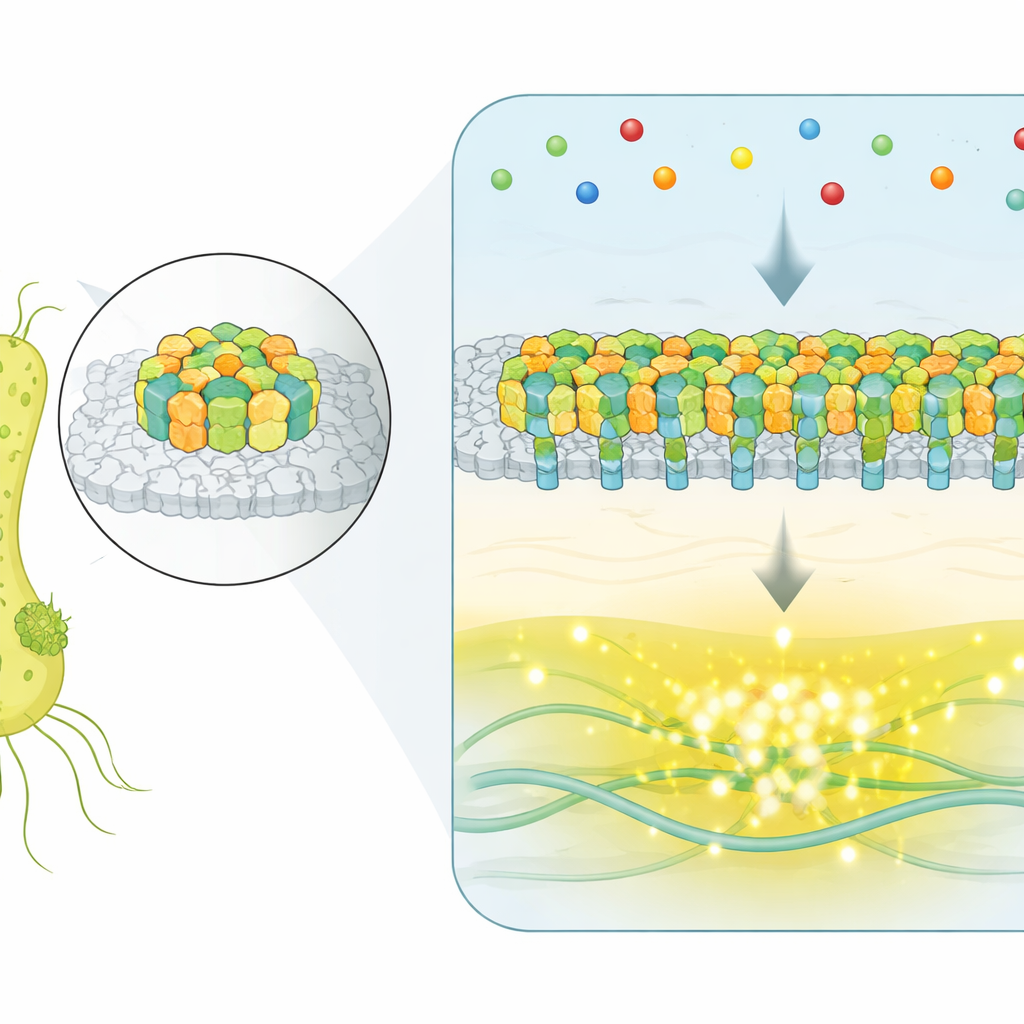
Tam Dizi Çarpışmalarını Gerçek Zamanlı Yakalamak
Dizileri yaşayan hücrelerin içinde eylem halinde izlemek için araştırmacılar, anahtar bir sinyal enziminin aktivitesini bildiren bir floresans tekniği kullandılar. Tek bir baskın dizinin tüm hücreyi kontrol ettiği suşlar tasarladılar ve ardından dış kimyasal ortam sabit tutulsa bile binlerce bireysel bakteriyi zaman içinde izlediler. Hücrelerin önemli bir kısmında çıktı sadece rastgele titremedi—iki iyi tanımlanmış seviye arasında gidip geliyordu: tamamen AÇIK ve tamamen KAPALI bir durum. Bu kendiliğinden iki seviyeli geçiş, pek çok bileşenin bağımsız yerine birlikte davrandığı işbirlikçi sistemlerin ayırt edici özelliğidir.
Protein Kararları İçin Bir Fizik Modeli
Bu ani geçişleri anlamak için yazarlar, manyetikte spinlerin nasıl hizalandığını açıklamak üzere geliştirilen klasik bir fizik modeli olan Ising modeline yöneldiler. Uyumlarında, dizideki her reseptör birimi aktif veya inaktif olabilir ve komşu birimlerin birbirine uymayı tercih ettiği varsayılıyor. Bilgisayar simulasyonları, komşular arasındaki bağlanma zayıf olduğunda aktivitenin orta bir değer etrafında titreştiğini gösterdi. Ancak bağlanma kritik bir eşikten çok yakın bir şekilde ayarlandığında, tüm örgü ara sıra neredeyse tamamen aktif ve neredeyse tamamen inaktif durumlar arasında atlıyor; bu geçişlerin istatistikleri deneysel verilerle yakından eşleşiyordu. Birçok hücredeki geçiş zamanları ve sürelerini bu simulasyonlarla karşılaştırarak ekip, gerçek bakteriyel dizilerin bu kritik noktaya birkaç yüzde puan içinde yerleştiği sonucuna ulaştı.
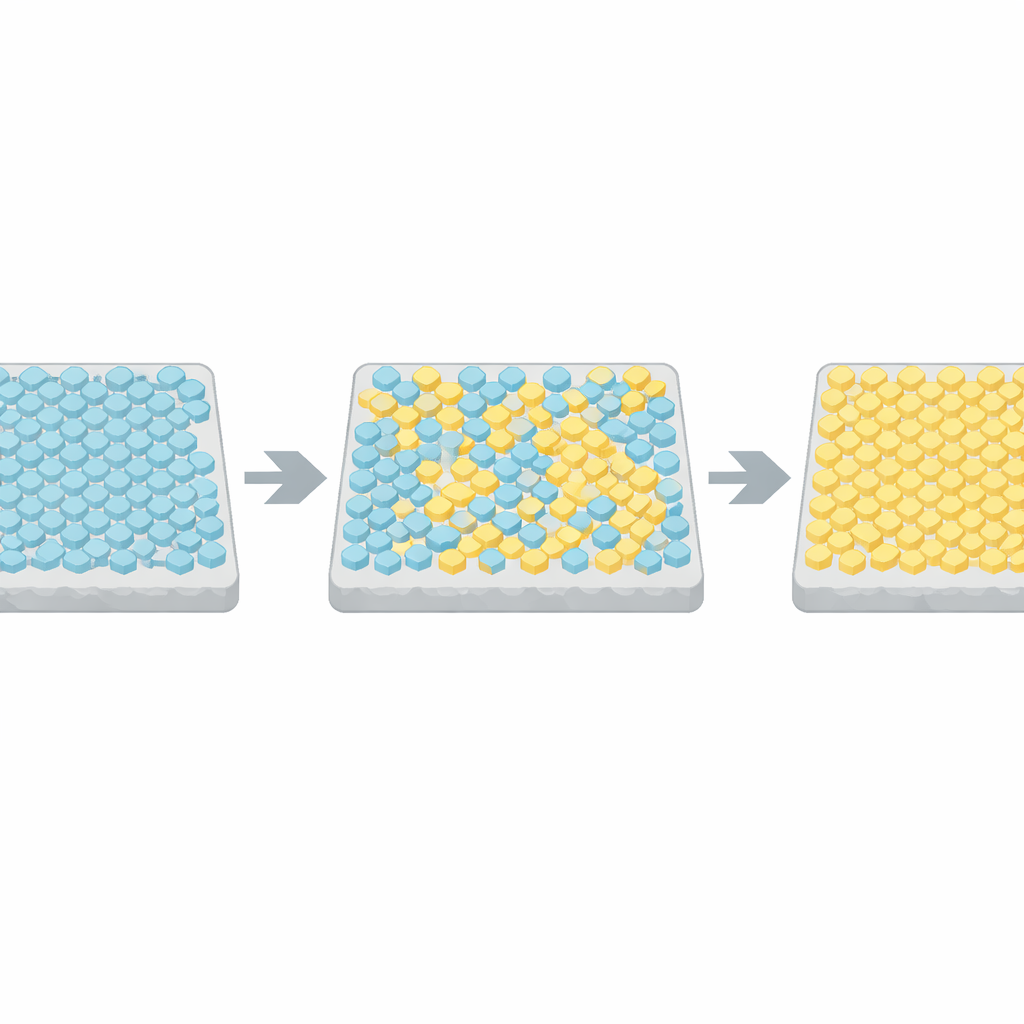
Yanıtın Hızı ve Gücü Arasındaki Denge
Kritikliğe yakın çalışmanın bir bedeli vardır. Reseptörler arasındaki güçlü bağlanma küçük girdileri büyük ölçüde güçlendirir, fakat aynı zamanda sistemin durum değiştirme yeteneğini de yavaşlatır—bu olgu kritik yavaşlama olarak bilinir. Simulasyonlar, kritikliğe yakın dizilerin yeni bir uyaranı yanıtlamak için onlarca saniye sürebileceğini; oysa bakterilerin yaklaşık her saniyede bir yön değiştirdiğini öngördü. Yazarlar bunu mikroakışkan cihazlarla hızlı kimyasal adımlar uygulayarak doğrudan test ettiler. Normal adaptasyon mekanizmalarından yoksun, oldukça tek tip dizilere sahip olacak şekilde tasarlanmış hücreler gerçekten çok yavaş yanıt verdi; bu da yanıt büyüklüğü ile yanıt hızı arasında bir takas olduğunu doğruladı.
Düzensizliği Bir Tasarım Özelliği Olarak Kullanmak
Ancak vahşi tip bakteriler bu kadar yavaş davranışla sınırlı değildir. Dizileri genellikle farklı reseptör türlerini karıştırır ve hassasiyeti kimyasal işaretlerle ayarlayan enzimler tarafından sürekli olarak değiştirilir. Her iki etki de düzenli örgüye mekânsal ve zamansal bir tür “düzensizlik” katar. Çalışmanın simulasyonları ve deneyleri, bu düzensizliğin işbirliğini şiddetli yavaşlamayı önleyecek kadar yumuşattığını, ancak yine de güçlü amplifikasyon ve sinyal çıktısında önemli doğal dalgalanmaları koruduğunu gösterdi. Bu dalgalanmalar ya da gürültü, E. coli’nin yüzme desenlerini değiştirerek çevresini daha etkili keşfetmesine yardımcı olduğu düşünülen bir özelliktir.
Düzen ile Kaos Arasındaki Kenarda Yaşam
Yazarlar, kritikliğe yakın işbirliğinin bakteriyel kemosezgisel dizinin temel bir tasarım ilkesi olduğunu sonuçlandırıyor. Dizi, küçük kimyasal ipuçlarının büyük, koordine tepkileri tetikleyebileceği fiziksel bir eşikle yakın olacak şekilde ayarlanmış; ancak kararların hızlı ve esnek kalmasını sağlamak için yerleşik düzensizlikle dengelenmiş. Bu çalışma, istatistiksel fiziğin soyut fikirlerini yaşayan hücrelerdeki somut davranışlarla ilişkilendiriyor ve birçok protein topluluğunun—ve belki geleceğin sentetik moleküler aygıtlarının—duyarlılık ile hız arasındaki bu hassas dengede çalışacak şekilde tasarlanabileceğini öne sürüyor.
Atıf: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
Anahtar kelimeler: bakteriyel kemotaksi, protein sinyalizasyon dizileri, biyolojide kritiklik, işbirlikçi reseptörler, hücresel karar verme