Clear Sky Science · sv
Spontan omkoppling i ett proteinsignaleringsnätverk avslöjar nästan-kritisk kooperativitet
Hur bakterier fattar splitsekundbeslut
Bakterier må vara små, men de fattar ständigt livsavgörande beslut: simma mot näring, fly från toxiner eller fortsätta rakt fram. Denna studie undersöker den molekylära ”antennen” som låter tarmbakterien Escherichia coli känna kemikalier och styra sin rörelse. Författarna visar att dessa antenner fungerar precis på knivseggen mellan ordning och oordning — ett fysikaliskt regime känt som kritikalitet — vilket gör att bakterier kan ge starka svar på svaga signaler utan att bli slöa.
En molekylär kontrollcentral på cellytan
I stället för att använda enstaka, isolerade receptorer samlar E. coli tusentals sensorproteiner i ett platt, kristallinliknande fält på cellytan. Dessa fält, kallade chemosensoriska arrayer, upptäcker molekyler i omgivningen och styr motorerna som driver bakteriens flageller. När attraktanter binder till receptorerna dämpar ett internt enzymnätverk en kinas som normalt främjar tumlande, vilket skjuter cellen mot längre, rakare löpningar mot bättre förhållanden. Den stora frågan har varit hur sådana stora sammankomster koordinerar sina många delar för att producera precisa, pålitliga signaler.
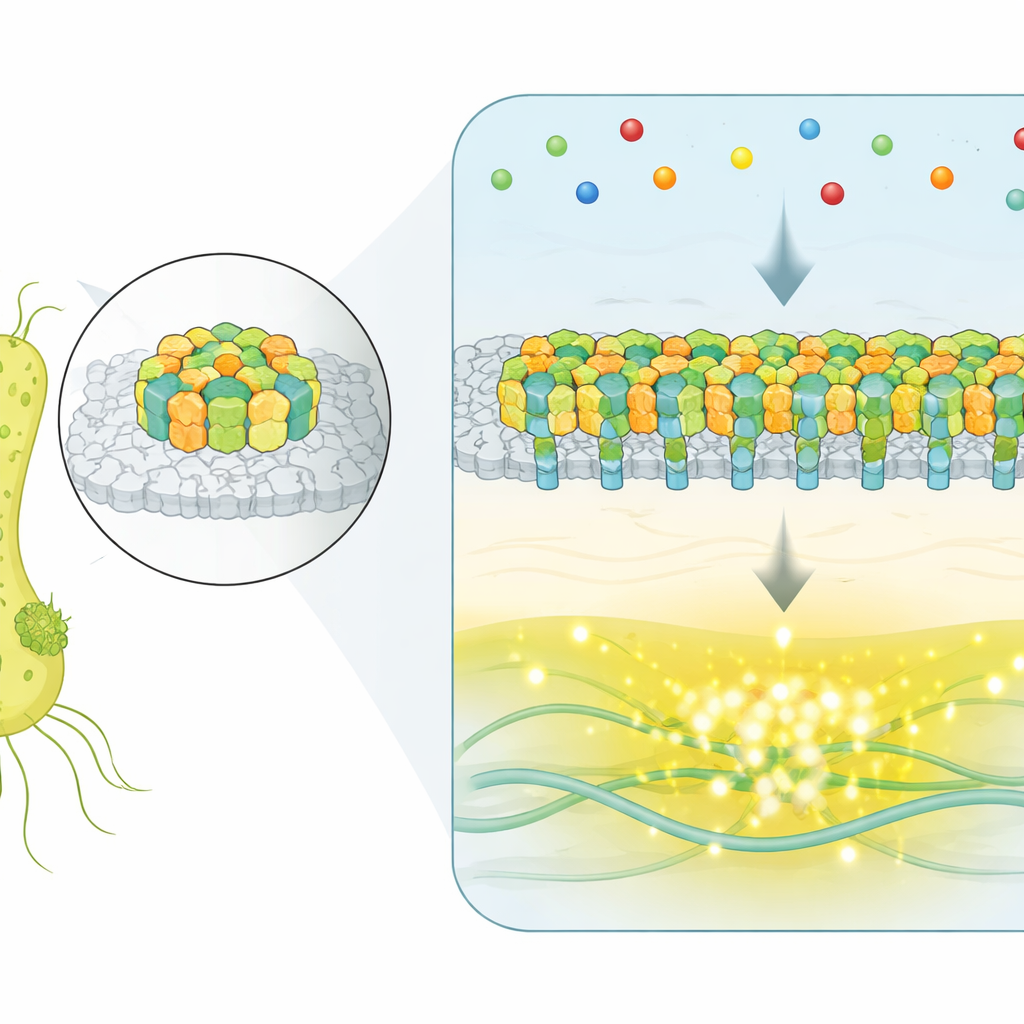
Fånga hel-array-omslag i realtid
För att se arrayerna i aktion inne i levande celler använde forskarna en fluorescensmetod som rapporterar aktiviteten hos ett nyckelenzym i signaleringen. De konstruerade stammar där en enda, dominerande array styr hela cellen och övervakade sedan tusentals individuella bakterier över tid, även när den yttre kemiska miljön hölls konstant. I en betydande andel celler fladdrade inte utsignalen bara slumpmässigt — den växlade tvärt fram och tillbaka mellan två väl definierade nivåer: ett helt PÅ- och ett helt AV-läge. Denna spontana tvånivå-omkoppling är ett kännetecken för kooperativa system, där många komponenter agerar tillsammans snarare än oberoende.
En fysikalisk modell för proteinbeslut
För att förstå dessa plötsliga omslag vände sig författarna till en klassisk modell från fysiken, Ising-modellen, ursprungligen utvecklad för att beskriva hur spinn i ett magnetfält anpassar sig. I deras anpassning kan varje receptorenhet i arrayen vara aktiv eller inaktiv, och närliggande enheter föredrar att stämma överens med varandra. Datorimuleringar visade att när kopplingen mellan grannar är svag, så jäser aktiviteten runt ett medelvärde. Men när kopplingen är inställd mycket nära en kritisk gräns hoppar hela gitteret ibland mellan nästan helt aktivt och nästan helt inaktivt, med statistik som stämde väl överens med de experimentella uppgifterna. Genom att jämföra växlingstider och varaktigheter över många celler med dessa simuleringar drog teamet slutsatsen att verkliga bakteriella arrayer befinner sig inom några procent av denna kritiska punkt.
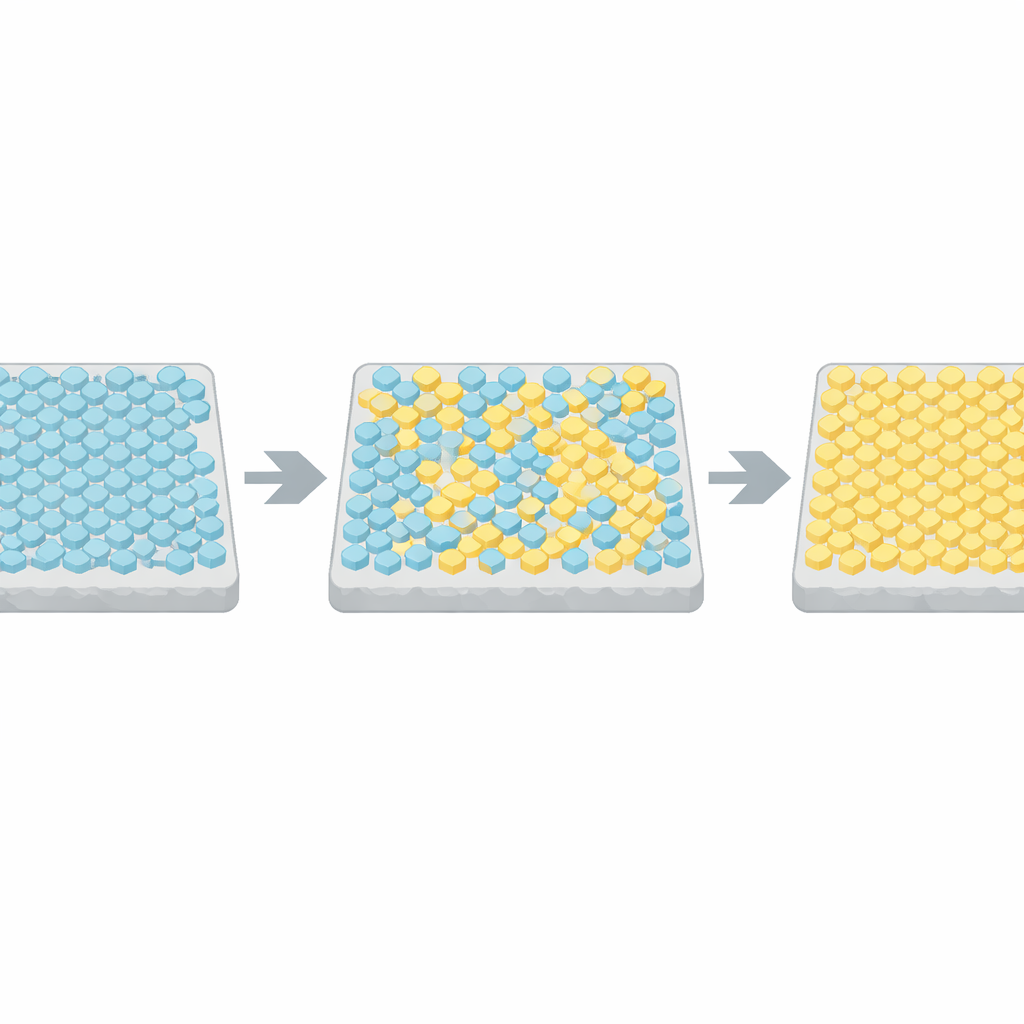
Att balansera svarsstyrka och svarshastighet
Att operera nära kritikalitet har en pris. Stark koppling mellan receptorer förstärker små insignaleringar kraftigt, men bromsar också systemets förmåga att byta tillstånd — ett fenomen känt som kritisk avtrappning. Simuleringar förutspådde att nära-kritiska arrayer kan ta tiotals sekunder att svara på ett nytt stimulus, för långsamt för bakterier som reorienterar ungefär en gång per sekund. Författarna testade detta direkt genom att införa snabba kemiska steg med hjälp av mikrofluida enheter. Celler konstruerade för att ha mycket homogena arrayer, utan deras normala anpassningsmaskineri, svarade faktiskt mycket långsamt, vilket bekräftade avvägningen mellan svarsstorlek och svarshastighet.
Använda oordning som en konstruktiv egenskap
Vilda stammar är emellertid inte fångade i sådan slöhet. Deras arrayer blandar vanligtvis olika receptorsorter, och de modifieras ständigt av enzymer som justerar känsligheten via kemiska märkningar. Båda effekterna inför en sorts rumslig och tidsmässig ”oordning” i det annars ordnade gitteret. Studiens simuleringar och experiment visade att denna oordning effektivt mjukar upp kooperativiteten precis så mycket att allvarlig avtrappning undviks, samtidigt som stark förstärkning och betydande naturliga fluktuationer i signalutgången bevaras. Dessa fluktuationer, eller brus, tros hjälpa E. coli att utforska sin omgivning mer effektivt genom att variera sina simmönster.
Liv på gränsen mellan ordning och kaos
Författarna drar slutsatsen att nästan-kritisk kooperativitet är en grundläggande designprincip för den bakteriella chemosensoriska arrayen. Arrayen är inställd att ligga nära en fysisk tippingpunkt där små kemiska signaler kan utlösa stora, koordinerade svar, men den dämpas av inbyggd oordning så att besluten förblir snabba och flexibla. Detta arbete kopplar abstrakta idéer från statistisk fysik till påtagligt beteende i levande celler och antyder att många proteinmonteringar — och kanske framtida syntetiska molekylära enheter — kan konstrueras för att fungera i denna känsliga balans mellan känslighet och hastighet.
Citering: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
Nyckelord: bakteriell kemotaxi, proteinsignaleringsarrayer, kritikalitet i biologin, kooperativa receptorer, cellulärt beslutsfattande