Clear Sky Science · ru
Спонтанные переключения в белковом сигнальном массиве выявляют почти критическую кооперативность
Как бактерии принимают решения за доли секунды
Бактерии могут быть крошечными, но они постоянно принимают решения «на жизнь и смерть»: плыть к пище, избегать токсинов или продолжать движение прямо. В этом исследовании заглядывают внутрь молекулярной «антенны», которая позволяет кишечной бактерии Escherichia coli чувствовать химические вещества и направлять движение. Авторы показывают, что эти антенны работают прямо на острие между упорядоченностью и хаосом — в физическом режиме, известном как критичность — что позволяет бактериям сильно реагировать на слабые сигналы, не становясь при этом вялыми.
Молекулярная диспетчерская на поверхности клетки
Вместо отдельных разрозненных рецепторов E. coli собирает тысячи сенсорных белков в плоский кристаллический участок на поверхности клетки. Эти участки, называемые хемосенсорными массивами, обнаруживают молекулы в окружении и контролируют моторы, раскручивающие жгутики бактерии. Когда молекулы-привлекательные вещества связываются с рецепторами, внутренняя сеть ферментов понижает активность киназы, которая обычно способствует «покачиванию» (tumbling), подталкивая клетку к более длительным, прямым пробегам в сторону лучших условий. Главный вопрос заключался в том, как такие большие сборки координируют многочисленные части, чтобы выдавать точные и надежные сигналы.
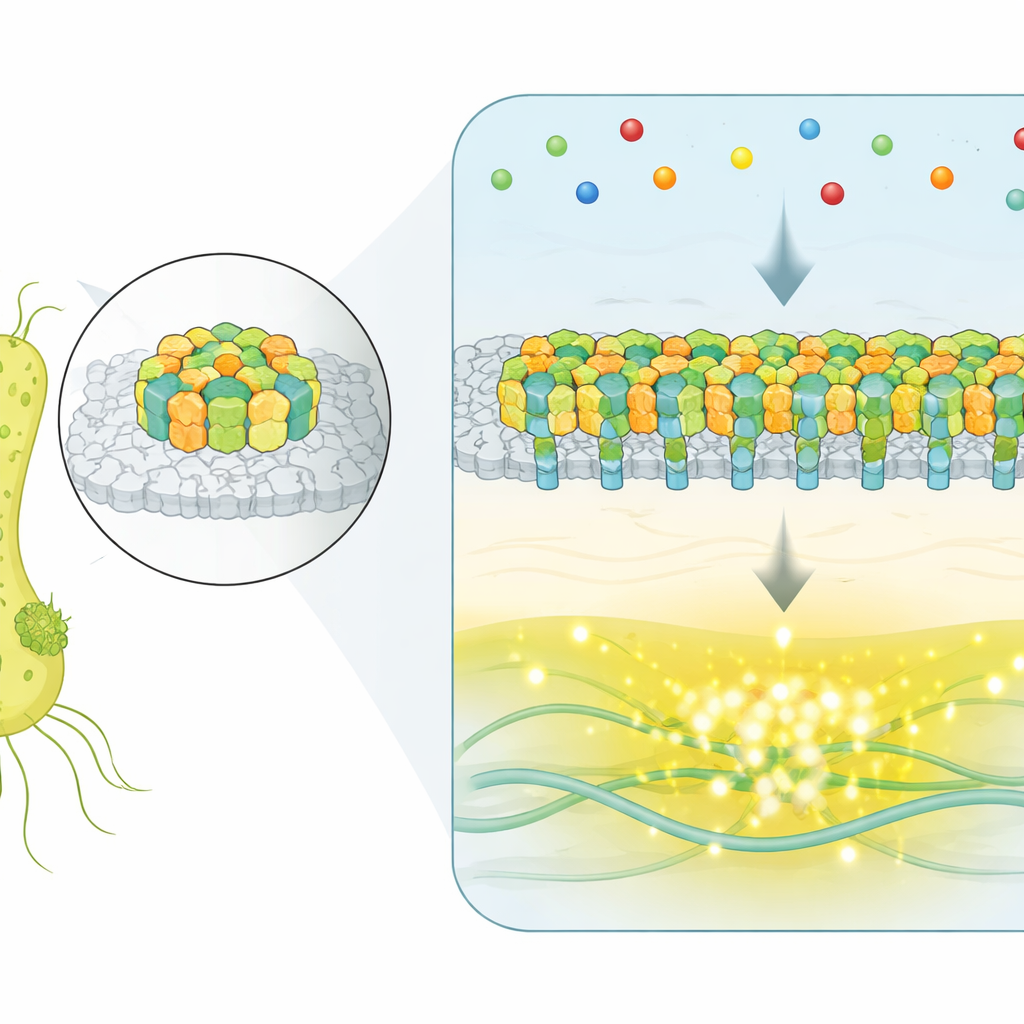
Наблюдение мгновенных перестроек всего массива в реальном времени
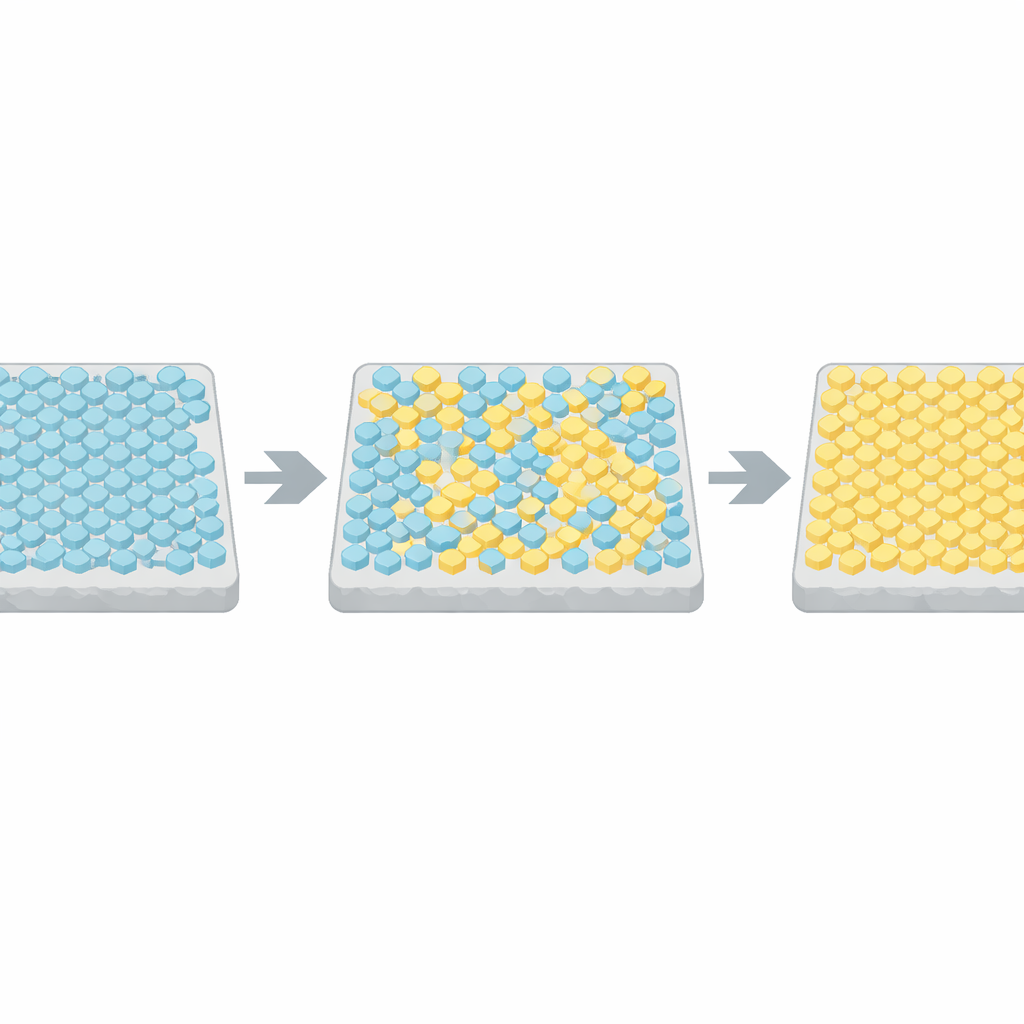
Чтобы наблюдать массивы в действии внутри живых клеток, исследователи использовали флуоресцентную методику, которая сообщает об активности ключевого сигнального фермента. Они сконструировали штаммы, в которых один доминирующий массив контролировал всю клетку, и затем отслеживали тысячи отдельных бактерий во времени, даже когда внешняя химическая среда оставалась постоянной. У значительной доли клеток выходной сигнал не просто флуктуационировал случайно — он переключался между двумя чётко выраженными уровнями: полностью ВКЛ и полностью ВЫКЛ. Это спонтанное двухуровневое переключение является отличительной чертой кооперативных систем, где многие компоненты действуют согласованно, а не независимо.
Физическая модель принятия решений белками
Чтобы понять эти резкие перепады, авторы обратились к классической модели из физики — модели Изинга, изначально разработанной для описания выравнивания спинов в магните. В их адаптации каждый рецепторный блок в массиве может быть активным или неактивным, а соседние блоки предпочитают соответствовать друг другу. Компьютерные симуляции показали, что когда связь между соседями слаба, активность лишь слегка дрожит вокруг среднего значения. Но когда связь настроена очень близко к критическому порогу, вся решётка время от времени прыгает между почти полностью активным и почти полностью неактивным состояниями, с статистикой, очень близкой к экспериментальным данным. Сравнивая времена переключений и длительности между многими клетками и симуляциями, команда вывела, что реальные бактериальные массивы находятся в пределах нескольких процентов от этой критической точки.
Баланс скорости и силы отклика
Работа вблизи критичности имеет свою цену. Сильная связь между рецепторами значительно усиливает малые входы, но также замедляет способность системы менять состояние — явление, известное как критическое замедление. Симуляции предсказывали, что массивы, находящиеся близко к критической точке, могут требовать десятков секунд на отклик на новый стимул — слишком медленно для бактерий, которые перенастраиваются примерно раз в секунду. Авторы проверили это напрямую, налагая быстрые химические ступенчатые изменения с помощью микрофлюидики. Клетки, сконструированные так, чтобы иметь очень однородные массивы без обычного механизма адаптации, действительно реагировали очень медленно, подтвердив компромисс между величиной отклика и скоростью реакции.
Использование беспорядка как конструктивной черты
Однако у диких штаммов бактерий нет такой вялой судьбы. Их массивы обычно смешивают разные виды рецепторов, и они постоянно модифицируются ферментами, которые корректируют чувствительность через химические метки. Оба эффекта вводят своего рода пространственный и временной «беспорядок» в иначе упорядоченную решётку. Симуляции и эксперименты в работе показали, что этот беспорядок эффективно ослабляет кооперативность чуть-чуть — достаточно, чтобы предотвратить сильное замедление, при этом сохраняя мощное усиление и значительные естественные флуктуации в выходном сигнале. Считается, что эти флуктуации, или шум, помогают E. coli эффективнее исследовать окружение за счёт разнообразия паттернов плавания.
Жизнь на грани порядка и хаоса
Авторы делают вывод, что почти критическая кооперативность — ключевой принцип устройства бактериального хемосенсорного массива. Массив настроен так, чтобы находиться близко к физической точке перегиба, где малые химические сигналы могут вызывать большие согласованные отклики, но при этом смягчается встроенным беспорядком, чтобы решения оставались быстрыми и гибкими. Эта работа связывает абстрактные идеи статистической физики с осязаемым поведением живых клеток, предлагая, что многие белковые сборки — а возможно, и синтетические молекулярные устройства будущего — могут быть сконструированы для работы в этой деликатной границе между чувствительностью и скоростью.
Цитирование: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
Ключевые слова: бактериальный хемотаксис, белковые сигнальные массивы, критичность в биологии, кооперативные рецепторы, клеточное принятие решений