Clear Sky Science · de
Spontanes Umschalten in einem Protein‑Signalisierungs‑Array zeigt nahezu kritische Kooperation
Wie Bakterien in Bruchteilen einer Sekunde entscheiden
Bakterien sind zwar winzig, aber sie treffen ständig Entscheidungen über Leben und Tod: zum Futter schwimmen, vor Toxinen fliehen oder geradeaus weiterschwimmen. Diese Studie blickt in die molekulare „Antenne“, mit der das Darmbakterium Escherichia coli Chemikalien wahrnimmt und seine Richtung steuert. Die Autorinnen und Autoren zeigen, dass diese Antennen genau an der Grenze zwischen Ordnung und Unordnung arbeiten — einem physikalischen Regime, das als Kritikalität bekannt ist —, was es den Bakterien ermöglicht, stark auf schwache Signale zu reagieren, ohne träge zu werden.
Ein molekularer Kontrollraum auf der Zelloberfläche
Anstatt einzelne, isolierte Rezeptoren zu nutzen, versammelt E. coli Tausende von Sensorproteinen zu einer flachen, kristallinen Struktur an seiner Zelloberfläche. Diese Patches, sogenannte chemosensorischen Arrays, detektieren Moleküle in der Umgebung und steuern die Motoren, die die Flagellen des Bakteriums antreiben. Wenn Lockstoffe an die Rezeptoren binden, reduziert ein internes Enzymnetzwerk die Aktivität einer Kinas e, die normalerweise das „Tumbling“ fördert, und veranlasst die Zelle so zu längeren, geraderen Läufen in günstigere Bedingungen. Die zentrale Frage war, wie solche großen Verbände ihre vielen Teile koordinieren, um präzise und verlässliche Signale zu erzeugen.
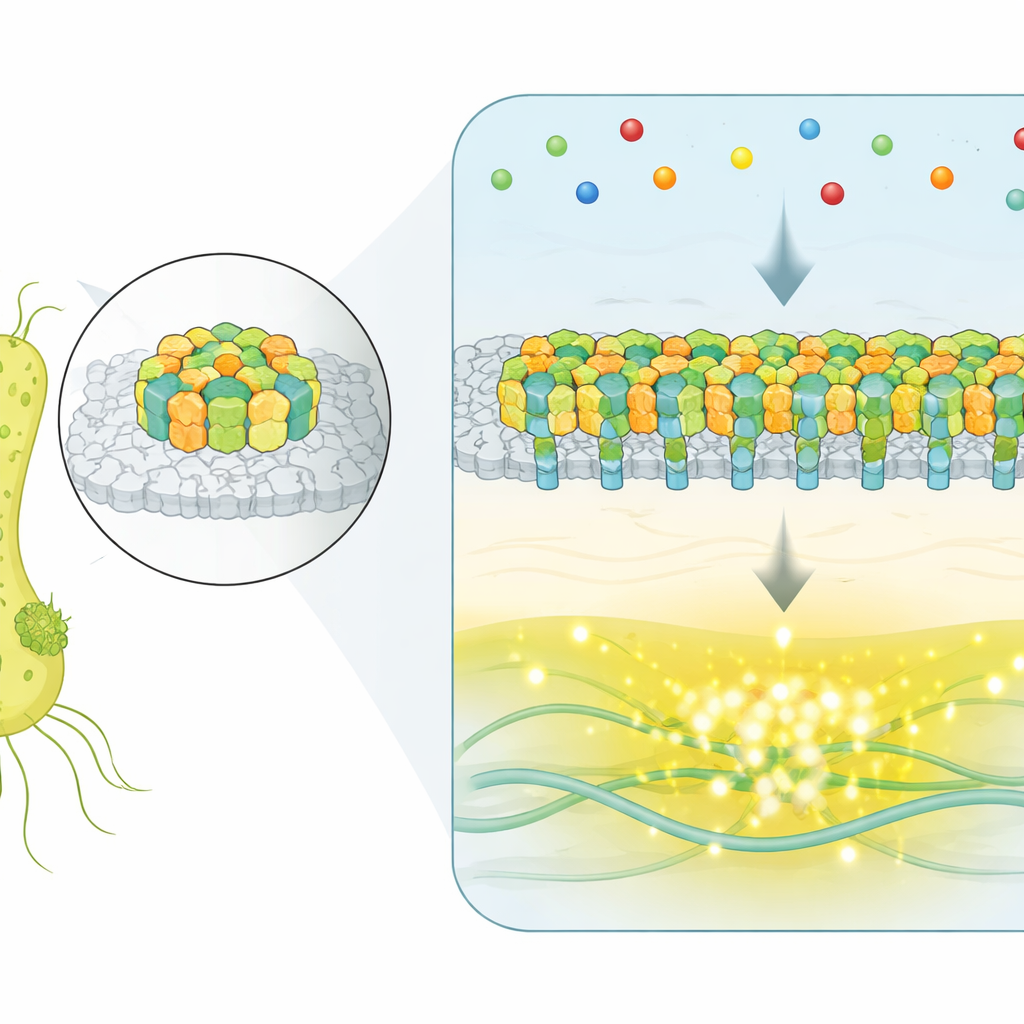
Ganzen Array‑Sprünge in Echtzeit einfangen
Um die Arrays in Aktion in lebenden Zellen zu beobachten, verwendeten die Forschenden eine Fluoreszenztechnik, die die Aktivität eines Schlüssel‑Signalenzymes anzeigt. Sie konstruierten Stämme, in denen ein einzelnes, dominantes Array die ganze Zelle kontrolliert, und überwachten dann tausende einzelne Bakterien über die Zeit, selbst bei konstant gehaltener äußerer chemischer Umgebung. In einem erheblichen Teil der Zellen zeigte die Ausgabe kein bloßes zufälliges Flattern — sie schaltete zwischen zwei klar definierten Pegeln hin und her: einem komplett AN‑ und einem komplett AUS‑Zustand. Dieses spontane Zwei‑Niveauschalten ist typisch für kooperative Systeme, in denen viele Komponenten zusammenwirken statt unabhängig zu handeln.
Ein Physikmodell für proteinbasierte Entscheidungen
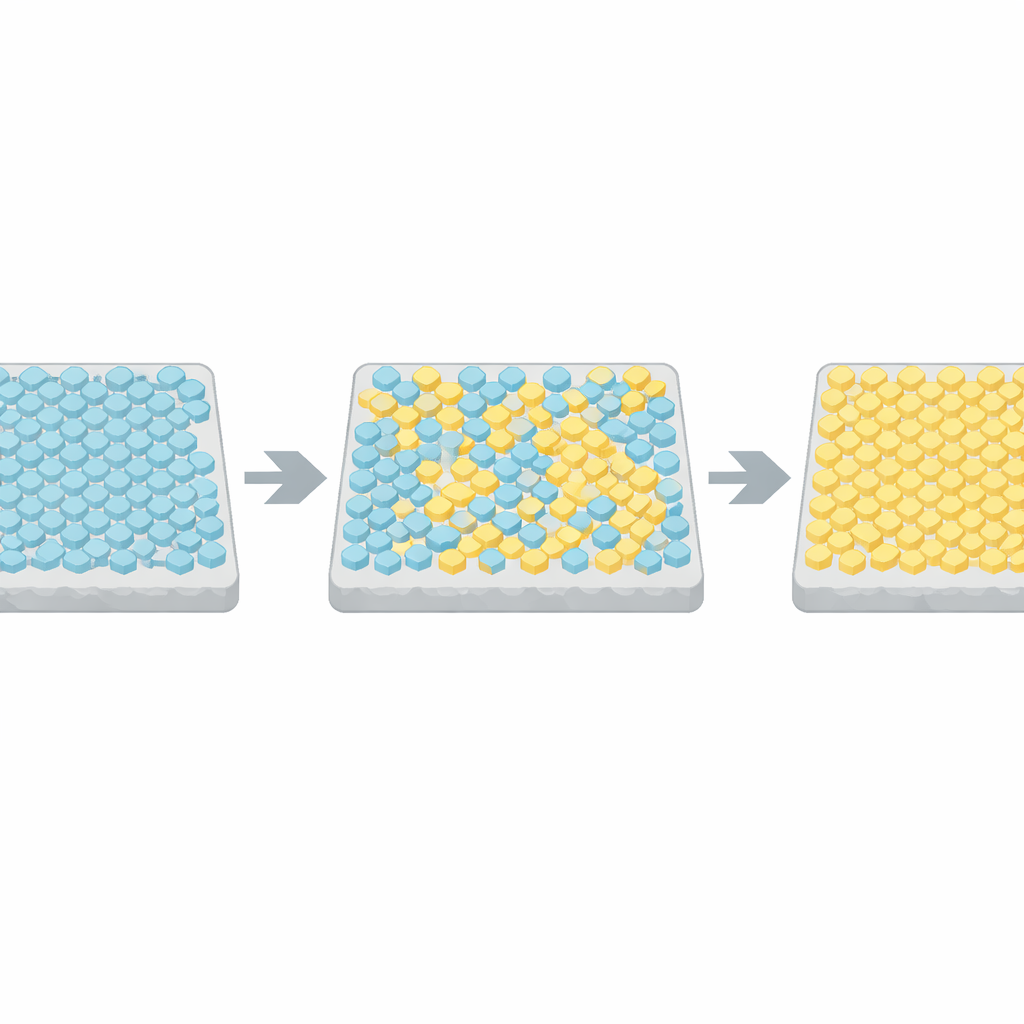
Um diese abrupten Umschläge zu verstehen, griffen die Autorinnen und Autoren auf ein klassisches Physikmodell zurück, das Ising‑Modell, ursprünglich entwickelt, um zu beschreiben, wie Spins in einem Magneten ausgerichtet sind. In ihrer Anpassung kann jede Rezeptoreinheit im Array aktiv oder inaktiv sein, und benachbarte Einheiten bevorzugen denselben Zustand. Computersimulationen zeigten, dass bei schwacher Kopplung zwischen Nachbarn die Aktivität lediglich um einen mittleren Wert herum schwankt. Wenn die Kopplung jedoch sehr nahe an eine kritische Schwelle eingestellt ist, springt das ganze Gitter gelegentlich zwischen nahezu vollständig aktivem und nahezu vollständig inaktivem Zustand, mit Statistiken, die gut zu den experimentellen Daten passen. Durch den Vergleich von Schaltzeiten und -dauern vieler Zellen mit diesen Simulationen schloss das Team, dass reale bakterielle Arrays innerhalb weniger Prozent dieses kritischen Punktes liegen.
Abwägung zwischen Geschwindigkeit und Stärke der Reaktion
Das Arbeiten nahe der Kritikalität hat seinen Preis. Starke Kopplung zwischen Rezeptoren verstärkt kleine Eingänge erheblich, verlangsamt aber auch die Fähigkeit des Systems, den Zustand zu wechseln — ein Phänomen, das als kritische Verlangsamung bekannt ist. Simulationen sagten voraus, dass nahe‑kritische Arrays zig Sekunden benötigen könnten, um auf einen neuen Stimulus zu reagieren, was für Bakterien, die sich ungefähr einmal pro Sekunde neu ausrichten, zu langsam wäre. Die Autorinnen und Autoren prüften das direkt, indem sie schnelle chemische Schritte mit mikrofluidischen Geräten aufzwangen. Zellen, die so konstruiert waren, dass sie sehr uniforme Arrays besaßen, ohne ihre normale Adaptationsmaschinerie, reagierten tatsächlich sehr langsam und bestätigten damit den Kompromiss zwischen Reaktionsgröße und Reaktionsgeschwindigkeit.
Unordnung als Gestaltungsmerkmal nutzen
Wildtyp‑Bakterien sind jedoch nicht zu solcher Trägheit verdammt. Ihre Arrays mischen üblicherweise verschiedene Rezeptorspezies, und sie werden ständig von Enzymen modifiziert, die die Empfindlichkeit durch chemische Markierungen anpassen. Beide Effekte führen eine Art räumlicher und zeitlicher „Unordnung“ in das sonst geordnete Gitter ein. Die Simulationen und Experimente der Studie zeigten, dass diese Unordnung die Kooperativität effektiv so abmildert, dass starke Verlangsamung verhindert wird, während die starke Verstärkung und beträchtliche natürliche Schwankungen im Signaloutput erhalten bleiben. Man geht davon aus, dass diese Fluktuationen oder Rauschen E. coli dabei helfen, seine Umgebung effektiver zu erkunden, indem sie seine Schwimmmuster variieren.
Leben am Rande von Ordnung und Chaos
Die Autorinnen und Autoren kommen zu dem Schluss, dass nahezu kritische Kooperativität ein zentrales Gestaltungsprinzip des bakteriellen chemosensorischen Arrays ist. Das Array ist so eingestellt, dass es nahe an einem physikalischen Kipppunkt sitzt, an dem kleine chemische Reize große, koordinierte Reaktionen auslösen können, aber durch eingebaute Unordnung abgeschwächt wird, sodass Entscheidungen schnell und flexibel bleiben. Diese Arbeit verbindet abstrakte Ideen der statistischen Physik mit greifbarem Verhalten in lebenden Zellen und legt nahe, dass viele Proteinverbände — und vielleicht auch synthetische molekulare Geräte der Zukunft — so konstruiert werden könnten, in diesem empfindlichen Gleichgewicht zwischen Sensitivität und Geschwindigkeit zu operieren.
Zitation: Keegstra, J.M., Avgidis, F., Usher, E. et al. Spontaneous switching in a protein signalling array reveals near-critical cooperativity. Nat. Phys. 22, 452–460 (2026). https://doi.org/10.1038/s41567-025-03158-3
Schlüsselwörter: bakterielle Chemotaxis, Protein‑Signalisierungs‑Arrays, Kritikalität in der Biologie, kooperative Rezeptoren, zelluläre Entscheidungsfindung