Clear Sky Science · zh
经验性阿奇霉素改变上呼吸道微生物组和耐药基因组,但对 COVID-19 无抗炎益处
这对日常使用抗生素有何意义
在 COVID-19 大流行初期,许多人被给予阿奇霉素,寄望于其能抑制有害炎症或帮助对抗病毒。本研究提出了一个看似简单却至关重要的问题:大量额外使用抗生素究竟在患者的鼻腔和咽喉——病毒首先定植的地方——造成了什么影响?通过追踪超过一千名住院成人,研究者显示阿奇霉素明显扰动了上气道的微生物群落并促进了抗生素耐药基因的增多——但并未带来期望的抗炎益处。
研究如何设计
科学家利用了一项在美国全国范围内展开的项目,跟踪了 2020 至 2021 年间在 20 家医院住院的 1,164 名 COVID-19 成人患者。患者自然分为三组:经验性使用阿奇霉素者、服用其他抗生素者和未使用抗生素者。研究团队从反复采集的鼻拭子样本中,使用称为转录组元分析(metatranscriptomics)的技术读取哪些微生物处于活跃状态及哪些耐药基因被表达。他们还对血液和鼻部细胞中的免疫相关基因进行测序,以评估阿奇霉素是否改变患者的炎症反应。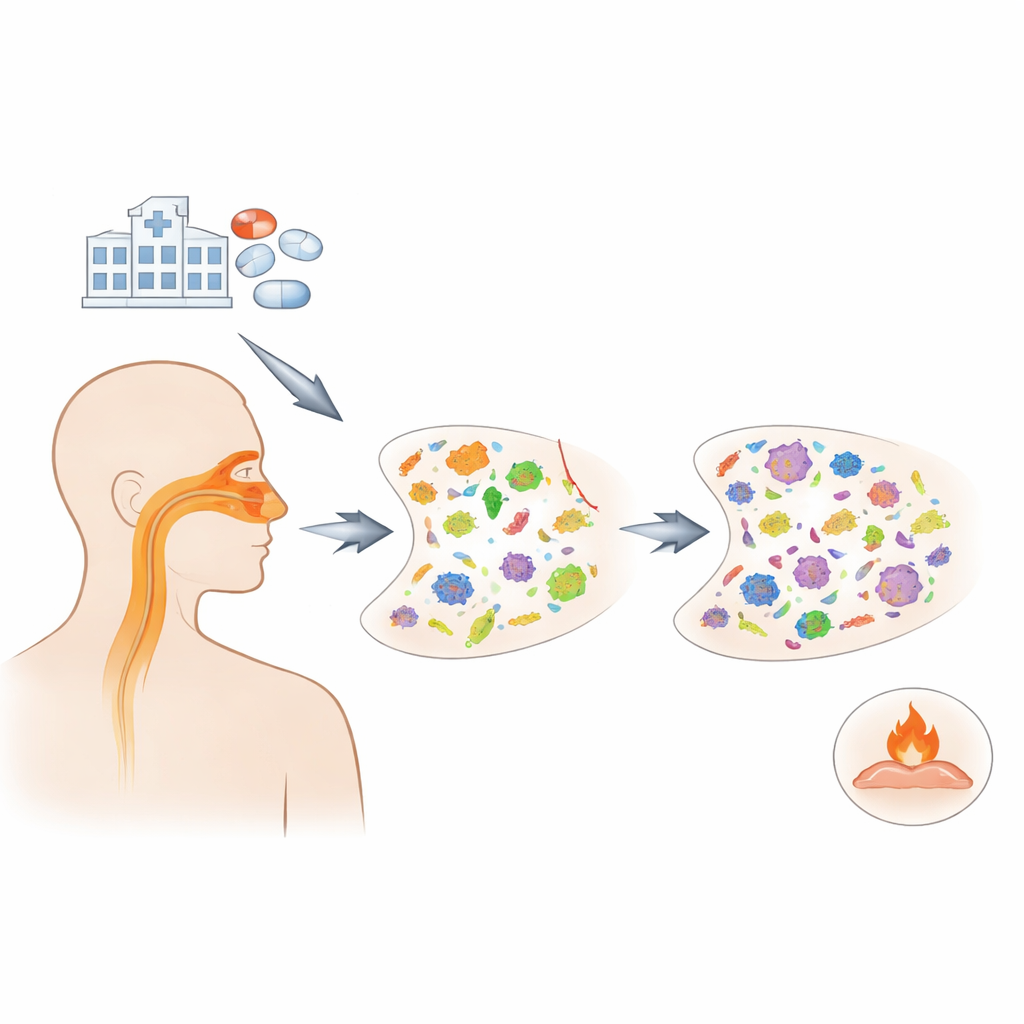
气道中微生物的变化
在开始使用阿奇霉素后仅一天内,鼻腔中细菌的总量就减少了,这种下降在大约五天治疗后仍然明显。但损失并非均匀分布。通常无害地生活在上呼吸道的微生物,如奈瑟菌属(Neisseria)和梭杆菌属(Fusobacterium),趋于减少。与此同时,某些可致病的物种,包括一些葡萄球菌(Staphylococcus)和克雷伯氏菌(Klebsiella),出现更常见的趋势。真菌在同一时期也有所上升,这提示当细菌邻居被压制时,其他生物可能会进入被腾空的生态位。
耐药基因的隐性变化
除了统计哪类微生物存在外,研究者还关注“耐药基因组”(resistome)——使细菌能耐受抗生素的一组基因。阿奇霉素属于大环内酯类药物,团队发现对大环内酯及相关药物的耐药基因迅速扩增。仅在用药几天后,阿奇霉素组中被积极表达的不同大环内酯耐药基因数量比未用抗生素或使用其他药物的患者高出约 50% 至 70%。这些大环内酯耐药基因在整体耐药基因组中的比例几乎翻倍,值得注意的是,这些变化在停药后一周或更久仍持续存在。
哪些微生物携带了新的防御技能
通过将耐药基因与存在的细菌相关联,研究把这些大环内酯耐药工具联系到既有的常见病原体和通常无害的共生菌。潜在致病菌如葡萄球菌(Staphylococcus)和链球菌(Streptococcus)与关键耐药基因(例如 ermA 和 msrA)强相关,这表明常见的肺炎致病菌在暴露于阿奇霉素后可能变得更难治疗。与此同时,鼻腔的日常常驻菌群,如棒状杆菌属(Corynebacterium)和 Dolosigranulum,也显示与耐药基因的关联,提示上呼吸道可能成为耐药性积累并潜在传播的安静储库。
没有观察到期望的抗炎效果
阿奇霉素在慢性肺病中以减轻炎症著称,因此许多临床医师希望它能抑制重症 COVID-19 中的失控免疫反应。然而,当研究者比较接受与未接受阿奇霉素患者的血液和鼻细胞中免疫基因活动模式时,未发现有意义的差异。鼻腔中的 SARS-CoV-2 病毒载量在各组间也类似。换言之,尽管该药明显重塑了微生物组和耐药基因组,但在住院患者中并未显现缓解有害炎症或降低病毒量的作用。
对患者和公共卫生的意义
总体而言,这些发现提供了一个值得警惕的图景。在这大规模住院病毒性感染队列中,经验性使用阿奇霉素未能提供可测量的抗炎或抗病毒益处,但确实促进了上呼吸道耐药基因的生长与表达,并将微生物平衡向更具潜在危害的物种倾斜。对个体患者而言,这可能增加随后出现更难以治疗的细菌感染的风险。从群体层面看,这类使用会加剧抗生素耐药的更广泛问题。该研究强调了一个直接的信息:面对像 COVID-19 这样的病毒性疾病时,出于“以防万一”而使用抗生素可能带来持久的不利影响,审慎的抗生素管理对于保护这些药物在真正需要时的有效性至关重要。
引用: Glascock, A., Maguire, C., Phan, H.V. et al. Empiric azithromycin alters the upper respiratory microbiome and resistome without anti-inflammatory benefit in COVID-19. Nat Microbiol 11, 1100–1112 (2026). https://doi.org/10.1038/s41564-026-02285-8
关键词: 阿奇霉素, COVID-19, 呼吸道微生物组, 抗生素耐药, 抗生素管理