Clear Sky Science · de
Empirische Azithromycin-Behandlung verändert das obere Atemwegs-Mikrobiom und das Resistom ohne entzündungshemmenden Nutzen bei COVID-19
Warum das für den alltäglichen Einsatz von Antibiotika wichtig ist
In den frühen Monaten der COVID-19-Pandemie erhielten viele Menschen das Antibiikum Azithromycin in der Hoffnung, es könnte schädliche Entzündungen dämpfen oder bei der Bekämpfung des Virus helfen. Diese Studie stellt eine auf den ersten Blick einfache, aber entscheidende Frage: Was hat der erhöhte Antibiotikaeinsatz tatsächlich in den Nasen und Rachen der Patientinnen und Patienten bewirkt, wo sich das Virus zuerst festsetzt? Anhand von mehr als tausend hospitalisierten Erwachsenen zeigen die Forschenden, dass Azithromycin die Gemeinschaft der Mikroben im oberen Atemweg deutlich störte und die Menge an Antibiotika-Resistenzgenen erhöhte — ohne den erhofften entzündungshemmenden Effekt zu liefern.
Wie die Studie aufgebaut war
Die Wissenschaftlerinnen und Wissenschaftler nutzten Daten aus einem landesweiten US-Projekt, das 1.164 Erwachsene verfolgte, die zwischen 2020 und 2021 mit COVID-19 in 20 Krankenhäusern hospitalisiert waren. Die Patienten fielen natürlicherweise in drei Gruppen: diejenigen, die empirisch mit Azithromycin behandelt wurden, diejenigen, die andere Antibiotika erhielten, und diejenigen, die keine Antibiotika bekommen hatten. Aus wiederholt über einen Monat entnommenen Nasenabstrichen nutzte das Team eine Technik namens Metatranskriptomik, um zu erfassen, welche Mikroben aktiv waren und welche Resistenzgene exprimiert wurden. Außerdem sequenzierten sie immunbezogene Gene aus Blut- und Nasenzellen, um zu prüfen, ob Azithromycin die entzündlichen Reaktionen der Patienten veränderte. 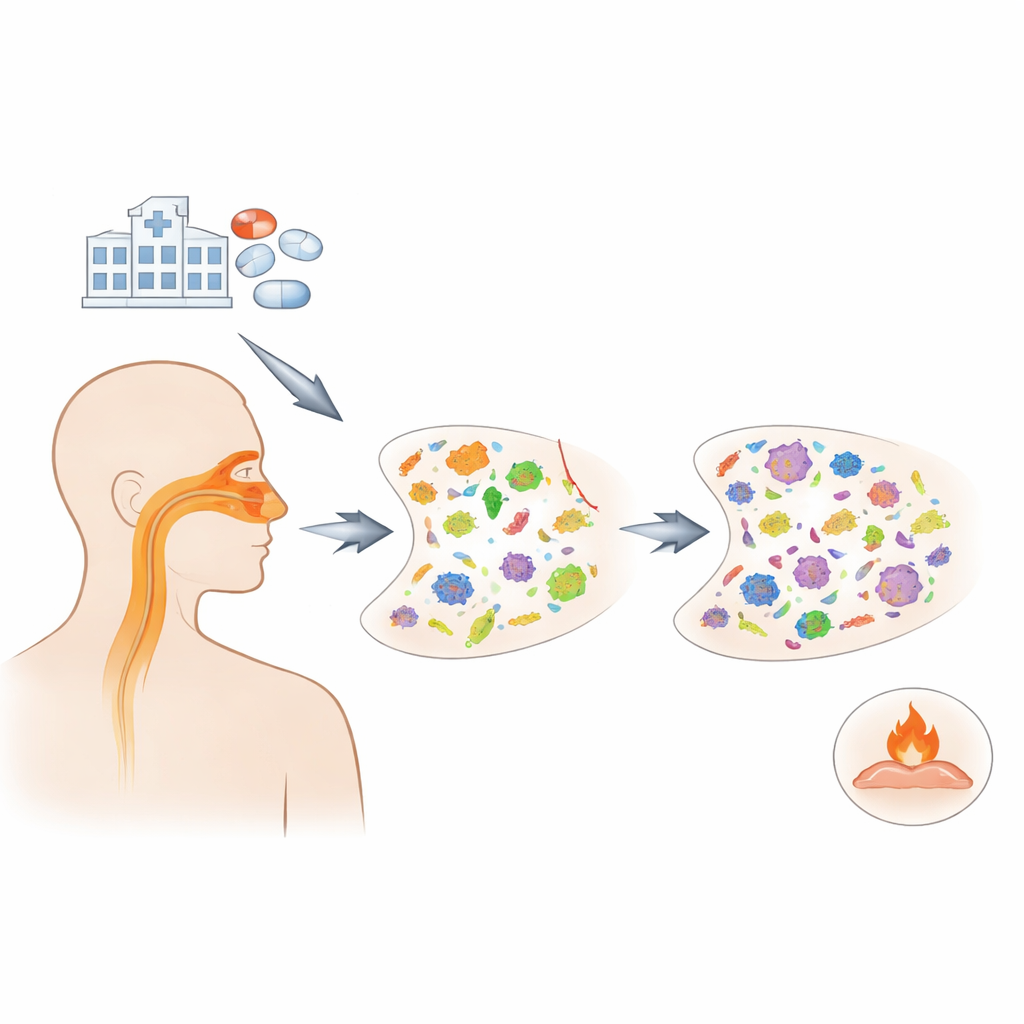
Was mit den kleinen Bewohnern der Atemwege geschah
Bereits einen Tag nach Beginn der Azithromycin-Behandlung sank die Gesamtmenge an Bakterien in der Nase, und diese Reduktion war nach etwa fünf Behandlungstagen weiterhin deutlich. Der Verlust war jedoch nicht gleichmäßig. Mikroben, die normalerweise harmlos im oberen Atemweg leben, wie Neisseria und Fusobacterium, gingen tendenziell zurück. Gleichzeitig wurden Arten, die Krankheiten verursachen können, darunter bestimmte Staphylococcus- und Klebsiella-Stämme, häufiger. Auch Pilze nahmen im selben Zeitraum an Häufigkeit zu, was darauf hindeutet, dass andere Organismen in die frei gewordenen Nischen vordringen können, wenn bakterielle Nachbarn zurückgedrängt werden.
Verborgene Verschiebungen bei Resistenzgenen
Über das bloße Zählen vorhandener Mikroben hinaus konzentrierten sich die Forschenden auf das „Resistom“ — die Gesamtheit der Gene, die Bakterien das Überstehen von Antibiotika ermöglichen. Azithromycin gehört zur Gruppe der Makrolide, und das Team fand, dass Gene, die Resistenzen gegen Makrolide und verwandte Wirkstoffe vermitteln, schnell zunahmen. Nach nur wenigen Tagen Behandlung war die Anzahl unterschiedlicher aktiv exprimierter Makrolid-Resistenzgene bei mit Azithromycin behandelten Patienten etwa 50 bis 70 Prozent höher als bei denen, die keine oder andere Antibiotika erhielten. Der Anteil des gesamten Resistoms, der durch diese Makrolid-Resistenzgene ausgemacht wurde, verdoppelte sich nahezu, und auffallend war, dass diese Veränderungen noch eine Woche oder länger nach Absetzen des Antibiotikums anhielten. 
Welche Mikroben die neuen Abwehrmechanismen tragen
Durch die Korrelation von Resistenzgenen mit den vorhandenen Bakterien verband die Studie diese Makrolid-Abwehrwerkzeuge sowohl mit bekannten Problemkeimen als auch mit normalerweise harmlosen Mitbewohnern. Potenzielle Krankheitserreger wie Staphylococcus und Streptococcus standen in starker Beziehung zu Schlüsselmolekülen der Resistenz wie ermA und msrA, was nahelegt, dass gängige für Pneumonien verantwortliche Bakterien nach Azithromycin-Exposition schwerer zu behandeln sein könnten. Zugleich zeigten alltägliche Nasenbewohner, darunter Corynebacterium und Dolosigranulum, ebenfalls Verbindungen zu Resistenzgenen, was darauf hindeutet, dass der obere Atemweg als stilles Reservoir dienen kann, in dem sich Antibiotikaresistenzen anhäufen und potenziell verbreiten.
Kein Hinweis auf den erhofften dämpfenden Effekt
Azithromycin hat den Ruf, Entzündungen bei chronischen Lungenerkrankungen zu dämpfen, sodass viele Kliniker hofften, es könnte die übermäßigen Immunreaktionen bei schwerer COVID-19 abschwächen. Als die Forschenden jedoch Muster der Immun-Genaktivität im Blut und in Nasenzellen von Patientengruppen mit und ohne Azithromycin verglichen, fanden sie keine bedeutsamen Unterschiede. Auch die Viruslast von SARS-CoV-2 in der Nase war in den Gruppen ähnlich. Mit anderen Worten: Während das Medikament eindeutig das Mikrobiom und das Resistom veränderte, schien es nicht die schädliche Entzündung zu lindern oder die Menge an Virus bei hospitalisierten Patienten zu verringern.
Was das für Patienten und die öffentliche Gesundheit bedeutet
Zusammen ergeben diese Befunde ein warnendes Bild. In dieser großen Kohorte von mit einem Virus infizierten, hospitalisierten Menschen brachte der empirische Einsatz von Azithromycin keinen messbaren entzündungshemmenden oder antiviralen Nutzen, förderte jedoch die Vermehrung und Aktivität von Resistenzgenen im oberen Atemweg und verschob das Mikrobiom zugunsten potenziell schädlicherer Arten. Für einzelne Patientinnen und Patienten kann das das Risiko späterer bakterieller Infektionen erhöhen, die schwerer zu behandeln sind. Auf Bevölkerungsebene trägt ein solcher Einsatz zudem zur übergreifenden Problematik der Antibiotikaresistenz bei. Die Arbeit betont eine einfache Botschaft für Kliniker und die Öffentlichkeit: Bei viralen Erkrankungen wie COVID-19 kann die prophylaktische Gabe von Antibiotika langfristige Nachteile haben, und ein sorgfältiges Antibiotika-Management ist essenziell, um die Wirksamkeit dieser Medikamente für die Fälle zu bewahren, in denen sie wirklich nötig sind.
Zitation: Glascock, A., Maguire, C., Phan, H.V. et al. Empiric azithromycin alters the upper respiratory microbiome and resistome without anti-inflammatory benefit in COVID-19. Nat Microbiol 11, 1100–1112 (2026). https://doi.org/10.1038/s41564-026-02285-8
Schlüsselwörter: Azithromycin, COVID-19, Atemwegs-Mikrobiom, antibiotische Resistenz, Antibiotika-Management