Clear Sky Science · fr
L’azithromycine empirique modifie le microbiome et le réservoir de résistance des voies respiratoires supérieures sans bénéfice anti‑inflammatoire dans la COVID‑19
Pourquoi cela importe pour l’usage courant des antibiotiques
Pendant les premiers mois de la pandémie de COVID‑19, beaucoup de personnes ont reçu l’antibiotique azithromycine dans l’espoir qu’il calme une inflammation nocive ou aide à combattre le virus. Cette étude pose une question apparemment simple mais cruciale : qu’a réellement provoqué cette surutilisation d’antibiotiques dans le nez et la gorge des patients, où le virus s’installe en premier lieu ? En suivant plus d’un millier d’adultes hospitalisés, les chercheurs montrent que l’azithromycine perturbe nettement la communauté microbienne des voies aériennes supérieures et favorise les gènes de résistance aux antibiotiques — sans apporter le bénéfice anti‑inflammatoire escompté.
Comment l’étude a été organisée
Les scientifiques se sont appuyés sur un projet national aux États‑Unis qui a suivi 1 164 adultes hospitalisés pour COVID‑19 dans 20 hôpitaux entre 2020 et 2021. Les patients se sont naturellement répartis en trois groupes : ceux traités empiriquement par azithromycine, ceux ayant reçu d’autres antibiotiques et ceux n’ayant reçu aucun antibiotique. À partir d’écouvillonnages nasaux répétés sur un mois, l’équipe a utilisé une technique appelée métatranscriptomique pour identifier quels microbes étaient actifs et quels gènes de résistance étaient exprimés. Ils ont aussi séquencé des gènes liés à l’immunité à partir de sang et de cellules nasales pour déterminer si l’azithromycine modifiait la réponse inflammatoire des patients. 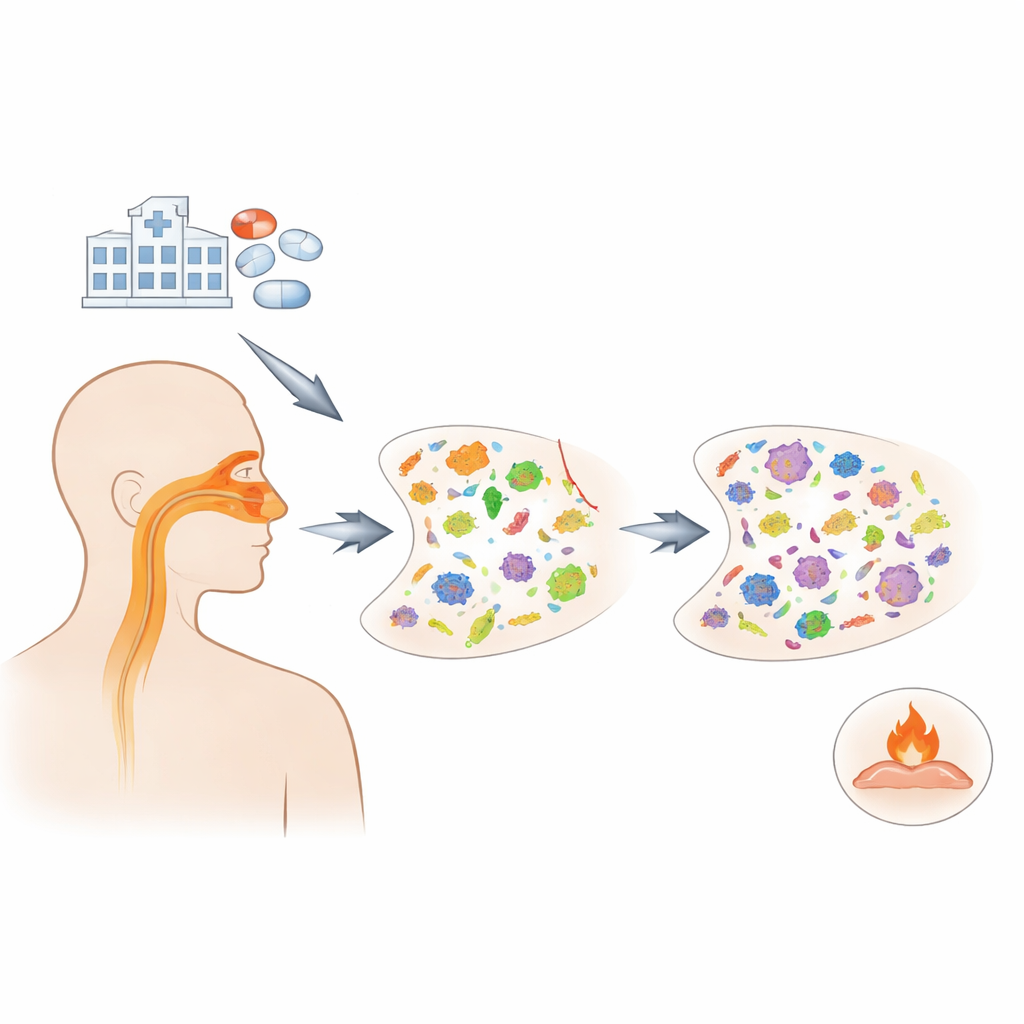
Ce qui est arrivé aux minuscules habitants des voies aériennes
Dès le premier jour suivant le début de l’azithromycine, la quantité globale de bactéries dans le nez a chuté, et cette réduction restait visible après environ cinq jours de traitement. Mais la perte n’était pas uniforme. Les microbes qui vivent normalement sans danger dans les voies aériennes supérieures, comme Neisseria et Fusobacterium, ont tendance à décliner. En revanche, des espèces potentiellement pathogènes, dont certains Staphylococcus et Klebsiella, sont devenues plus communes. Les champignons ont aussi gagné en abondance sur la même période, suggérant que lorsque les voisins bactériens sont réduits, d’autres organismes peuvent occuper la niche libérée.
Des déplacements cachés des gènes de résistance
Au‑delà du décompte des microbes présents, les chercheurs se sont concentrés sur le « réservoir de résistance » — l’ensemble des gènes permettant aux bactéries de résister aux antibiotiques. L’azithromycine appartient à une famille de médicaments appelés macrolides, et l’équipe a constaté que les gènes conférant une résistance aux macrolides et aux médicaments proches se sont rapidement amplifiés. Après seulement quelques jours de traitement, le nombre de gènes distincts de résistance aux macrolides activement exprimés était d’environ 50 à 70 % plus élevé chez les patients traités par azithromycine que chez ceux n’ayant reçu aucun antibiotique ou d’autres antibiotiques. La part du réservoir global constituée par ces gènes de résistance aux macrolides a presque doublé et, de manière frappante, ces changements ont perduré une semaine ou plus après l’arrêt de l’antibiotique. 
Quels microbes portent les nouvelles défenses
En corrélant les gènes de résistance avec les bactéries présentes, l’étude a lié ces mécanismes de défense contre les macrolides à la fois à des agents pathogènes connus et à des commensaux généralement inoffensifs. Des agents pathogènes potentiels comme Staphylococcus et Streptococcus étaient fortement associés à des gènes clés de résistance tels que ermA et msrA, ce qui implique que des bactéries responsables de pneumonies courantes pourraient devenir plus difficiles à traiter après une exposition à l’azithromycine. En même temps, des habitants ordinaires du nez, y compris Corynebacterium et Dolosigranulum, montraient également des liens avec des gènes de résistance, suggérant que les voies aériennes supérieures peuvent servir de réservoir discret où la résistance aux antibiotiques s’accumule et peut potentiellement se propager.
Aucun signe de l’effet apaisant espéré
L’azithromycine a la réputation d’atténuer l’inflammation dans les maladies pulmonaires chroniques, si bien que beaucoup de cliniciens espéraient qu’elle pourrait réduire les réponses immunitaires excessives observées dans les formes sévères de la COVID‑19. Pourtant, quand les chercheurs ont comparé les profils d’expression des gènes immunitaires dans le sang et les cellules nasales des patients ayant ou non reçu de l’azithromycine, ils n’ont trouvé aucune différence notable. Les niveaux viraux de SARS‑CoV‑2 dans le nez semblaient également similaires entre les groupes. Autrement dit, si le médicament a clairement remodelé le microbiome et le réservoir de résistance, il n’a pas semblé diminuer l’inflammation nocive ni réduire la quantité de virus chez les patients hospitalisés.
Ce que cela signifie pour les patients et la santé publique
Ces résultats dressent ensemble un tableau prudent. Dans cette vaste cohorte de personnes hospitalisées pour une infection virale, l’utilisation empirique d’azithromycine n’a pas apporté d’avantages anti‑inflammatoires ou antiviraux mesurables, mais elle a favorisé la croissance et l’activité des gènes de résistance dans les voies respiratoires supérieures et a déplacé l’équilibre microbien vers des espèces potentiellement plus nocives. Pour un patient individuel, cela peut augmenter le risque d’infections bactériennes ultérieures plus difficiles à traiter. À l’échelle de la population, un tel usage alimente le problème plus large de la résistance aux antibiotiques. Le travail souligne un message simple pour cliniciens et grand public : face à des maladies virales comme la COVID‑19, l’usage d’antibiotiques « au cas où » peut avoir des conséquences durables, et une gestion prudente est essentielle pour préserver l’efficacité de ces médicaments lorsque leur emploi est réellement nécessaire.
Citation: Glascock, A., Maguire, C., Phan, H.V. et al. Empiric azithromycin alters the upper respiratory microbiome and resistome without anti-inflammatory benefit in COVID-19. Nat Microbiol 11, 1100–1112 (2026). https://doi.org/10.1038/s41564-026-02285-8
Mots-clés: azithromycine, COVID-19, microbiome respiratoire, résistance aux antibiotiques, stewardship des antibiotiques