Clear Sky Science · pl
Empiryczne stosowanie azytromycyny zmienia mikrobiom i rezystom górnych dróg oddechowych bez korzyści przeciwzapalnych w COVID-19
Dlaczego to ma znaczenie dla codziennego stosowania antybiotyków
W pierwszych miesiącach pandemii COVID-19 wiele osób otrzymywało antybiotyk azytromycynę w nadziei, że złagodzi on szkodliwe zapalenie lub pomoże zwalczyć wirusa. Badanie stawia pozornie proste, lecz kluczowe pytanie: co tak naprawdę zrobiło to dodatkowe stosowanie antybiotyku w nosie i gardle pacjentów, gdzie wirus najpierw się osadza? Śledząc ponad tysiąc hospitalizowanych dorosłych, badacze pokazują, że azytromycyna wyraźnie zaburzyła społeczność drobnoustrojów w górnych drogach oddechowych i zwiększyła liczbę genów oporności na antybiotyki — bez oczekiwanego efektu przeciwzapalnego.
Jak przeprowadzono badanie
Naukowcy oparli się na ogólnokrajowym projekcie w USA, który śledził 1 164 dorosłych hospitalizowanych z powodu COVID-19 w 20 szpitalach między 2020 a 2021 rokiem. Pacjenci naturalnie rozdzielili się na trzy grupy: tych leczonych empirycznie azytromycyną, tych poddanych innym antybiotykom oraz tych, którzy nie otrzymali antybiotyków. Z nosowych wymazów pobieranych wielokrotnie w ciągu miesiąca zespół zastosował technikę metatranskryptomiki, aby odczytać, które mikroby są aktywne i które geny oporności są wyrażane. Sekwencjonowali też geny związane z odpowiedzią immunologiczną z krwi i komórek nosa, by sprawdzić, czy azytromycyna zmienia odpowiedź zapalną pacjentów. 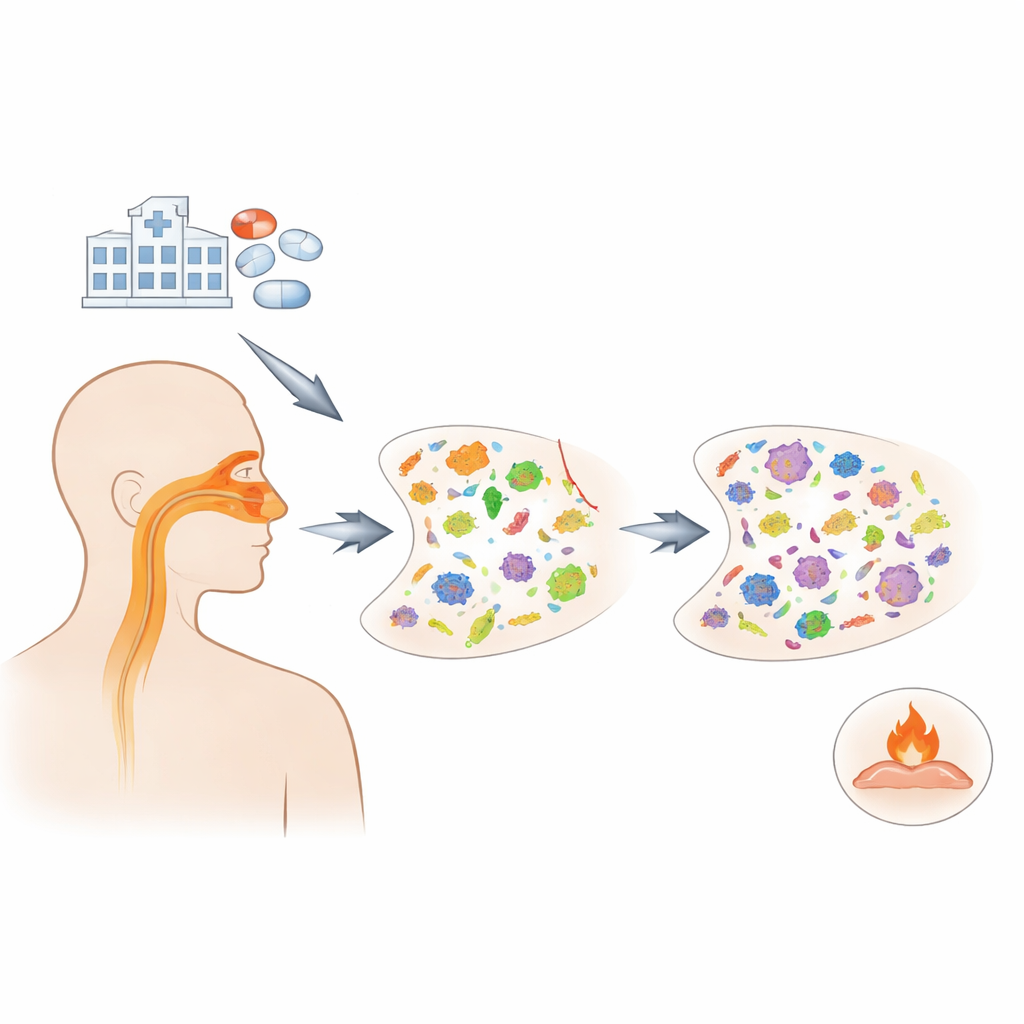
Co się stało z drobnymi mieszkańcami dróg oddechowych
Już dzień po rozpoczęciu terapii azytromycyną całkowita ilość bakterii w nosie spadła, a to obniżenie było nadal widoczne po około pięciu dniach leczenia. Ubytek nie był jednak równomierny. Mikroby, które zwykle bytują w górnych drogach oddechowych bez szkody, takie jak Neisseria i Fusobacterium, miały tendencję do wygaszania. Tymczasem gatunki mogące wywoływać choroby, w tym niektóre Staphylococcus i Klebsiella, stały się bardziej powszechne. Grzyby również zwiększyły swoją obfitość w tym samym okresie, co sugeruje, że gdy bakteryjni sąsiedzi zostają stłumieni, inne organizmy mogą zająć uwolnioną niszę.
Ukryte przesunięcia w genach oporności
Poza liczeniem obecnych drobnoustrojów, badacze skupili się na „rezystomie” — zbiorze genów umożliwiających bakteriom przetrwanie w obecności antybiotyków. Azytromycyna należy do rodziny leków zwanych makrolidami, a zespół stwierdził, że geny nadające oporność na makrolidy i pokrewne leki szybko się rozrosły. Już po kilku dniach leczenia liczba odrębnych genów oporności na makrolidy aktywnie wyrażanych była o około 50–70 procent większa u pacjentów leczonych azytromycyną niż u tych, którzy nie otrzymali antybiotyków lub otrzymali inne leki. Udział tych genów oporności na makrolidy w całej rezystomie niemal się podwoił i, co uderzające, zmiany te utrzymywały się przez tydzień lub dłużej po zakończeniu kuracji. 
Które mikroby niosą nowe mechanizmy obronne
Korelacja genów oporności z obecnymi bakteriami pozwoliła powiązać te makrolidowe „narzędzia obronne” zarówno ze znanymi sprawcami chorób, jak i z zwykle nieszkodliwymi współlokatorami. Potencjalni patogeny, jak Staphylococcus i Streptococcus, wykazywały silne powiązania z kluczowymi genami oporności, takimi jak ermA i msrA, co sugeruje, że zwykłe bakterie wywołujące zapalenie płuc mogą stać się trudniejsze w leczeniu po ekspozycji na azytromycynę. Jednocześnie codzienni mieszkańcy nosa, w tym Corynebacterium i Dolosigranulum, także wykazywali związki z genami oporności, co sugeruje, że górne drogi oddechowe mogą służyć jako ciche rezerwuarium, w którym gromadzi się i potencjalnie rozprzestrzenia oporność na antybiotyki.
Brak oznak oczekiwanego efektu uspokajającego zapalenie
Azytromycyna ma reputację środka tłumiącego zapalenie w przewlekłych chorobach płuc, dlatego wielu klinicystów miało nadzieję, że złagodzi ona nadmierne reakcje immunologiczne obserwowane w ciężkim COVID-19. Jednak gdy badacze porównali wzorce aktywności genów immunologicznych w krwi i komórkach nosa u pacjentów, którzy otrzymali azytromycynę i tych, którzy jej nie otrzymali, nie stwierdzili istotnych różnic. Poziomy wirusa SARS-CoV-2 w nosie także wyglądały podobnie w poszczególnych grupach. Innymi słowy, podczas gdy lek wyraźnie przekształcił mikrobiom i rezystom, nie wydawał się łagodzić szkodliwego zapalenia ani zmniejszać ilości wirusa u hospitalizowanych pacjentów.
Co to oznacza dla pacjentów i zdrowia publicznego
W świetle tych wyników wyłania się ostrzegający obraz. W tej dużej kohorcie osób hospitalizowanych z infekcją wirusową empiryczne stosowanie azytromycyny nie przyniosło mierzalnych korzyści przeciwzapalnych ani przeciwwirusowych, ale sprzyjało wzrostowi i aktywności genów oporności w górnych drogach oddechowych oraz przesunęło równowagę drobnoustrojów w stronę bardziej potencjalnie szkodliwych gatunków. Dla pojedynczych pacjentów może to zwiększać ryzyko późniejszych zakażeń bakteryjnych trudniejszych do leczenia. Na poziomie populacyjnym takie stosowanie dokłada się do szerszego problemu oporności na antybiotyki. Praca podkreśla prosty komunikat dla klinicystów i społeczeństwa: w przypadku chorób wirusowych, takich jak COVID-19, stosowanie antybiotyków „na wszelki wypadek” może mieć długotrwałe negatywne skutki, dlatego odpowiedzialne gospodarowanie antybiotykami jest niezbędne, by chronić ich skuteczność na przyszłość, gdy będą naprawdę potrzebne.
Cytowanie: Glascock, A., Maguire, C., Phan, H.V. et al. Empiric azithromycin alters the upper respiratory microbiome and resistome without anti-inflammatory benefit in COVID-19. Nat Microbiol 11, 1100–1112 (2026). https://doi.org/10.1038/s41564-026-02285-8
Słowa kluczowe: azytromycyna, COVID-19, mikrobiom dróg oddechowych, oporność na antybiotyki, nadzór nad stosowaniem antybiotyków