Clear Sky Science · zh
与癌症相关的成纤维细胞通过NDRG1介导的R-环处理调节胰腺癌中的DNA修复
为何肿瘤周围环境很重要
胰腺癌因难以治疗而著称,部分原因在于肿瘤被坚硬、纤维化的支持细胞和蛋白质包围。这项研究揭示了那种疤痕样组织不仅仅阻挡药物进入——它还能主动帮助癌细胞修复化疗造成的DNA损伤,使肿瘤得以存活并复发。理解这一隐蔽的保护机制为提高治疗效果提供了新的思路。
在恶劣环境中生长的强悍癌症
胰腺导管腺癌在营养匮乏、充满称为间质的结缔组织的环境中生长。大量间质由与癌症相关的成纤维细胞(CAFs)产生,它们分泌大量细胞外基质蛋白,如胶原和层粘连蛋白。临床上长期知道富含间质的肿瘤对化疗耐受,但具体原因尚不清楚。研究者提出疑问:这些成纤维细胞及其基质发出的信号是否直接改变了癌细胞对损伤DNA药物的反应。
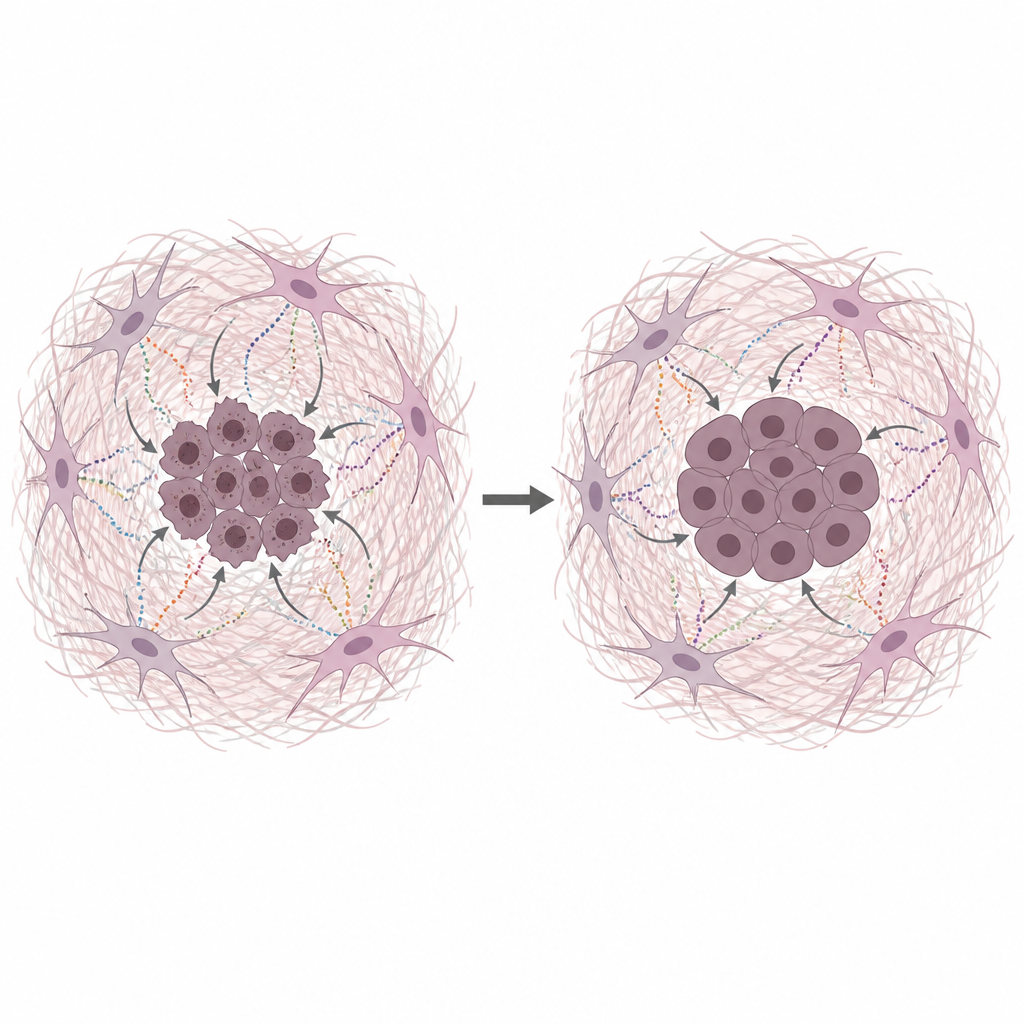
成纤维细胞分泌物为癌细胞DNA提供屏障
研究团队将人类胰腺癌细胞与来自饥饿状态下CAFs的培养基混合培养,该培养基模拟真实肿瘤中的营养匮乏条件。该条件培养基使癌细胞既增殖更多,又更能抵御多种通过损伤DNA或阻滞复制发挥作用的常见化疗药物。对DNA损伤的直接检测显示,在存在CAFs来源培养基或纯化基质蛋白时,DNA断裂更少。胶原、纤连蛋白和层粘连蛋白各自都能减少DNA损伤,表明基质本身——而不仅仅是微量营养物——是关键的保护因素。
一个压力感应器将基质信号与DNA修复连接起来
为弄清基质信号如何在癌细胞内部被转译,作者筛查了数百种蛋白。一种应激响应蛋白NDRG1脱颖而出,尤其是在其被激活(磷酸化)形式下。基质蛋白和CAFs条件培养基通过细胞表面的粘附受体整合素及细胞内的一系列信号蛋白增强了NDRG1的活性。阻断这条信号通路,尤其是名为SGK的激酶家族,会阻止NDRG1被激活。在患者和小鼠模型的肿瘤样本中,高表达的NDRG1主要出现在纤维化间质附近,并与肿瘤生长更快、细胞分裂增多以及化疗后生存率更差相关联。
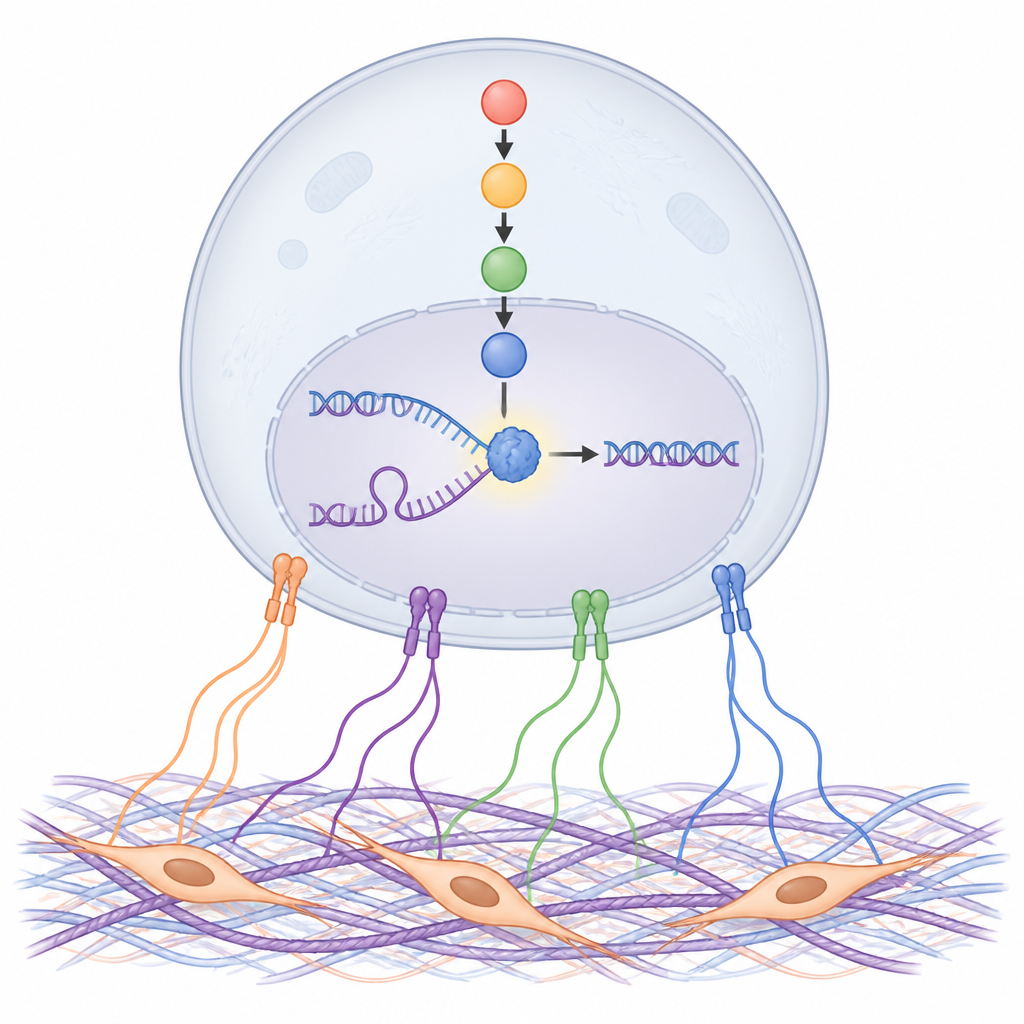
NDRG1保持DNA复制的正轨
研究进一步聚焦NDRG1对DNA的具体作用。使用敏感方法标记并拉出新复制的DNA,研究者发现NDRG1直接定位于DNA复制发生处,尤其是在复制叉被药物阻滞时。去除NDRG1或阻断其被SGK激活会减慢DNA复制,使阻滞的复制叉难以重新启动并增加DNA损伤,无论在培养皿内还是在小鼠体内均是如此。NDRG1中位于194位的组氨酸这一特定残基对其保护作用至关重要,这提示NDRG1的构象及其可能的类酶活性对于稳定复制叉至关重要。
清除有害的RNA–DNA纠结
复制受阻的一个常见原因是R-环的形成,即新合成的RNA回粘到DNA模板上形成的小纠结。作者证明,缺失NDRG1或其激活的细胞会积累这些RNA–DNA杂合物,并遭遇更多复制机器与转录机器之间的碰撞。当他们加入一种专门去除R-环的酶时,复制叉的移动和DNA损伤都回到接近正常的水平。这表明NDRG1通过限制R-环、减轻转录–复制冲突来维持复制过程的顺畅。
这对未来治疗意味着什么
简言之,包绕胰腺肿瘤的纤维组织发出信号,在癌细胞内部开启NDRG1,使它们能够修补化疗引起的DNA损伤并继续分裂。肿瘤中NDRG1表达更高的患者在常规损伤DNA的药物治疗下往往预后更差。针对这一基质–NDRG1通路,或将化疗与削弱NDRG1修复功能的药物联合使用,或能在不提高有毒治疗剂量的情况下使癌细胞更易被击败。
引用: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
关键词: 胰腺癌, 肿瘤微环境, DNA修复, 与癌症相关的成纤维细胞, R-环