Clear Sky Science · sv
Fibroblaster kopplade till cancer reglerar DNA-reparation i pankreascancer via NDRG1-medierad R-loop-hantering
Varför tumörens omgivning spelar roll
Pankreascancer är notoriskt svår att behandla, delvis eftersom tumörerna sitter inbäddade i en hård, fibrös miljö av stödjeceller och proteiner. Denna studie visar att den ärrliknande vävnaden gör mer än att bara hindra läkemedel från att tränga in. Den hjälper aktivt cancerceller att reparera det DNA‑skador som orsakas av kemoterapi, vilket låter tumörer överleva och komma tillbaka. Att förstå detta dolda skyddssystem ger nya idéer för att förbättra behandlingar.
En hård tumör i en karg miljö
Pankreasductalt adenokarcinom växer i en näringsfattig miljö fylld av bindväv som kallas stroma. Mycket av denna stroma bildas av cancerassocierade fibroblaster, eller CAFs, som utsöndrar stora mängder extracellulära matrixproteiner som kollagen och laminin. Läkare har länge vetat att stroma‑rika tumörer är motståndskraftiga mot kemoterapi, men de exakta orsakerna har varit oklara. Forskarna undrade om signaler från dessa fibroblaster och deras matrix direkt förändrar hur cancerceller svarar på DNA‑skadande läkemedel.
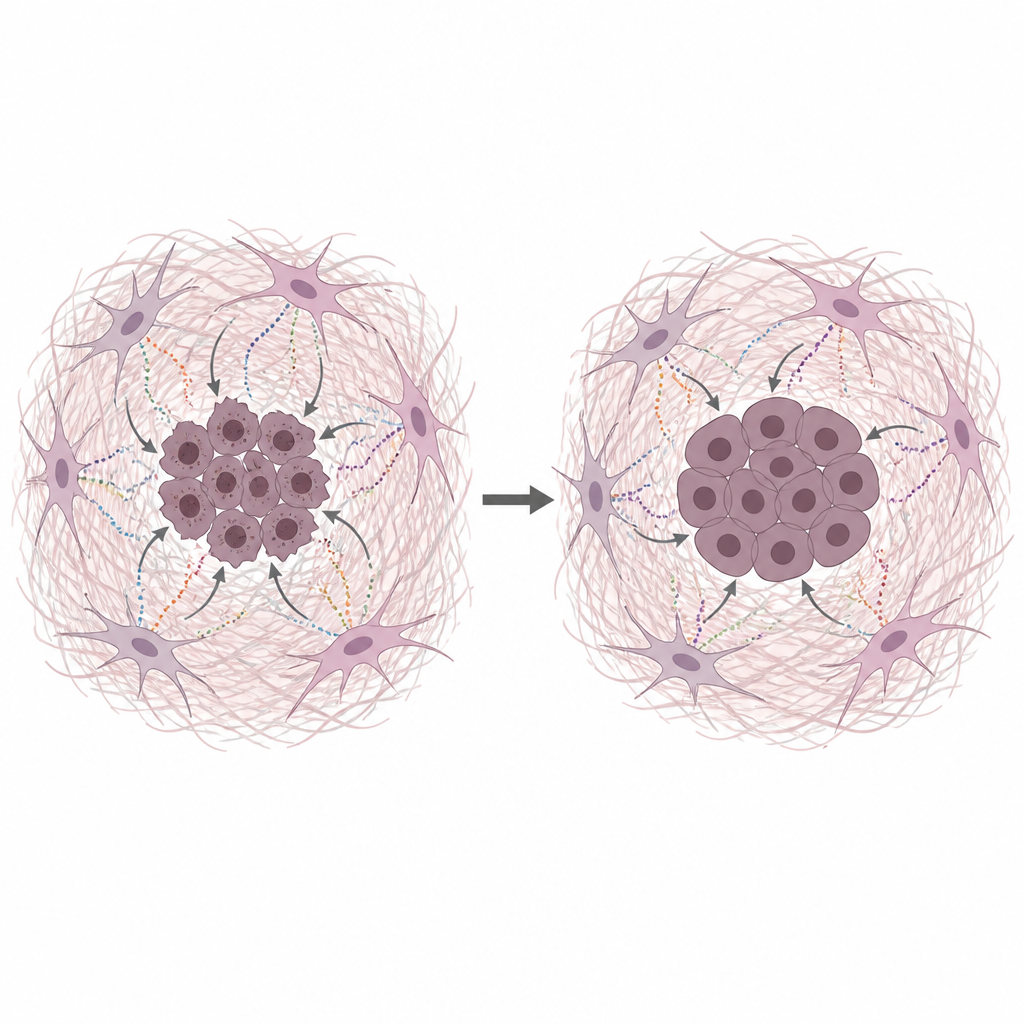
Fibroblast‑sekret skyddar cancerns DNA
Teamet odlade humana pankreascellinjer tillsammans med medium taget från svältade CAFs, vilket efterliknar de näringsfattiga förhållandena i verkliga tumörer. Detta betingade medium fick cancercellerna att både växa mer och stå emot flera vanliga cytostatika som verkar genom att skada DNA eller stoppa dess kopiering. Direkta tester av DNA‑skador visade färre brott när CAF‑deriverat medium eller renade matrixproteiner fanns närvarande. Kollagen, fibronectin och laminin minskade alla DNA‑skador, vilket pekar på matrixen i sig — inte bara små näringsämnen — som en viktig skyddsfaktor.
En stressensor kopplar matrix till DNA‑reparation
För att ta reda på hur matrixsignaler översätts inne i cancercellerna undersökte författarna hundratals proteiner. Ett protein stack ut: ett stressresponssprotein kallat NDRG1, särskilt i sin aktiverade, fosforylerade form. Matrixproteiner och CAF‑betingat medium ökade NDRG1‑aktiviteten via cell‑ytintegriner och en kaskad av signalproteiner inuti cellen. Att blockera denna kaskad, särskilt en kinasfamilj kallad SGK, förhindrade NDRG1‑aktivering. I tumörprover från patienter och i musemodeller var höga NDRG1‑nivåer mest framträdande nära fibrös stroma och kopplades till snabbare tumörtillväxt, högre celldelning och sämre överlevnad efter kemoterapi.
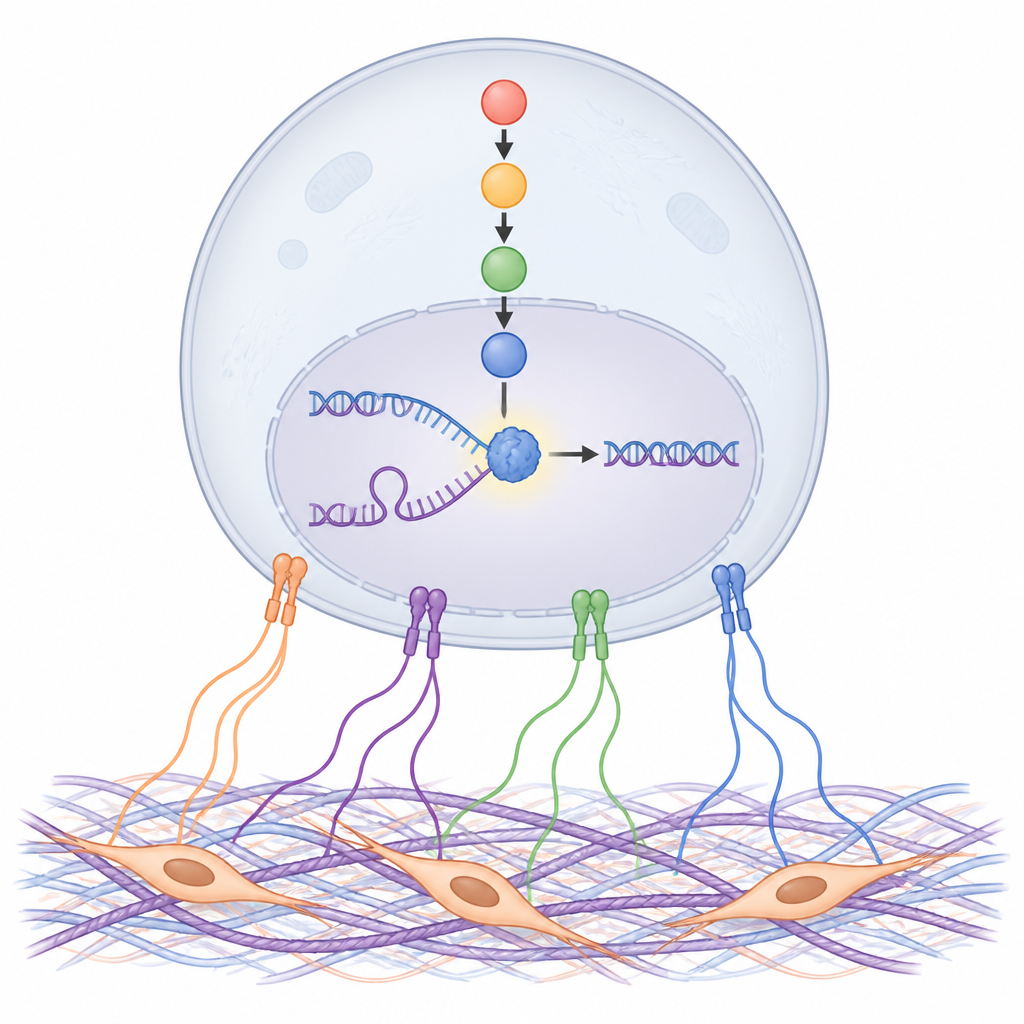
NDRG1 håller DNA‑kopieringen på spåret
Studien zoomade sedan in på vad NDRG1 faktiskt gör med DNA. Med känsliga metoder för att märka och dra ut nysyntetiserat DNA fann forskarna NDRG1 direkt vid de platser där DNA replikeras, särskilt när replikeringsgafflar stannade upp på grund av läkemedel. Att ta bort NDRG1, eller blockera dess aktivering via SGK, försenade DNA‑kopieringen, gjorde det svårare för stoppade gafflar att starta om och ökade DNA‑skador, både i odlingar och i möss. En specifik byggsten i NDRG1, aminosyran histidin vid position 194, visade sig vara avgörande för denna skyddande funktion, vilket tyder på att NDRG1:s form och möjliga enzymlika aktivitet är kritiska för att stabilisera replikeringsgafflar.
Rensning av skadliga RNA–DNA‑knutar
En vanlig orsak till stopp i DNA‑kopieringen är bildandet av R‑loopar, små knutar där nyproducerat RNA fäster tillbaka på DNA‑mallen. Författarna visade att celler utan NDRG1 eller utan dess aktivering ackumulerar dessa RNA–DNA‑hybrider och drabbas av fler kollisioner mellan maskinerna som kopierar DNA och de som transkriberar gener. När de tillsatte ett enzym som specifikt tar bort R‑loopar återgick gaffelrörelse och DNA‑skador mot det normala. Detta indikerar att NDRG1 hjälper till att hålla replikeringsprocessen igång genom att begränsa R‑loopar och mildra konflikter mellan transkription och replikation.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt skickar den fibrösa vävnaden runt pankreastumörer signaler som slår på NDRG1 inne i cancercellerna, vilket gör att de kan laga kemoterapi‑inducerade DNA‑skador och fortsätta dela sig. Patienter vars tumörer uttrycker mer NDRG1 tenderar att få sämre utfall på standardbehandlingar med DNA‑skadande läkemedel. Att rikta in sig på denna matrix–NDRG1‑väg, eller kombinera kemoterapi med läkemedel som försvagar NDRG1:s reparationsfunktion, skulle kunna göra cancerceller mer sårbara utan att öka dosen av toxiska behandlingar.
Citering: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Nyckelord: pankreascancer, tumörmikromiljö, DNA-reparation, cancerassocierade fibroblaster, R-loopar