Clear Sky Science · fr
Les fibroblastes associés au cancer régulent la réparation de l’ADN dans le cancer du pancréas via le traitement des R-loops médié par NDRG1
Pourquoi le voisinage de la tumeur compte
Le cancer du pancréas est notoirement difficile à traiter, en partie parce que les tumeurs se développent dans un environnement résistant et fibreux composé de cellules de soutien et de protéines. Cette étude révèle que ce tissu cicatriciel fait plus que simplement empêcher les médicaments de pénétrer : il aide activement les cellules cancéreuses à réparer les dommages à l’ADN causés par la chimiothérapie, ce qui permet aux tumeurs de survivre et de réapparaître. Comprendre ce système de protection caché ouvre de nouvelles pistes pour améliorer l’efficacité des traitements.
Un cancer tenace dans un environnement hostile
L’adénocarcinome canalaire du pancréas se développe dans un milieu pauvre en nutriments, encombré de tissu conjonctif appelé stroma. Une grande partie de ce stroma est produite par des fibroblastes associés au cancer (CAF), qui sécrètent de grandes quantités de protéines de matrice extracellulaire comme le collagène et la laminine. Les cliniciens savent depuis longtemps que les tumeurs riches en stroma résistent à la chimiothérapie, mais les raisons précises restaient floues. Les chercheurs se sont demandé si les signaux émis par ces fibroblastes et leur matrice modifiaient directement la réponse des cellules cancéreuses aux médicaments endommageant l’ADN.
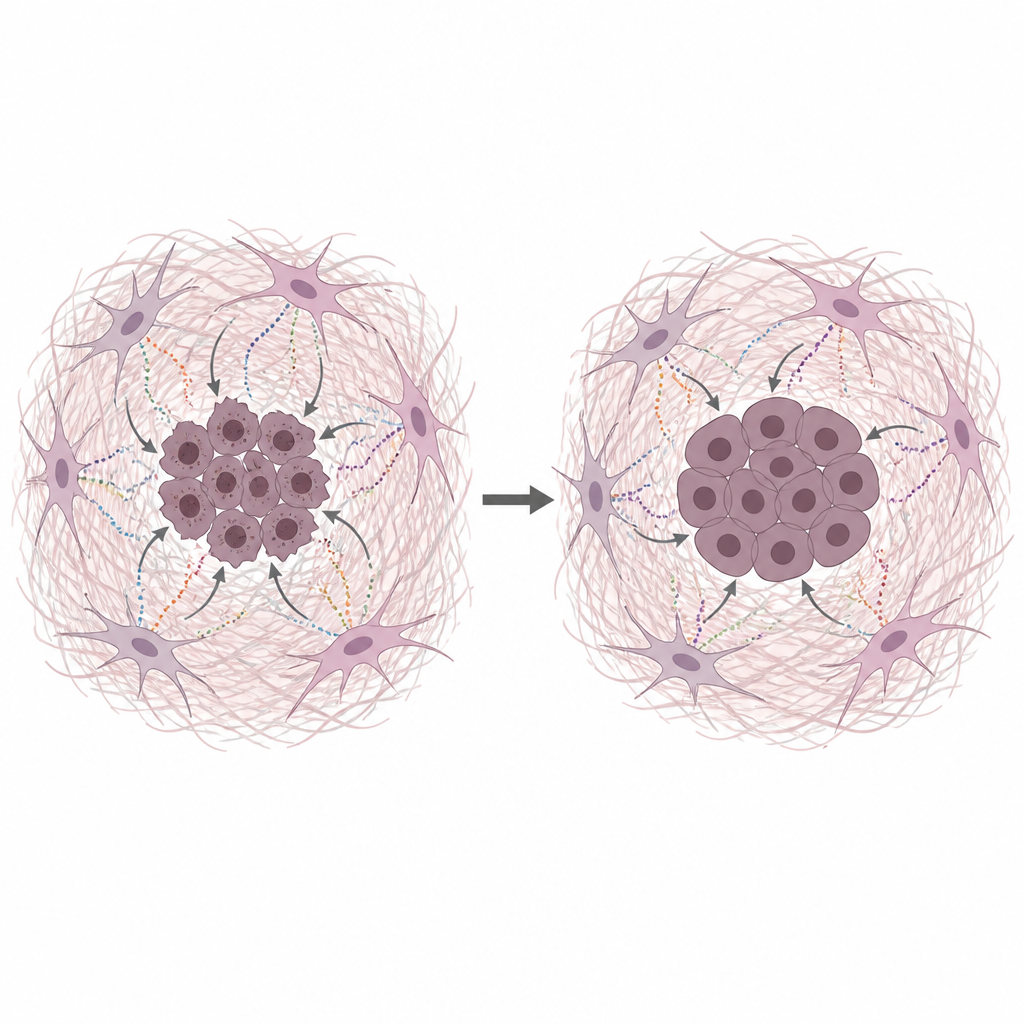
Les sécrétions des fibroblastes protègent l’ADN cancéreux
L’équipe a cultivé des cellules cancéreuses pancréatiques humaines en présence de milieu conditionné provenant de CAF affamés, ce qui reproduit les conditions pauvres en nutriments des vraies tumeurs. Ce milieu conditionné a rendu les cellules cancéreuses plus proliférantes et plus résistantes à plusieurs chimiothérapies courantes qui agissent en endommageant l’ADN ou en bloquant sa copie. Des tests directs des lésions de l’ADN ont montré moins de cassures lorsque le milieu dérivé des CAF ou des protéines de matrice purifiées étaient présents. Le collagène, la fibronectine et la laminine ont chacun réduit les dommages à l’ADN, ce qui indique que la matrice elle‑même, et pas seulement de petits nutriments, joue un rôle protecteur clé.
Un capteur de stress relie la matrice à la réparation de l’ADN
Pour comprendre comment les signaux de la matrice sont traduits à l’intérieur des cellules cancéreuses, les auteurs ont passé en revue des centaines de protéines. Une a émergé : une protéine de réponse au stress appelée NDRG1, particulièrement dans sa forme activée, phosphorylée. Les protéines de matrice et le milieu conditionné des CAF ont renforcé l’activité de NDRG1 via des récepteurs d’adhésion à la surface cellulaire appelés intégrines et une cascade de signaux intracellulaires. Bloquer cette cascade, en particulier une famille de kinases nommée SGK, empêchait l’activation de NDRG1. Dans des échantillons tumoraux de patients et dans des modèles murins, des niveaux élevés de NDRG1 étaient surtout visibles près du stroma fibreux et étaient associés à une croissance tumorale plus rapide, à une division cellulaire accrue et à une survie moindre après chimiothérapie.
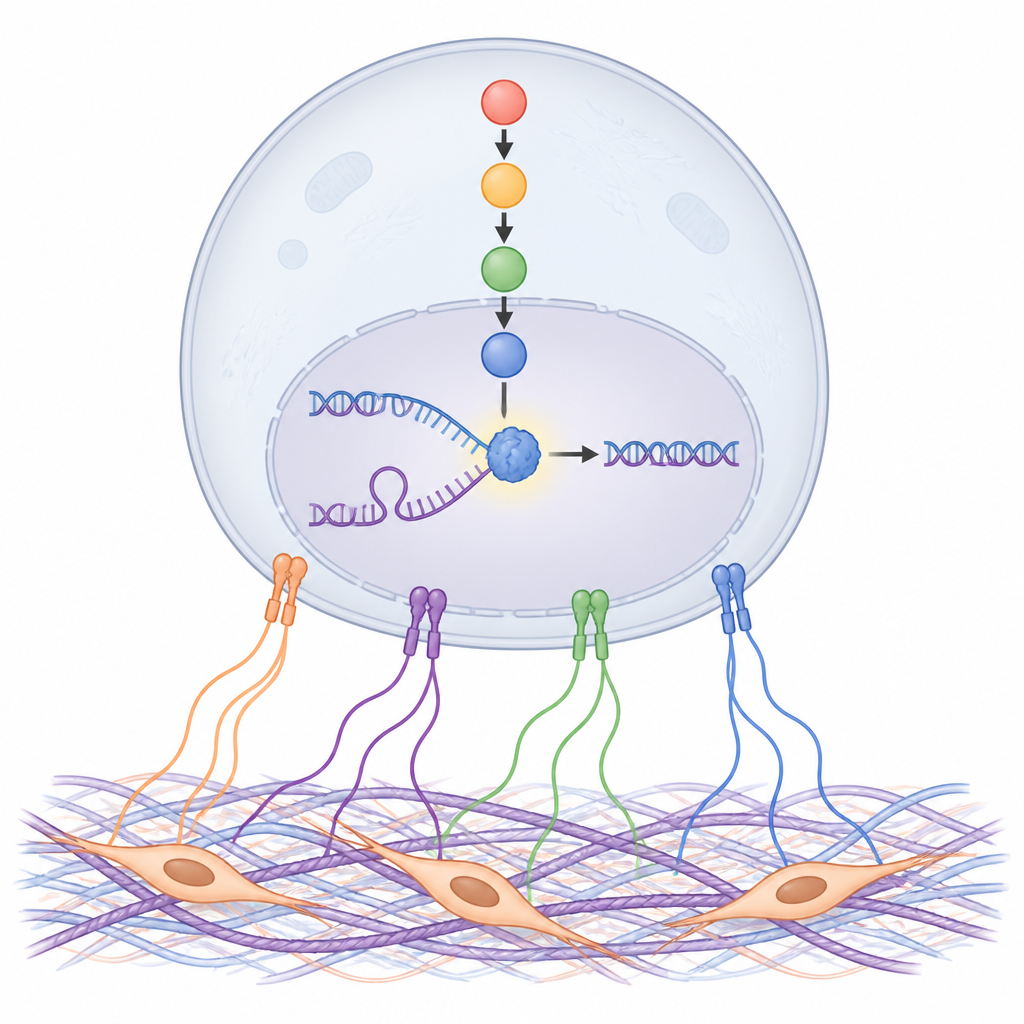
NDRG1 maintient la copie de l’ADN sur la bonne voie
L’étude s’est ensuite intéressée à ce que NDRG1 fait réellement sur l’ADN. En utilisant des méthodes sensibles pour marquer et isoler l’ADN nouvellement répliqué, les chercheurs ont trouvé NDRG1 directement aux sites de réplication, en particulier lorsque les fourches de réplication sont bloquées par des médicaments. Supprimer NDRG1, ou inhiber son activation par SGK, ralentissait la réplication de l’ADN, rendait plus difficile le redémarrage des fourches bloquées et augmentait les dommages à l’ADN, en culture comme chez la souris. Un acide aminé précis de NDRG1, l’histidine en position 194, s’est avéré essentiel pour ce rôle protecteur, suggérant que la conformation de NDRG1 et sa possible activité de type enzymatique sont critiques pour stabiliser les fourches de réplication.
Éliminer les nœuds nocifs ARN–ADN
Une cause fréquente d’interruption de la réplication est la formation de R‑loops, de petits nœuds où l’ARN nouvellement synthétisé se réassocie à la matrice d’ADN. Les auteurs ont montré que les cellules privées de NDRG1 ou de son activation accumulent ces hybrides ARN–ADN et subissent davantage de collisions entre les machines de réplication et les complexes de transcription. Lorsqu’ils ont ajouté une enzyme qui élimine spécifiquement les R‑loops, la progression des fourches et les dommages à l’ADN revenaient vers la normale. Cela indique que NDRG1 aide à maintenir une réplication fluide en limitant les R‑loops et en atténuant ces conflits transcription‑réplication.
Ce que cela signifie pour les traitements futurs
En termes simples, le tissu fibreux entourant les tumeurs pancréatiques envoie des signaux qui activent NDRG1 dans les cellules cancéreuses, leur permettant de réparer les dommages à l’ADN induits par la chimiothérapie et de continuer à se diviser. Les patients dont les tumeurs expriment davantage NDRG1 ont tendance à obtenir de moins bons résultats avec les traitements traditionnels qui endommagent l’ADN. Cibler cette voie matrice–NDRG1, ou combiner la chimiothérapie avec des médicaments qui affaiblissent la fonction réparatrice de NDRG1, pourrait rendre les cellules cancéreuses plus vulnérables sans augmenter la dose de traitements toxiques.
Citation: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Mots-clés: cancer du pancréas, microenvironnement tumoral, réparation de l’ADN, fibroblastes associés au cancer, R-loops