Clear Sky Science · pl
Fibroblasty związane z rakiem regulują naprawę DNA w raku trzustki poprzez przetwarzanie R-pętli zależne od NDRG1
Dlaczego otoczenie guza ma znaczenie
Rak trzustki jest niezwykle trudny do leczenia, częściowo dlatego, że guzy rozwijają się w twardym, włóknistym otoczeniu komórek podporowych i białek. Badanie ujawnia, że ta bliznowata tkanka robi znacznie więcej niż tylko blokuje wnikanie leków. Aktywnie pomaga komórkom nowotworowym naprawiać uszkodzenia DNA spowodowane chemioterapią, co pozwala guzom przetrwać i odrastać. Zrozumienie tego ukrytego systemu ochronnego otwiera nowe pomysły na zwiększenie skuteczności terapii.
Trudny nowotwór w surowym środowisku
Gruczolakorak przewodowy trzustki rozwija się w ubogim w składniki odżywcze środowisku wypełnionym tkanką łączną zwaną stromą. Znaczna część tej stromy jest wytwarzana przez fibroblasty związane z rakiem (CAF), które wydzielają duże ilości białek macierzy pozakomórkowej, takich jak kolagen i laminina. Lekarze od dawna wiedzą, że guzy bogate w stromę są oporne na chemioterapię, ale dokładne przyczyny były niejasne. Naukowcy zastanawiali się, czy sygnały od tych fibroblastów i ich macierzy bezpośrednio zmieniają reakcję komórek nowotworowych na leki uszkadzające DNA.
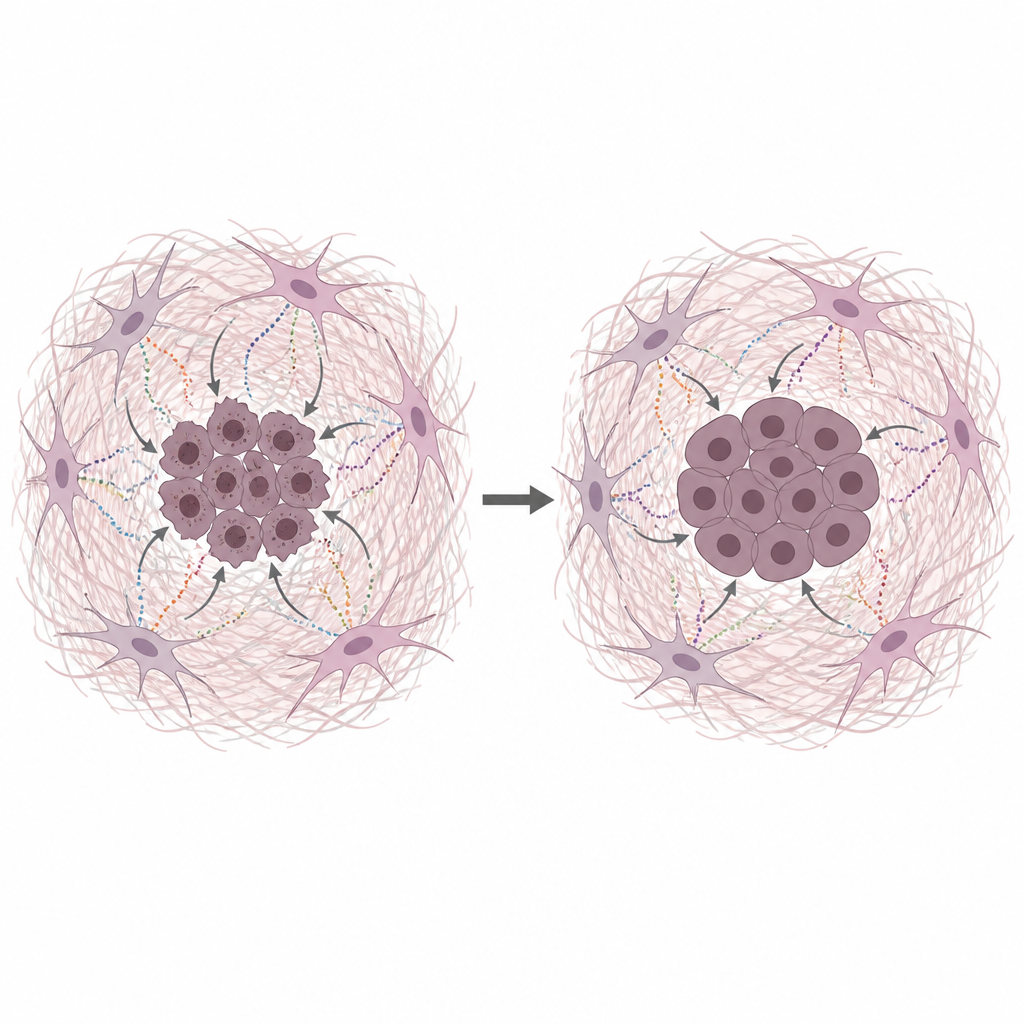
Wydzieliny fibroblastów chronią DNA nowotworu
Zespół hodował ludzkie komórki raka trzustki razem z medium pobranym od głodowanych CAF, co naśladuje ubogie warunki występujące w rzeczywistych guzach. To kondycjonowane medium sprawiło, że komórki nowotworowe szybciej rosły i były odporne na kilka powszechnie stosowanych chemioterapii działających przez uszkadzanie DNA lub blokowanie jego replikacji. Testy bezpośrednio mierzące uszkodzenia DNA wykazały mniej pęknięć, gdy obecne było medium pochodzące od CAF lub oczyszczone białka macierzy. Kolagen, fibryonektyna i laminina każda zmniejszały uszkodzenia DNA, co wskazuje, że sama macierz, a nie tylko drobne składniki odżywcze, działa jako kluczowy czynnik ochronny.
Czujnik stresu łączy macierz z naprawą DNA
Aby odkryć, jak sygnały z macierzy są przekazywane wewnątrz komórek nowotworowych, autorzy przeanalizowali setki białek. Jeden wyróżniał się szczególnie: białko odpowiedzi na stres o nazwie NDRG1, zwłaszcza w jego aktywnej, ufosforylowanej formie. Białka macierzy i kondycjonowane medium CAF zwiększały aktywność NDRG1 przez receptory adhezji na powierzchni komórki zwane integrynami oraz łańcuch sygnałowy wewnątrzkomórkowych białek. Zablokowanie tego łańcucha, w szczególności rodziny kinaz SGK, uniemożliwiało aktywację NDRG1. W próbkach guzów od pacjentów i modelach mysich wysokie poziomy NDRG1 były wyraźnie obecne w pobliżu włóknistej stromy i wiązały się z szybszym wzrostem guza, większym podziałem komórek oraz gorszym przeżyciem po chemioterapii.
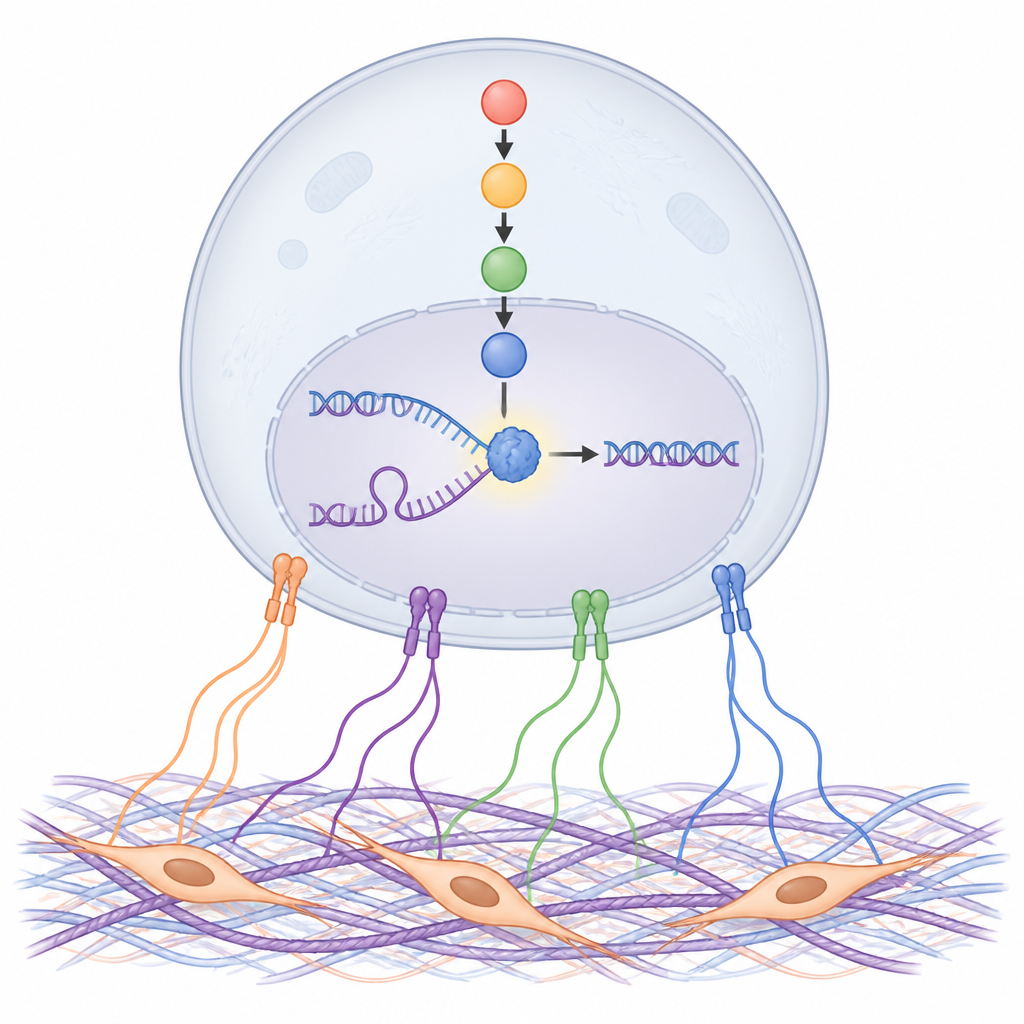
NDRG1 utrzymuje prawidłowe kopiowanie DNA
Badanie przyjrzało się następnie bliżej temu, co NDRG1 robi w odniesieniu do DNA. Przy użyciu czułych metod oznaczania i wyciągania nowo skopiowanego DNA badacze znaleźli NDRG1 bezpośrednio w miejscach replikacji DNA, szczególnie gdy widełki replikacyjne były zatrzymane przez leki. Usunięcie NDRG1 lub zablokowanie jego aktywacji przez SGK spowalniało kopiowanie DNA, utrudniało ponowne uruchomienie zatrzymanych widełek i zwiększało uszkodzenia DNA, zarówno in vitro, jak i w modelach mysich. Konkretny element budulcowy NDRG1, aminokwas histydyna na pozycji 194, okazał się niezbędny dla tej ochronnej roli, co sugeruje, że kształt NDRG1 i jego możliwa aktywność enzymatyczna są kluczowe dla stabilizacji widełek replikacyjnych.
Usuwanie szkodliwych supełków RNA–DNA
Jedną z częstych przyczyn zatrzymania replikacji DNA jest tworzenie się R-pętli — małych supłów, w których nowo syntetyzowane RNA przykleja się z powrotem do matrycy DNA. Autorzy pokazali, że komórki pozbawione NDRG1 lub jego aktywacji gromadzą te hybrydy RNA–DNA i doświadczają więcej kolizji między maszynerią replikacyjną a transkrypcyjną. Gdy dodano enzym, który specyficznie usuwa R-pętle, ruch widełek i uszkodzenia DNA wracały w kierunku normy. To wskazuje, że NDRG1 pomaga utrzymać płynność replikacji, ograniczając R-pętle i łagodząc konflikty między transkrypcją a replikacją.
Co to oznacza dla przyszłych terapii
Mówiąc w prostych słowach, włóknista tkanka otaczająca guzy trzustki wysyła sygnały, które włączają NDRG1 w komórkach nowotworowych, umożliwiając im naprawę uszkodzeń DNA wywołanych chemioterapią i kontynuowanie podziałów. Pacjenci, których guzy wykazują wyższą ekspresję NDRG1, mają tendencję do gorszych wyników po standardowych lekach uszkadzających DNA. Celowanie w szlak macierz–NDRG1 lub łączenie chemioterapii z lekami osłabiającymi funkcję naprawczą NDRG1 mogłoby uczynić komórki nowotworowe bardziej podatnymi, bez zwiększania dawek toksycznych terapii.
Cytowanie: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Słowa kluczowe: rak trzustki, mikrośrodowisko guza, naprawa DNA, fibroblasty związane z rakiem, R-pętle