Clear Sky Science · ru
Фибробласты, ассоциированные с раком, регулируют репарацию ДНК при раке поджелудочной железы через переработку R-спиралей, опосредованную NDRG1
Почему окружение опухоли имеет значение
Рак поджелудочной железы известно тяжело лечится отчасти потому, что опухоли находятся в плотной, волокнистой среде, богатой поддерживающими клетками и белками. В этом исследовании показано, что такая рубцовая ткань делает больше, чем просто препятствует поступлению препаратов. Она активно помогает раковым клеткам восстанавливать повреждения ДНК, вызванные химиотерапией, что позволяет опухолям выживать и рецидивировать. Понимание этой скрытой системы защиты открывает новые идеи для повышения эффективности лечения.
Жесткий рак в суровой среде
Панкреатическая дактильная аденокарцинома растет в бедной питательными веществами среде, насыщенной соединительной тканью, известной как строма. Большую часть этой стромы производят фибробласты, ассоциированные с раком (CAF), которые выделяют большие количества матричных внеклеточных белков, таких как коллаген и ламинин. Врачи давно заметили, что опухоли, богатые стромой, устойчивы к химиотерапии, но точные причины оставались неясными. Исследователи поставили вопрос, изменяют ли сигналы от этих фибробластов и их матрицы напрямую реакцию раковых клеток на препараты, повреждающие ДНК.
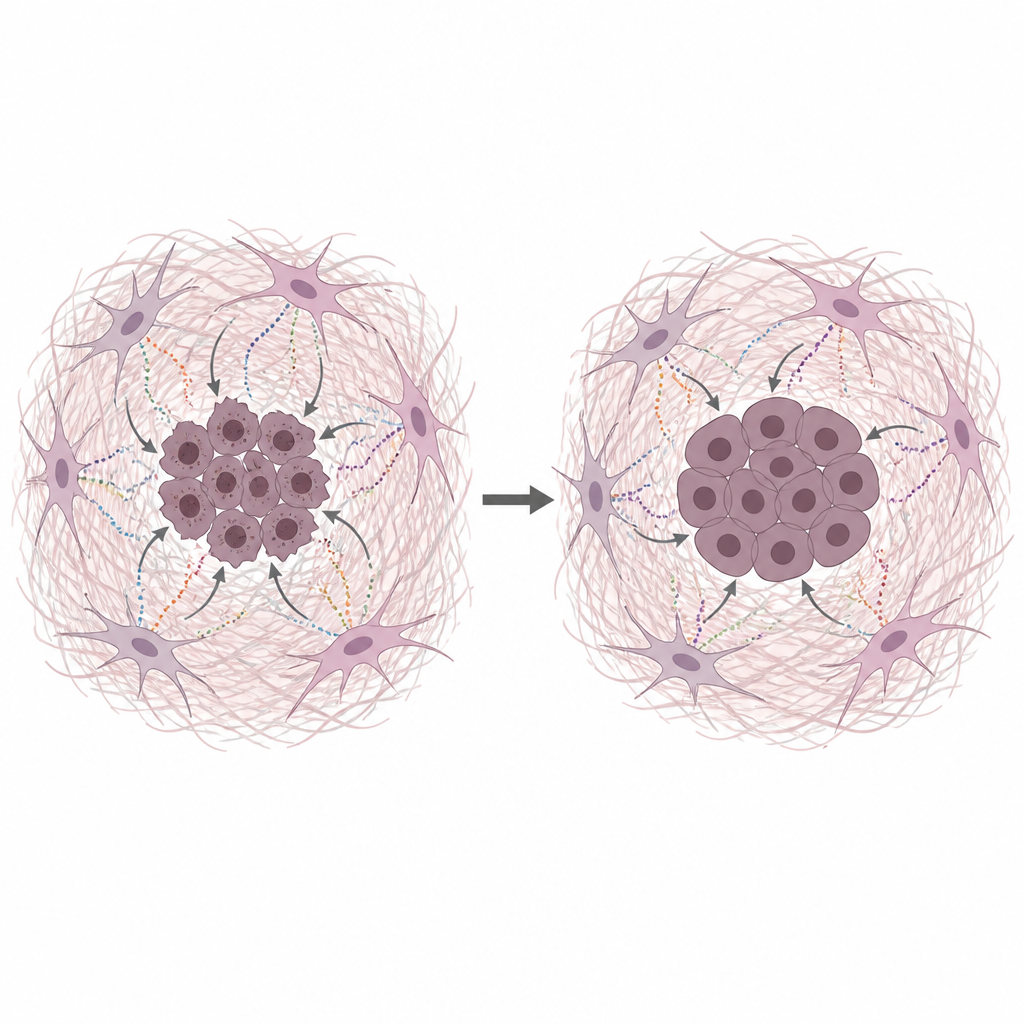
Секреты фибробластов защищают ДНК рака
Команда выращивала человеческие клетки рака поджелудочной железы вместе с средой, полученной от голодавших CAF, что имитирует бедные питательными веществами условия в реальных опухолях. Такая кондиционированная среда усиливала рост раковых клеток и повышала их устойчивость к нескольким распространенным химиопрепаратам, которые действуют за счет повреждения ДНК или торможения её копирования. Прямые тесты на повреждения ДНК показали меньше разрывов при наличии среды, полученной от CAF, или очищенных матричных белков. Коллаген, фибронектин и ламинин каждый снижали степень повреждений ДНК, что указывает на ключевую роль самой матрицы, а не только малых питательных веществ.
Датчик стресса связывает матрицу с репарацией ДНК
Чтобы выяснить, как сигналы от матрицы передаются внутри раковых клеток, авторы просканировали сотни белков. Выделился один — белок ответа на стресс NDRG1, особенно в его активной, фосфорилированной форме. Матричные белки и кондиционированная среда от CAF усиливали активность NDRG1 через клеточные адгезионные рецепторы — интегрины — и каскад сигнальных белков внутри клетки. Блокирование этой цепочки, в особенности семейства киназ SGK, предотвращало активацию NDRG1. В образцах опухолей пациентов и в мышиных моделях высокий уровень NDRG1 был наиболее выражен рядом с фибротической стромой и ассоциировался с более быстрым ростом опухоли, повышенной пролиферацией и худшей выживаемостью после химиотерапии.
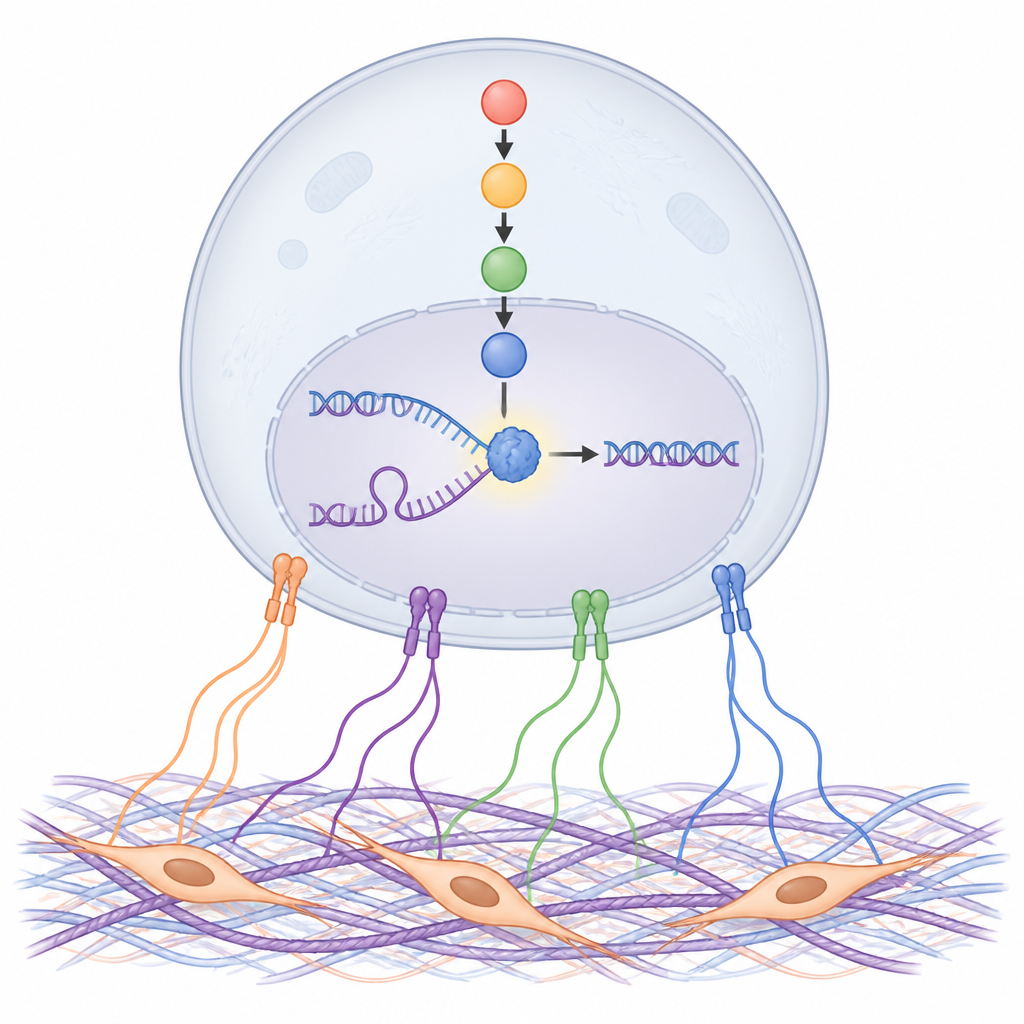
NDRG1 поддерживает нормальное копирование ДНК
Дальнейшее изучение показало, что именно делает NDRG1 с ДНК. С помощью чувствительных методов мечения и выделения недавно синтезированной ДНК исследователи обнаружили NDRG1 прямо в местах репликации ДНК, особенно когда вилки репликации останавливались под действием препаратов. Удаление NDRG1 или блокирование его активации через SGK замедляло копирование ДНК, затрудняло перезапуск остановившихся вилок и увеличивало повреждения ДНК как in vitro, так и у мышей. Конкретный строительный элемент NDRG1 — аминокислота гистидин в положении 194 — оказался необходим для этой защитной функции, что указывает на важность структуры NDRG1 и возможной ферментоподобной активности для стабилизации репликационных вилок.
Удаление вредных РНК–ДНК узлов
Частая причина остановки копирования ДНК — образование R-спиралей (R-loops), небольших узлов, где вновь синтезированная РНК присоединяется обратно к матрице ДНК. Авторы показали, что клетки, лишенные NDRG1 или его активации, накапливают эти РНК–ДНК гибриды и испытывают больше столкновений между механизмами репликации ДНК и транскрипции генов. При добавлении фермента, который специфически удаляет R-спирали, движение вилок и повреждения ДНК возвращались ближе к норме. Это указывает на то, что NDRG1 поддерживает плавность репликации, ограничивая образование R-спиралей и уменьшая конфликты между транскрипцией и репликацией.
Что это значит для будущих методов лечения
Проще говоря, фиброзная ткань, окружающая опухоли поджелудочной железы, посылает сигналы, которые включают NDRG1 внутри раковых клеток, позволяя им восстанавливать повреждения ДНК, вызванные химиотерапией, и продолжать деление. У пациентов с опухолями, экспрессирующими более высокий уровень NDRG1, как правило, результаты лечения стандартными препаратами, повреждающими ДНК, хуже. Нацеливание на путь матрица–NDRG1 или комбинирование химиотерапии с препаратами, ослабляющими репаративную функцию NDRG1, может сделать раковые клетки более уязвимыми без увеличения дозы токсичных препаратов.
Цитирование: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Ключевые слова: рак поджелудочной железы, микроокружение опухоли, репарация ДНК, фибробласты, ассоциированные с раком, R-спирали