Clear Sky Science · it
I fibroblasti associati al cancro regolano la riparazione del DNA nel tumore pancreatico tramite l’elaborazione degli R-loop mediata da NDRG1
Perché il quartiere del tumore conta
Il cancro pancreatico è notoriamente difficile da trattare, in parte perché i tumori si trovano all’interno di un ambiente di supporto duro e fibroso fatto di cellule e proteine. Questo studio rivela che quel tessuto simile a una cicatrice non si limita a ostacolare l’ingresso dei farmaci: aiuta attivamente le cellule tumorali a riparare i danni al DNA causati dalla chemioterapia, permettendo ai tumori di sopravvivere e ricomparire. Capire questo sistema di protezione nascosto offre nuove idee per rendere i trattamenti più efficaci.
Un cancro ostico in un ambiente ostile
L’adenocarcinoma duttale pancreatico cresce in un contesto povero di nutrienti, ricco di tessuto connettivo noto come stroma. Gran parte di questo stroma è prodotto dai fibroblasti associati al cancro, o CAF, che secernono grandi quantità di proteine della matrice extracellulare come collagene e laminina. I medici sanno da tempo che i tumori ricchi di stroma sono resistenti alla chemioterapia, ma i motivi esatti non erano chiari. I ricercatori si sono chiesti se i segnali provenienti da questi fibroblasti e dalla loro matrice alterino direttamente la risposta delle cellule tumorali ai farmaci che danneggiano il DNA.
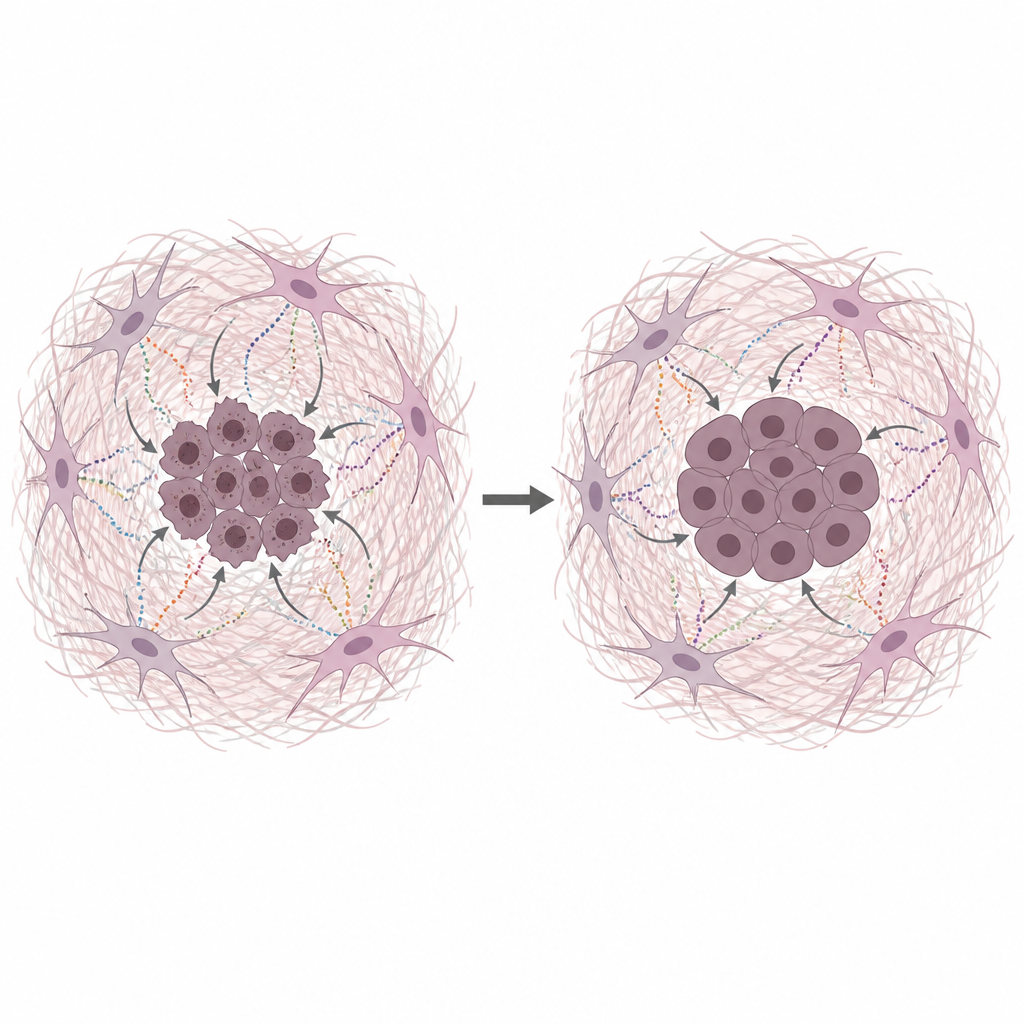
Le secrezioni dei fibroblasti proteggono il DNA del cancro
Il team ha coltivato cellule umane di cancro pancreatico insieme a un mezzo prelevato da CAF affamate, che imita le condizioni povere di nutrienti dei tumori reali. Questo mezzo condizionato ha reso le cellule tumorali sia più proliferative sia più resistenti a diverse chemioterapie comuni che agiscono danneggiando il DNA o bloccandone la copia. Test diretti sui danni al DNA hanno mostrato meno rotture quando era presente il mezzo derivato dai CAF o proteine della matrice purificate. Collagene, fibronectina e laminina hanno ciascuno ridotto i danni al DNA, indicando che è la matrice stessa, non solo piccole sostanze nutritive, a funzionare come protettore chiave.
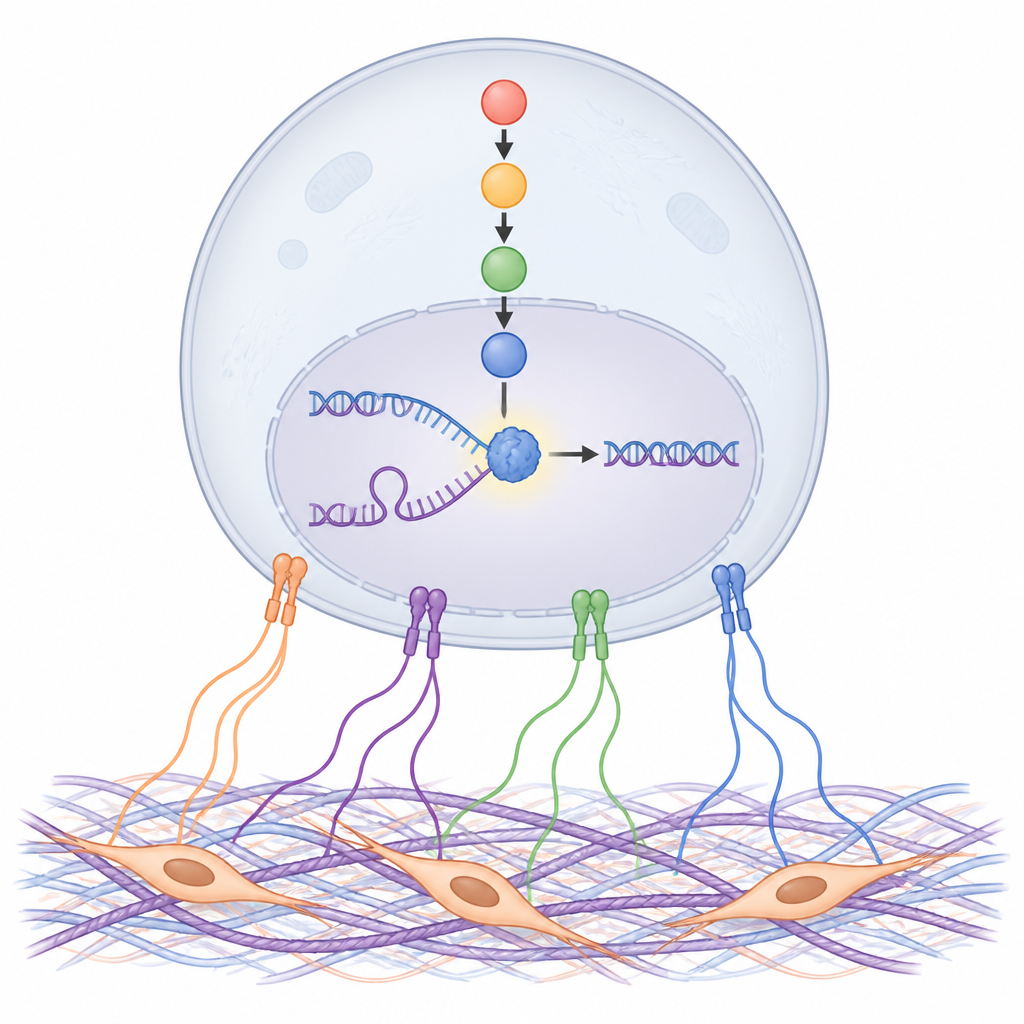
Un sensore dello stress collega la matrice alla riparazione del DNA
Per scoprire come i segnali della matrice vengono tradotti all’interno delle cellule tumorali, gli autori hanno esaminato centinaia di proteine. Una è emersa con chiarezza: una proteina della risposta allo stress chiamata NDRG1, in particolare nella sua forma attivata fosforilata. Le proteine della matrice e il mezzo condizionato dai CAF hanno aumentato l’attività di NDRG1 tramite recettori di adesione sulla superficie cellulare detti integrine e una catena di proteine di segnalazione intracellulare. Bloccare questa catena, in particolare una famiglia di chinasi chiamata SGK, ha impedito l’attivazione di NDRG1. Nei campioni tumorali di pazienti e in modelli murini, livelli elevati di NDRG1 erano più evidenti vicino allo stroma fibrótico e associati a crescita tumorale più rapida, maggiore proliferazione cellulare e sopravvivenza peggiore dopo chemioterapia.
NDRG1 mantiene la duplicazione del DNA in carreggiata
Lo studio si è poi concentrato su cosa faccia precisamente NDRG1 al DNA. Utilizzando metodi sensibili per marcare e isolare il DNA neo-sintetizzato, i ricercatori hanno trovato NDRG1 direttamente nei siti in cui il DNA viene replicato, soprattutto quando le forcelle di replicazione sono bloccate dai farmaci. Rimuovere NDRG1, o bloccarne l’attivazione tramite SGK, ha rallentato la replicazione del DNA, reso più difficile il riavvio delle forcelle bloccate e aumentato i danni al DNA, sia in colture sia nei topi. Un particolare elemento di NDRG1, l’amminoacido istidina in posizione 194, si è rivelato essenziale per questo ruolo protettivo, suggerendo che la forma di NDRG1 e una possibile attività simile a un enzima sono critiche per stabilizzare le forcelle di replicazione.
Eliminare i dannosi nodi RNA–DNA
Una causa frequente dell’arresto della duplicazione del DNA è la formazione di R-loop, piccoli intrecci in cui l’RNA neoformato si riattacca al filamento di DNA template. Gli autori hanno mostrato che le cellule prive di NDRG1 o della sua attivazione accumulano questi ibridi RNA–DNA e subiscono più collisioni tra le macchine che replicano il DNA e quelle che leggono i geni. Quando hanno aggiunto un enzima che rimuove specificamente gli R-loop, il movimento delle forcelle e i danni al DNA sono tornati verso valori normali. Questo indica che NDRG1 aiuta a mantenere la replicazione fluida limitando gli R-loop e attenuando questi conflitti trascrizione–replicazione.
Cosa significa per i trattamenti futuri
In termini semplici, il tessuto fibrotico che circonda i tumori pancreatici invia segnali che attivano NDRG1 all’interno delle cellule tumorali, permettendo loro di riparare i danni al DNA indotti dalla chemioterapia e di continuare a dividersi. I pazienti i cui tumori esprimono più NDRG1 tendono ad avere risultati peggiori con i farmaci standard che danneggiano il DNA. Mirare a questa via matrice–NDRG1, o combinare la chemioterapia con farmaci che indeboliscono la funzione riparativa di NDRG1, potrebbe rendere le cellule tumorali più vulnerabili senza aumentare la dose di trattamenti tossici.
Citazione: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Parole chiave: cancro pancreatico, microambiente tumorale, riparazione del DNA, fibroblasti associati al cancro, R-loop