Clear Sky Science · de
Fibroblasten in Tumorumgebung regulieren DNA-Reparatur bei Bauchspeicheldrüsenkrebs über NDRG1-vermittelte R-Loop-Verarbeitung
Warum die Nachbarschaft des Tumors zählt
Bauchspeicheldrüsenkrebs ist notorisch schwer zu behandeln, zum Teil weil die Tumoren in einem dichten, faserigen Umfeld aus Stützzellen und Proteinen liegen. Diese Studie zeigt, dass dieses narbenartige Gewebe mehr tut, als nur das Eindringen von Medikamenten zu erschweren. Es hilft aktiv den Krebszellen, die durch Chemotherapie verursachten DNA-Schäden zu reparieren, sodass Tumoren überleben und zurückkehren können. Das Verständnis dieses verborgenen Schutzsystems liefert neue Ansatzpunkte, um Therapien wirksamer zu machen.
Ein hartnäckiger Krebs in rauer Umgebung
Pankreasduktales Adenokarzinom wächst in einem nährstoffarmen Milieu, das von Bindegewebe, dem sogenannten Stroma, durchsetzt ist. Ein großer Teil dieses Stromas wird von tumorassoziierten Fibroblasten (CAFs) gebildet, die große Mengen an extrazellulären Matrixproteinen wie Kollagen und Laminin abgeben. Ärztinnen und Ärzte wissen seit Langem, dass stroma-reiche Tumoren gegen Chemotherapie resistent sind, doch die genauen Gründe waren unklar. Die Forschenden fragten, ob Signale von diesen Fibroblasten und ihrer Matrix direkt verändern, wie Krebszellen auf DNA-schädigende Medikamente reagieren.
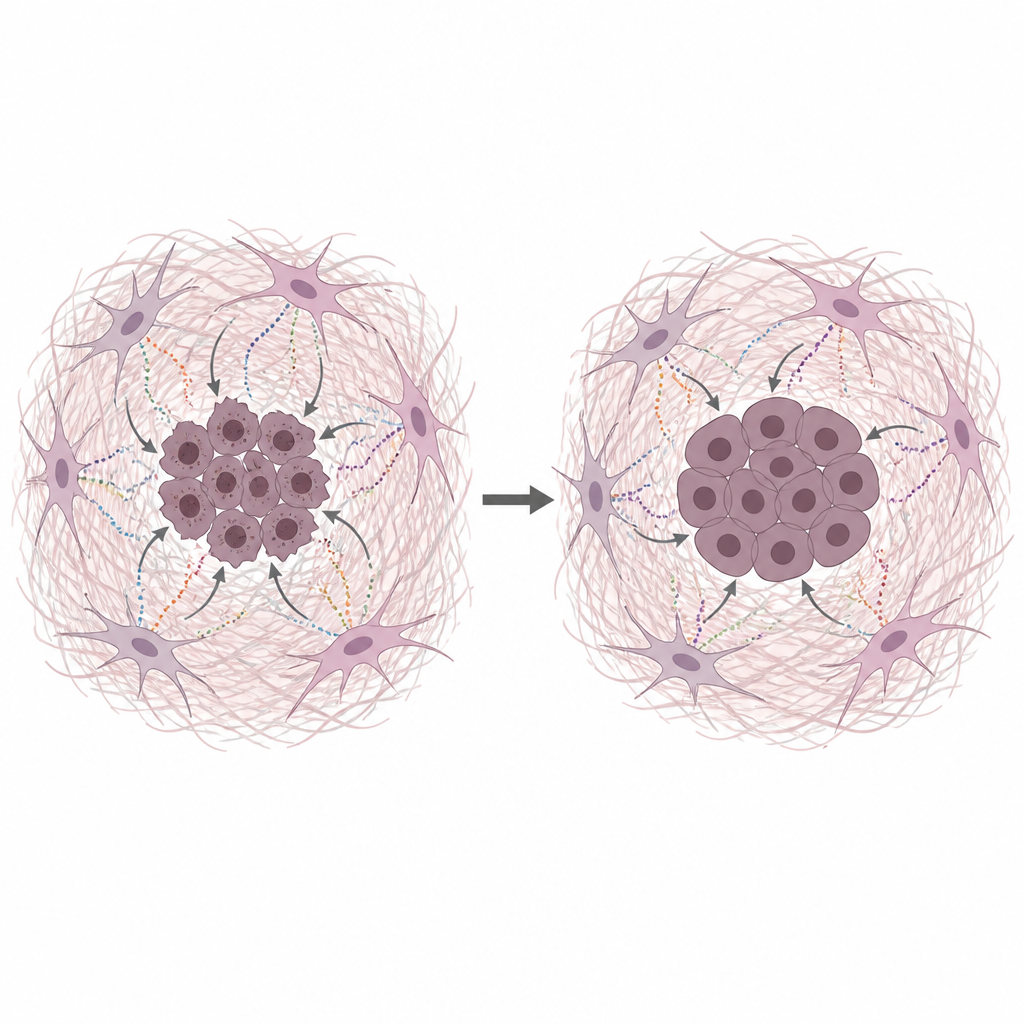
Fibroblasten-Sekrete schützen die Krebs-DNA
Das Team kultivierte humane Pankreaskrebszellen zusammen mit Medium, das von kalorien- oder nährstoff-entzogenen CAFs stammt und die nährstoffarmen Bedingungen in echten Tumoren nachahmt. Dieses konditionierte Medium ließ Krebszellen sowohl stärker wachsen als auch mehrere gängige Chemotherapien überstehen, die durch DNA-Schädigung oder das Blockieren der Replikation wirken. Direkte Tests auf DNA-Schäden zeigten weniger Brüche, wenn CAF-abgeleitetes Medium oder gereinigte Matrixproteine vorhanden waren. Kollagen, Fibronectin und Laminin verringerten jeweils die DNA-Schädigung, was auf die Matrix selbst – nicht nur auf kleine Nährstoffe – als wichtigen Schutzfaktor hinweist.
Ein Stresssensor verbindet die Matrix mit der DNA-Reparatur
Um aufzudecken, wie Matrix-Signale innerhalb der Krebszellen übersetzt werden, untersuchten die Autorinnen und Autoren Hunderte von Proteinen. Eines hob sich hervor: das Stress-Reaktionsprotein NDRG1, insbesondere in seiner aktivierten, phosphorylierten Form. Matrixproteine und CAF-konditioniertes Medium steigerten die NDRG1-Aktivität über zelloberflächenständige Adhäsionsrezeptoren, sogenannte Integrine, und eine Signalkette innerhalb der Zelle. Das Blockieren dieser Kette, insbesondere einer Kinase-Familie namens SGK, verhinderte die Aktivierung von NDRG1. In Tumorproben von Patientinnen und Patienten sowie in Mausmodellen fanden sich hohe NDRG1-Spiegel vor allem in der Nähe von fibrösem Stroma und waren mit schnellerem Tumorwachstum, erhöhter Zellteilung und schlechterem Überleben nach Chemotherapie assoziiert.
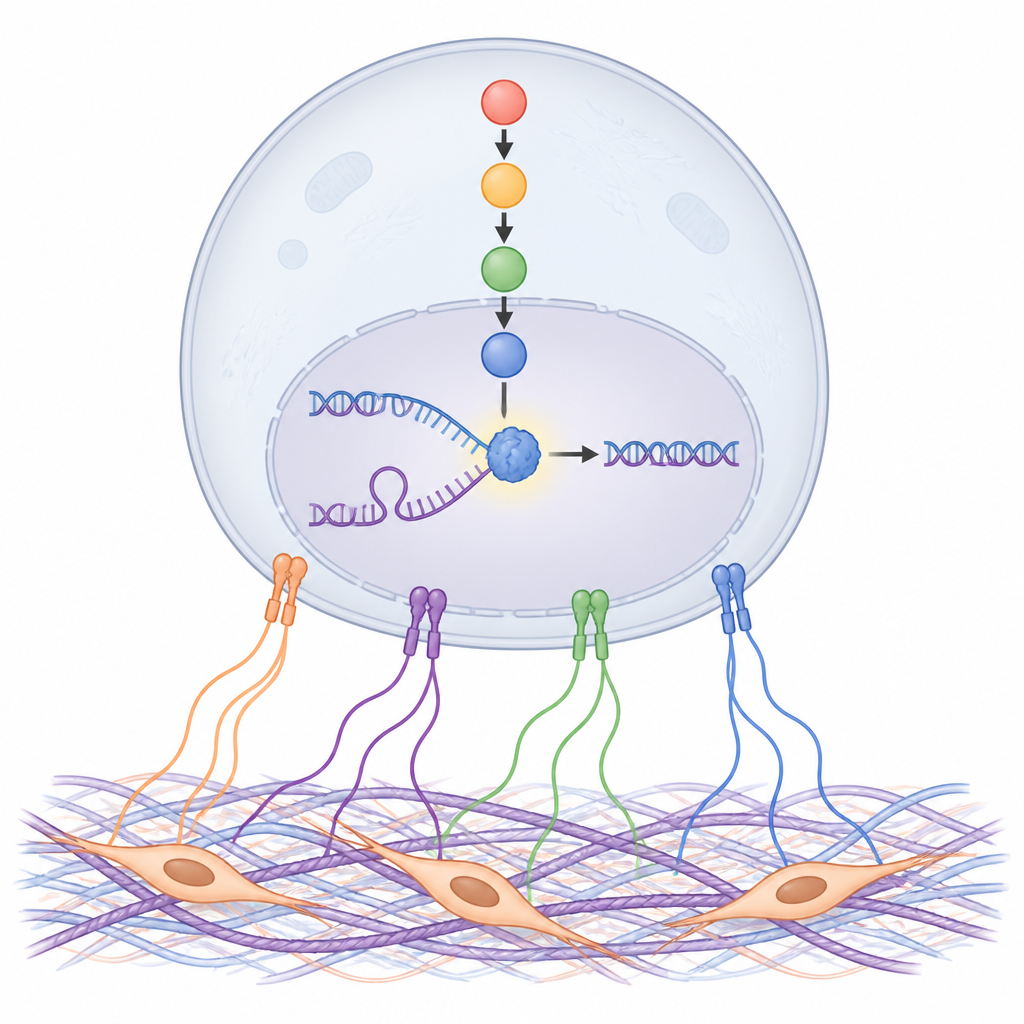
NDRG1 hält die DNA-Replikation auf Kurs
Die Studie untersuchte anschließend genauer, was NDRG1 an der DNA bewirkt. Mit empfindlichen Methoden, um neu synthetisierte DNA zu markieren und herauszufiltern, fanden die Forschenden NDRG1 direkt an den Stellen, an denen DNA repliziert wird, besonders wenn Replikationsgabeln durch Medikamente gestoppt waren. Entfernen von NDRG1 oder das Blockieren seiner Aktivierung durch SGK verlangsamte die DNA-Replikation, erschwerte das Wiederanfahren gestoppter Gabeln und erhöhte die DNA-Schädigung, sowohl in Zellkulturen als auch in Mäusen. Eine spezifische Aminosäure in NDRG1, das Histidin an Position 194, erwies sich als essentiell für diese Schutzfunktion, was darauf hindeutet, dass Form und mögliche enzymähnliche Aktivität von NDRG1 kritisch zur Stabilisierung von Replikationsgabeln beitragen.
Entfernung schädlicher RNA–DNA-Verwicklungen
Eine häufige Ursache für das Stocken der DNA-Replikation ist die Bildung von R-Loops, kleine Verwicklungen, bei denen frisch gebildete RNA wieder an die DNA-Vorlage bindet. Die Autorinnen und Autoren zeigten, dass Zellen ohne NDRG1 oder ohne dessen Aktivierung diese RNA–DNA-Hybride akkumulieren und mehr Kollisionen zwischen den Maschinen erleben, die DNA replizieren, und denen, die Gene ablesen. Wenn sie ein Enzym zugaben, das spezifisch R-Loops entfernt, normalisierten sich Gabelbewegung und DNA-Schädigung wieder. Das weist darauf hin, dass NDRG1 die Replikation dadurch unterstützt, dass es R-Loops begrenzt und Transkriptions–Replikations-Konflikte entschärft.
Was das für künftige Therapien bedeutet
Vereinfacht gesagt: Das fibröse Gewebe um Pankreastumoren sendet Signale, die NDRG1 in Krebszellen anschalten und es ihnen ermöglichen, durch Chemotherapie verursachte DNA-Schäden zu reparieren und weiter zu teilen. Patientinnen und Patienten, deren Tumoren mehr NDRG1 exprimieren, schneiden bei Standardtherapien mit DNA-schädigenden Mitteln tendenziell schlechter ab. Das Anvisieren dieses Matrix–NDRG1-Wegs oder die Kombination von Chemotherapie mit Wirkstoffen, die NDRG1s Reparaturfunktion schwächen, könnte Krebszellen verwundbarer machen, ohne die Dosis toxischer Behandlungen zu erhöhen.
Zitation: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Schlüsselwörter: Bauchspeicheldrüsenkrebs, Tumormikroumgebung, DNA-Reparatur, tumorassoziierte Fibroblasten, R-Loops