Clear Sky Science · ar
الخلايا الليفية المرتبطة بالسرطان تُنظّم إصلاح الحمض النووي في سرطان البنكرياس عبر معالجة العقد R بواسطة NDRG1
لماذا يهم حي الورم المحيط
يُعد سرطان البنكرياس من أصعب السرطانات علاجاً، جزئياً لأن الأورام تنمو داخل حي صلب ليفي مكوّن من خلايا داعمة وبروتينات. تكشف هذه الدراسة أن ذلك النسيج الشبيه بالندبة لا يقتصر دوره على عرقلة دخول الأدوية، بل يساعد فعلياً خلايا السرطان على إصلاح أضرار الحمض النووي الناجمة عن العلاج الكيميائي، مما يسمح للأورام بالبقاء والانتكاس. فهم هذا النظام الوقائي الخفي يفتح آفاقاً جديدة لتحسين فعالية العلاجات.
سرطان عنيد في بيئة قاسية
ينمو سرطان القنوات البنكرياسية الغدي في بيئة فقيرة بالمغذيات ومملوءة بالنسيج الضام المعروف بالسدى. ينتج جزء كبير من هذا السدى عن الخلايا الليفية المرتبطة بالسرطان (CAFs)، التي تفرز كميات كبيرة من بروتينات المصفوفة خارج الخلية مثل الكولاجين واللمنين. يعرف الأطباء منذ زمن أن الأورام الغنية بالسدى تقاوم العلاج الكيميائي، لكن الأسباب الدقيقة لم تكن واضحة. تساءل الباحثون عما إذا كانت إشارات هذه الخلايا الليفية ومصففتها تغيّر مباشرة كيفية استجابة خلايا السرطان للأدوية المسببة لأضرار الحمض النووي.
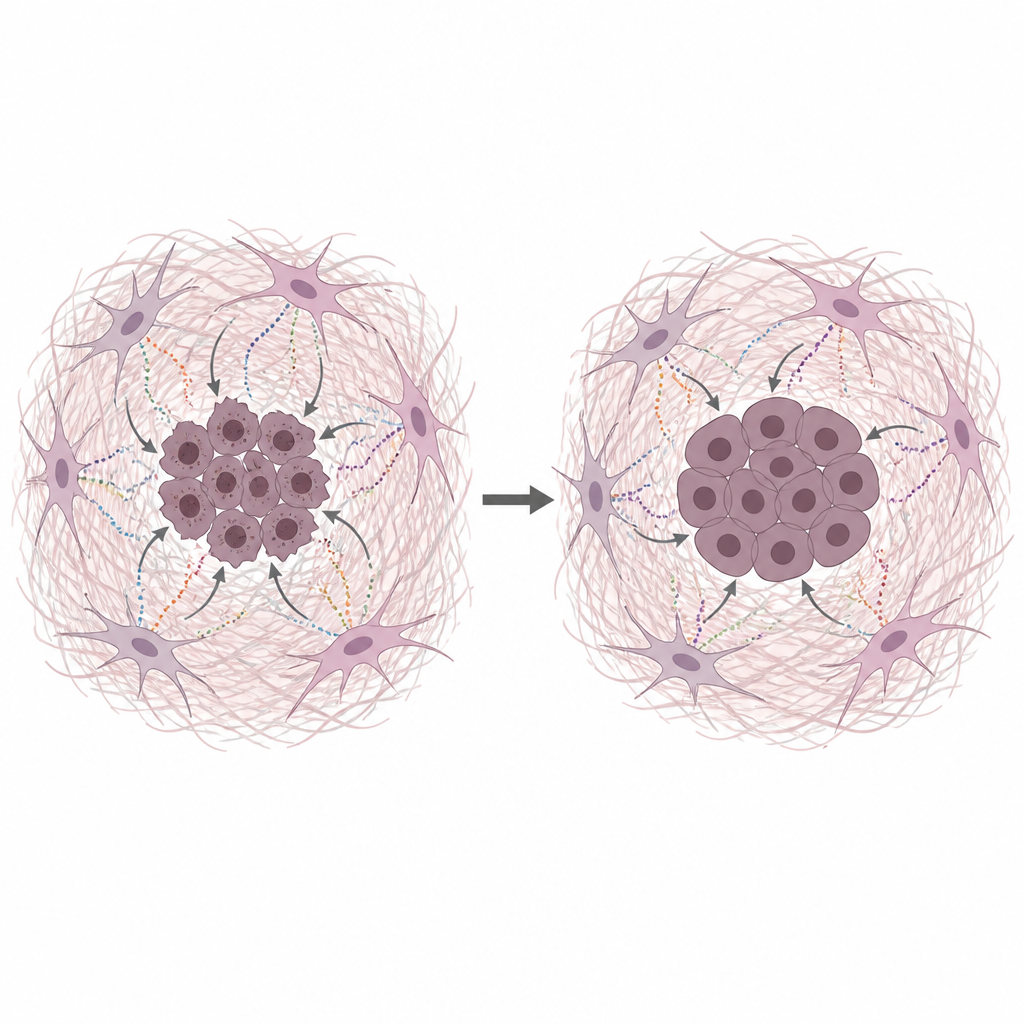
إفرازات الخلايا الليفية تحمي حمض سرطان الخلايا النووي
زرع الفريق خلايا سرطان بنكرياس بشرية مع وسط مأخوذ من خلايا CAF مجاعة، ليحاكي ظروف نقص المغذيات الموجودة في الأورام الحقيقية. جعل هذا الوسط المشروط خلايا السرطان تنمو أكثر وتتحمل عدة علاجات كيميائية شائعة تعمل عن طريق إتلاف الحمض النووي أو تعطيل نسخه. أظهرت اختبارات مباشرة لأضرار الحمض النووي وجود كسور أقل عندما وُجد وسط مشتق من CAF أو بروتينات مصفوفة مُنقّاة. خفّض كل من الكولاجين والفايبرونيكتين واللمنين من مقدار أضرار الحمض النووي، مما يشير إلى أن المصفوفة نفسها، وليس فقط العناصر الغذائية الصغيرة، هي الحاجز الحامي الرئيسي.
مستشعر الإجهاد يربط المصفوفة بإصلاح الحمض النووي
لكي يكشفوا كيف تُترجم إشارات المصفوفة داخل خلايا السرطان، مسح المؤلفون مئات البروتينات. برز بروتين واحد: بروتين استجابة للإجهاد يُسمى NDRG1، لا سيما في شكله المُنشَّط الفوسفوريلي. زادت بروتينات المصفوفة والوسط المشروط من نشاط NDRG1 عبر مستقبلات التصاق سطحية تُدعى الإنتغرينات وسلسلة من بروتينات الإشارة داخل الخلية. منع هذه السلسلة، وخصوصاً عائلة كينازات تُدعى SGK، حال دون تنشيط NDRG1. في عينات أورام من مرضى ونماذج فئران، كانت مستويات NDRG1 المرتفعة أكثر بروزا قرب السدى الليفي وارتبطت بنمو أسرع للورم، وزيادة في انقسام الخلايا وسوء بقاء بعد العلاج الكيميائي.
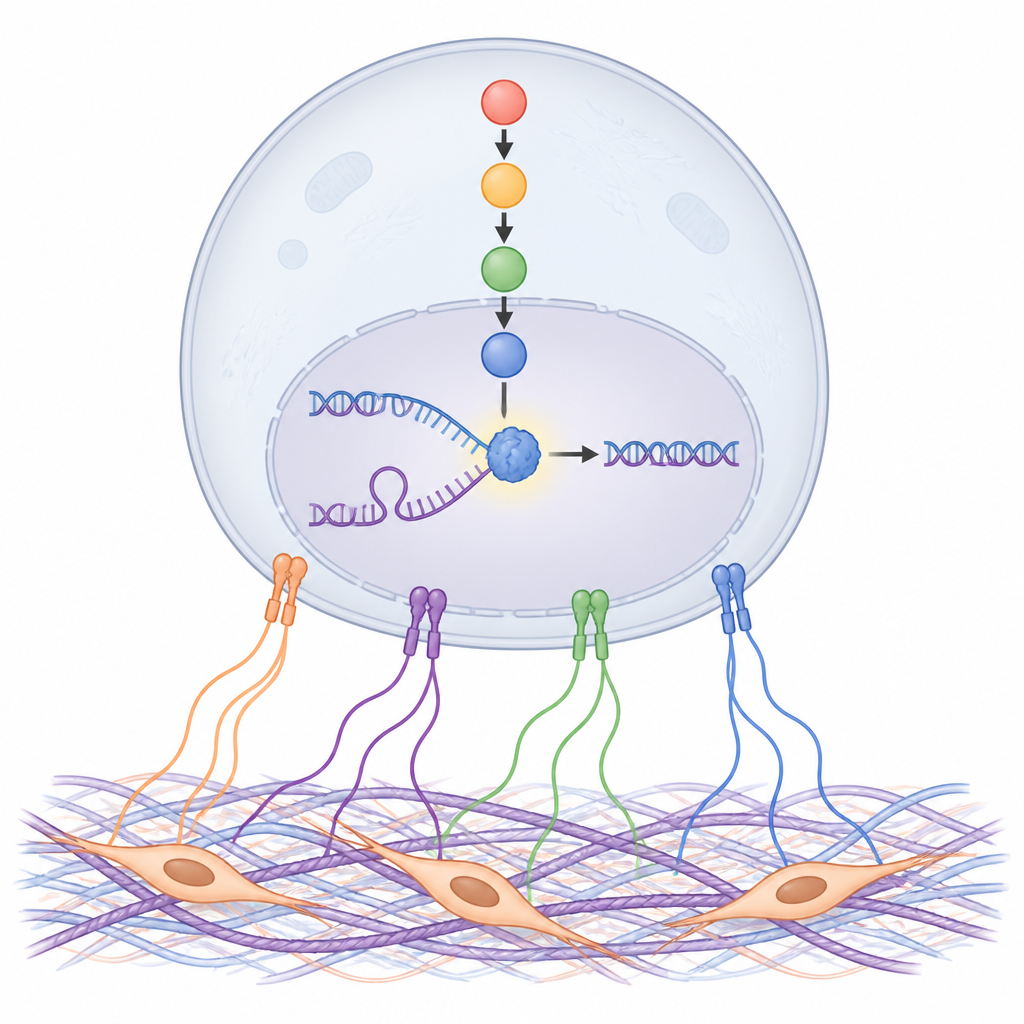
NDRG1 يحافظ على انسيابية نسخ الحمض النووي
انتقل البحث للتركيز على ما يفعله NDRG1 فعلاً للحمض النووي. باستخدام طرق حساسة لوسم وسحب الحمض النووي المنسوخ حديثاً، وجد الباحثون NDRG1 مباشرة في مواقع تكرار الحمض النووي، خصوصاً عندما تتعطل شوكات النسخ بفعل الأدوية. أدى حذف NDRG1، أو منع تنشيطه بواسطة SGK، إلى تباطؤ نسخ الحمض النووي، وصعوبة أكبر في إعادة تشغيل الشوكات المتعطلة وزيادة أضرار الحمض النووي، سواء في المختبر أو في الفئران. ثبت أن لبنة بنيوية محددة في NDRG1، الحمض الأميني الهستيدين عند الموضع 194، ضرورية لهذا الدور الوقائي، ما يشير إلى أن بنية NDRG1 ونشاطه المشابه للإنزيم حاسمان لاستقرار شوكات النسخ.
إزالة تشابكات الحمض النووي الريبي–الحمض النووي الضارة
أحد الأسباب المتكررة لتعطل نسخ الحمض النووي هو تكوّن عقيدات R، وهي تشابكات صغيرة حيث يلصق الحمض النووي الريبي الجديد نفسه مجدداً بقالب الحمض النووي. أظهر المؤلفون أن الخلايا التي تفتقد NDRG1 أو تنشيطه تتراكم فيها هذه الهجائن RNA–DNA وتتعرض لمزيد من التصادمات بين آليات نسخ الحمض النووي وآليات نسخ الجينات. عندما أضافوا إنزيمًا يزيل عقيدات R تحديداً، عاد تحرك الشوكات ومستوى أضرار الحمض النووي إلى أقرب الحالة الطبيعية. يشير هذا إلى أن NDRG1 يساعد على إبقاء التكرار جارياً بسلاسة عبر الحد من عقيدات R وتخفيف صراعات النسخ–التكرار.
ما الذي يعنيه هذا للعلاجات المستقبلية
بعبارة بسيطة، يرسل النسيج الليفي المحيط بأورام البنكرياس إشارات تُشغّل NDRG1 داخل خلايا السرطان، ما يمكّنها من إصلاح الأضرار التي يتسبب بها العلاج الكيميائي في الحمض النووي ومواصلة الانقسام. يميل المرضى الذين تعبر أورامهم عن مستويات أعلى من NDRG1 إلى نتائج أسوأ عند استخدام الأدوية التقليدية المسببة لأضرار الحمض النووي. قد يجعل استهداف مسار المصفوفة–NDRG1، أو الجمع بين العلاج الكيميائي وأدوية تُضعِف وظيفة إصلاح NDRG1، خلايا السرطان أكثر عرضة للعلاج من دون زيادة جرعات العلاجات السامة.
الاستشهاد: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
الكلمات المفتاحية: سرطان البنكرياس, البيئة الميكروية للورم, إصلاح الحمض النووي, الخلايا الليفية المرتبطة بالسرطان, عقيدات R