Clear Sky Science · tr
Pankreas kanserinde DNA onarımını NDRG1 aracılı R-döngü işleme yoluyla düzenleyen kanser ilişkili fibroblastlar
Neden tümörün çevresi önemlidir
Pankreas kanseri, kısmen tümörlerin sert, lifli destek hücreleri ve proteinleriyle çevrili bir ortamda yer alması nedeniyle tedavisi son derece zor bir hastalıktır. Bu çalışma, o skar benzeri dokunun ilaçların girişini engellemekten öte bir işleve sahip olduğunu ortaya koyuyor. Bu doku, kemoterapinin yol açtığı DNA hasarını kanser hücrelerinin onarmasına aktif olarak yardımcı oluyor ve tümörlerin hayatta kalıp yeniden büyümesine olanak tanıyor. Bu gizli koruma sistemini anlamak, tedavilerin etkinliğini artırmak için yeni fikirler sunuyor.
Zorlu bir tümör, zorlu bir ortam
Pankreatik duktal adenokarsinom, stroma olarak bilinen bağ dokusuyla dolu, besin açısından yoksun bir ortamda büyür. Bu stromanın büyük bir kısmını, kolajen ve laminin gibi ekstrasellüler matris proteinlerini bol miktarda salgılayan kanser ilişkili fibroblastlar (CAF'lar) oluşturur. Klinik olarak zaten stroması yoğun tümörlerin kemoterapiye dirençli olduğu biliniyordu, ancak bunun kesin nedenleri belirsizdi. Araştırmacılar, bu fibroblastlar ve onların matriksinin salgıladığı sinyallerin kanser hücrelerinin DNA hasarına yol açan ilaçlara yanıtını doğrudan değiştirip değiştirmediğini sordu.
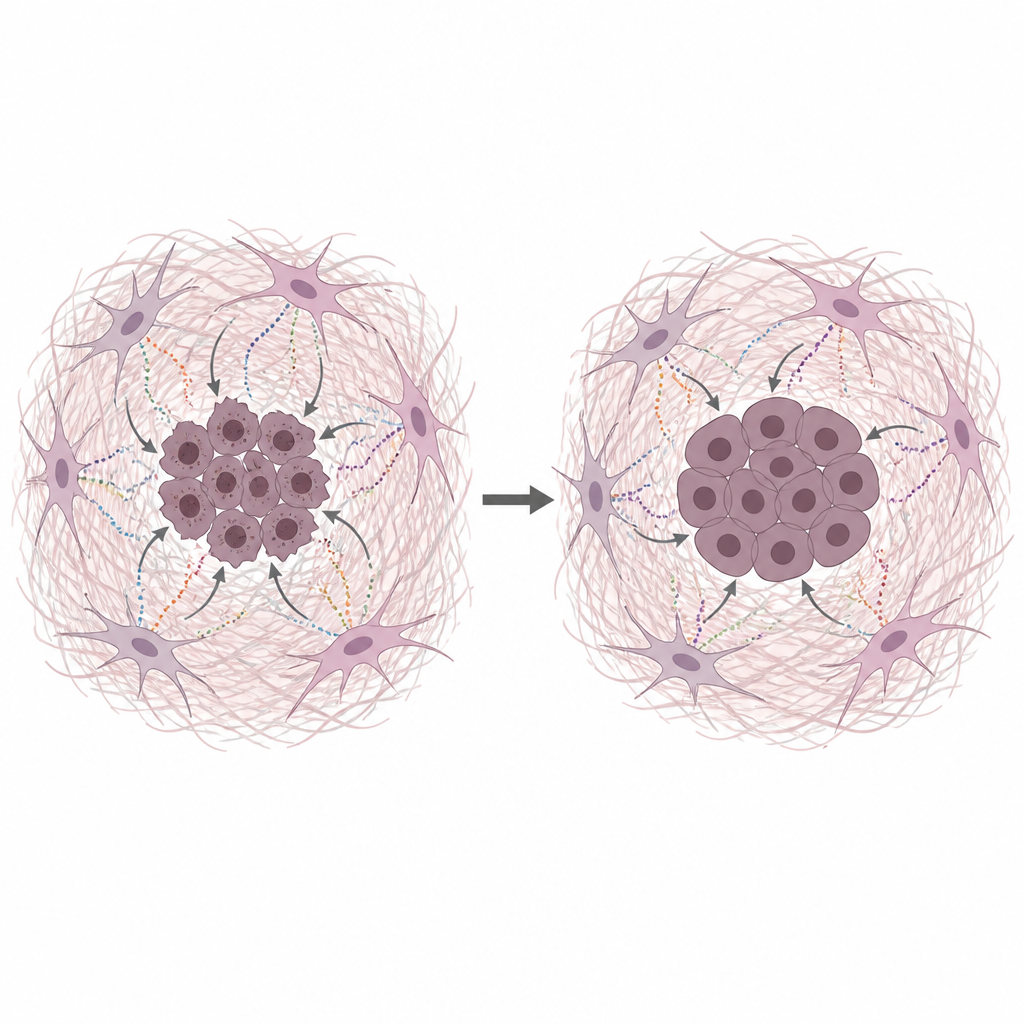
Fibroblast salgıları kanser DNA’sını koruyor
Araştırma ekibi, insan pankreas kanseri hücrelerini aç bırakılmış CAF'lardan alınan ortam ile birlikte büyüttü; bu ortam gerçek tümörlerdeki besin fakirliğini taklit eder. Bu kondisyone ortam, kanser hücrelerinin hem daha fazla büyümesini hem de DNA'ya zarar veren veya kopyalanmasını durduran birkaç yaygın kemoterapi ilacına karşı dayanıklılık kazanmasını sağladı. DNA hasarının doğrudan testleri, CAF kaynaklı ortam veya saflaştırılmış matris proteinleri varlığında daha az kırık gösterdi. Kolajen, fibronectin ve laminin'in her biri DNA hasarını azalttı; bu da koruyucu etkinin yalnızca küçük besinlerden değil, matrisin kendisinden kaynaklandığını işaret ediyor.
Bir stres sensörü matriksi DNA onarımına bağlıyor
Matriks sinyallerinin kanser hücrelerinin içinde nasıl çevrilip iletildiğini ortaya çıkarmak için yazarlar yüzlerce proteini taradı. Öne çıkan bir protein bulundu: özellikle etkinleşmiş, fosforile formunda bir stres yanıtı proteini olan NDRG1. Matris proteinleri ve CAF-kondisyone ortam, integrin adı verilen hücre yüzey yapışma reseptörleri ve hücre içindeki bir dizi sinyal proteinleri aracılığıyla NDRG1 aktivitesini artırdı. Bu zinciri, özellikle SGK adlı bir kinaz ailesini bloke etmek, NDRG1 aktivasyonunu engelledi. Hasta ve fare tümör örneklerinde yüksek NDRG1 seviyeleri fibrotik stroma yakınında en belirgin şekilde görüldü ve daha hızlı tümör büyümesi, daha yüksek hücre bölünmesi ile ve kemoterapi sonrası daha kötü sağkalım ile ilişkilendirildi.
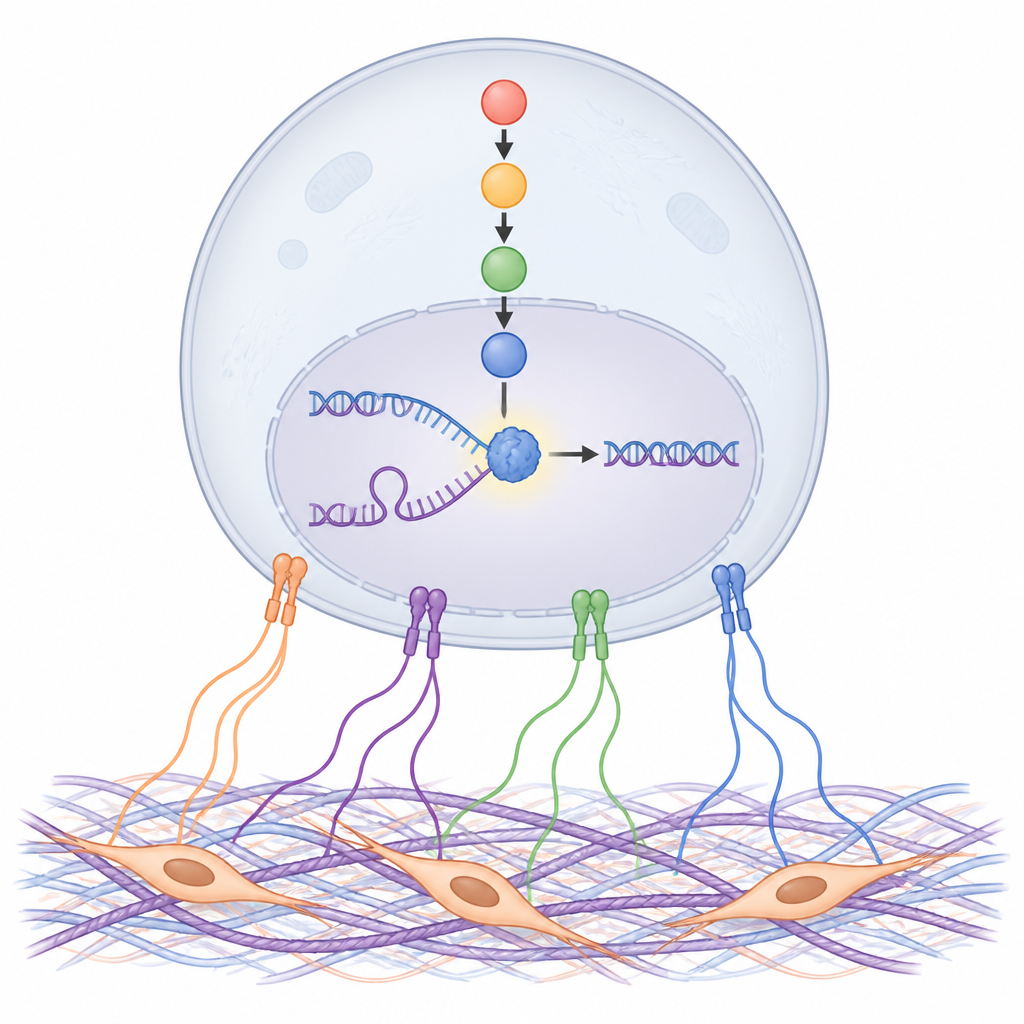
NDRG1, DNA kopyalanmasını rayında tutuyor
Çalışma daha sonra NDRG1'in DNA üzerinde gerçekten ne yaptığını ayrıntılandırdı. Yeni kopyalanan DNA'yı etiketleyip çekme konusunda hassas yöntemler kullanarak, araştırmacılar NDRG1'in özellikle ilaçlarla duraklatılan çatal bölgelerinde DNA'nın kopyalandığı yerlere doğrudan yerleştiğini buldu. NDRG1'in çıkarılması veya SGK ile etkinleşmesinin engellenmesi DNA kopyalanmasını yavaşlattı, duraklamış çatalların yeniden başlamasını zorlaştırdı ve hem kültürlerde hem de farelerde DNA hasarını artırdı. NDRG1'in belirli bir yapı taşı olan 194 numaralı pozisyondaki histidin aminoasidi bu koruyucu rol için hayati bulundu; bu da NDRG1'in yapısının ve olası enzim benzeri etkinliğinin replikasyon çatallarını stabilize etmek için kritik olduğunu düşündürüyor.
Zararlı RNA–DNA düğümlerinin temizlenmesi
Duraklamış DNA kopyalanmasının sık bir nedeni, yeni sentezlenen RNA'nın tekrar DNA şablonuna yapıştığı R-döngülerinin oluşmasıdır. Yazarlar, NDRG1 ya da onun etkinleşmesi eksik olan hücrelerin bu RNA–DNA hibritlerini biriktirdiğini ve DNA'yı kopyalayan makineler ile genleri okuyan makineler arasında daha fazla çarpışma yaşadığını gösterdi. Spesifik olarak R-döngülerini ortadan kaldıran bir enzim eklendiğinde çatalların hareketi ve DNA hasarı normale yaklaştı. Bu, NDRG1'in replikasyonu sorunsuz tutmaya R-döngülerini sınırlayarak ve bu transkripsiyon–replikasyon çatışmalarını hafifleterek yardımcı olduğunu gösteriyor.
Gelecek tedaviler için ne anlama geliyor
Basitçe söylemek gerekirse, pankreas tümörlerini çevreleyen fibrotik doku, kanser hücreleri içinde NDRG1'i açan sinyaller gönderir; bu da onların kemoterapi kaynaklı DNA hasarını onarmalarını ve bölünmeye devam etmelerini sağlar. Tümörlerinde daha fazla NDRG1 ifade eden hastalar, standart DNA hasarına yol açan ilaçlarla tedavide genellikle daha kötü sonuçlar gösterir. Bu matris–NDRG1 yolunu hedeflemek veya kemoterapiyi NDRG1’in onarım işlevini zayıflatan ilaçlarla birleştirmek, toksik tedavi dozunu artırmadan kanser hücrelerini daha savunmasız hale getirebilir.
Atıf: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Anahtar kelimeler: pankreas kanseri, tümör mikroçevresi, DNA onarımı, kanser ilişkili fibroblastlar, R-döngüleri