Clear Sky Science · pt
Fibroblastos associados ao câncer regulam o reparo de DNA no câncer pancreático por meio do processamento de R-loops mediado por NDRG1
Por que o entorno do tumor importa
O câncer de pâncreas é notoriamente difícil de tratar, em parte porque os tumores estão inseridos em um entorno resistente e fibroso feito de células de suporte e proteínas. Este estudo revela que esse tecido semelhante a cicatriz faz mais do que apenas bloquear a entrada de medicamentos. Ele ativa mecanismos que ajudam as células cancerosas a reparar os danos ao DNA causados pela quimioterapia, permitindo que os tumores sobrevivam e retornem. Compreender esse sistema de proteção oculto oferece novas ideias para tornar os tratamentos mais eficazes.
Um câncer agressivo em um ambiente hostil
O adenocarcinoma ductal pancreático cresce em um ambiente pobre em nutrientes e repleto de tecido conjuntivo conhecido como estroma. Grande parte desse estroma é produzido por fibroblastos associados ao câncer, ou CAFs, que secretam grandes quantidades de proteínas da matriz extracelular, como colágeno e laminina. Há muito tempo os médicos sabem que tumores ricos em estroma resistem à quimioterapia, mas as razões exatas não eram claras. Os pesquisadores investigaram se sinais desses fibroblastos e de sua matriz mudam diretamente a resposta das células cancerosas a drogas que danificam o DNA.
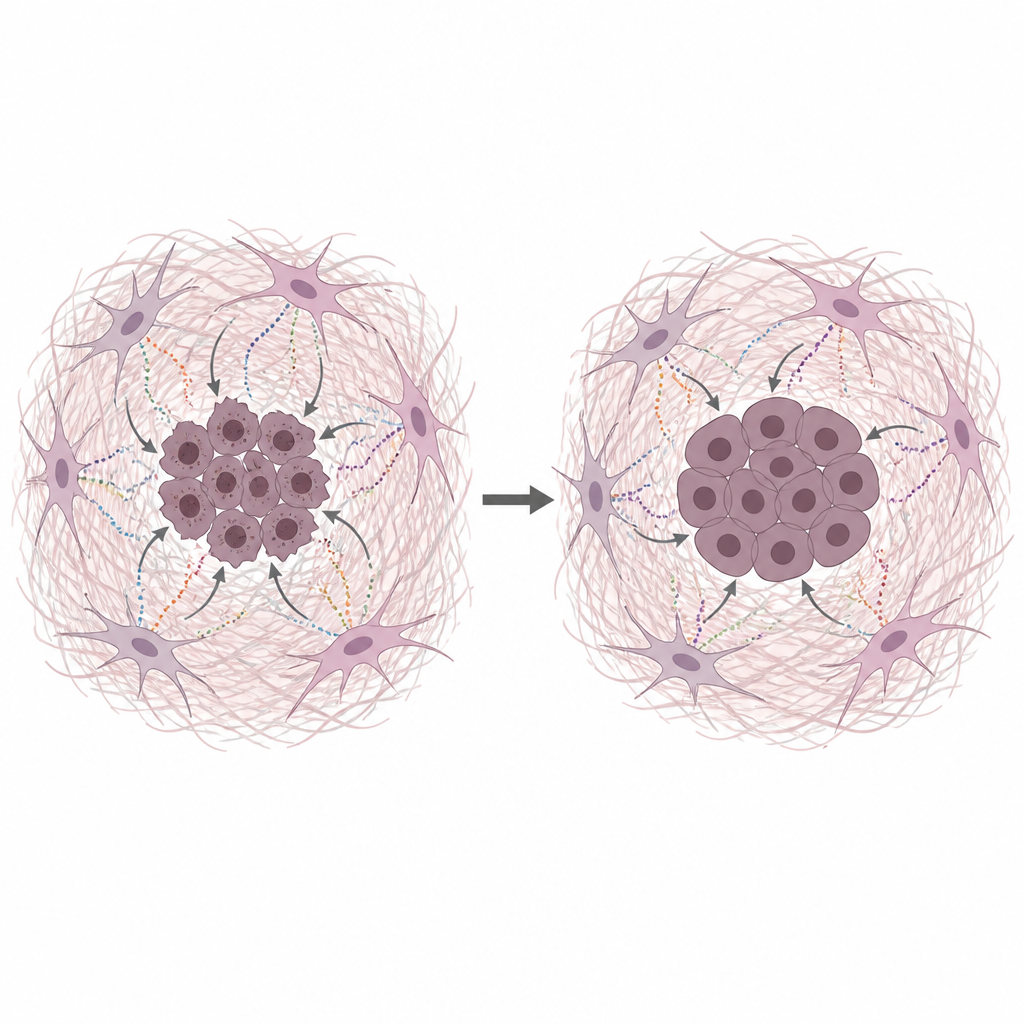
Secreções de fibroblastos protegem o DNA do câncer
A equipe cultivou células humanas de câncer pancreático junto com meio condicionado obtido de CAFs em privação de nutrientes, o que imita as condições pobres em nutrientes dos tumores reais. Esse meio condicionado fez com que as células cancerosas crescessem mais e resistissem a várias quimioterapias comuns que atuam danificando o DNA ou interrompendo sua cópia. Testes diretos de dano ao DNA mostraram menos quebras quando havia meio derivado de CAFs ou proteínas purificadas da matriz. Colágeno, fibronectina e laminina reduziram cada um o dano ao DNA, apontando para a própria matriz, não apenas pequenos nutrientes, como um protetor chave.
Um sensor de estresse conecta a matriz ao reparo do DNA
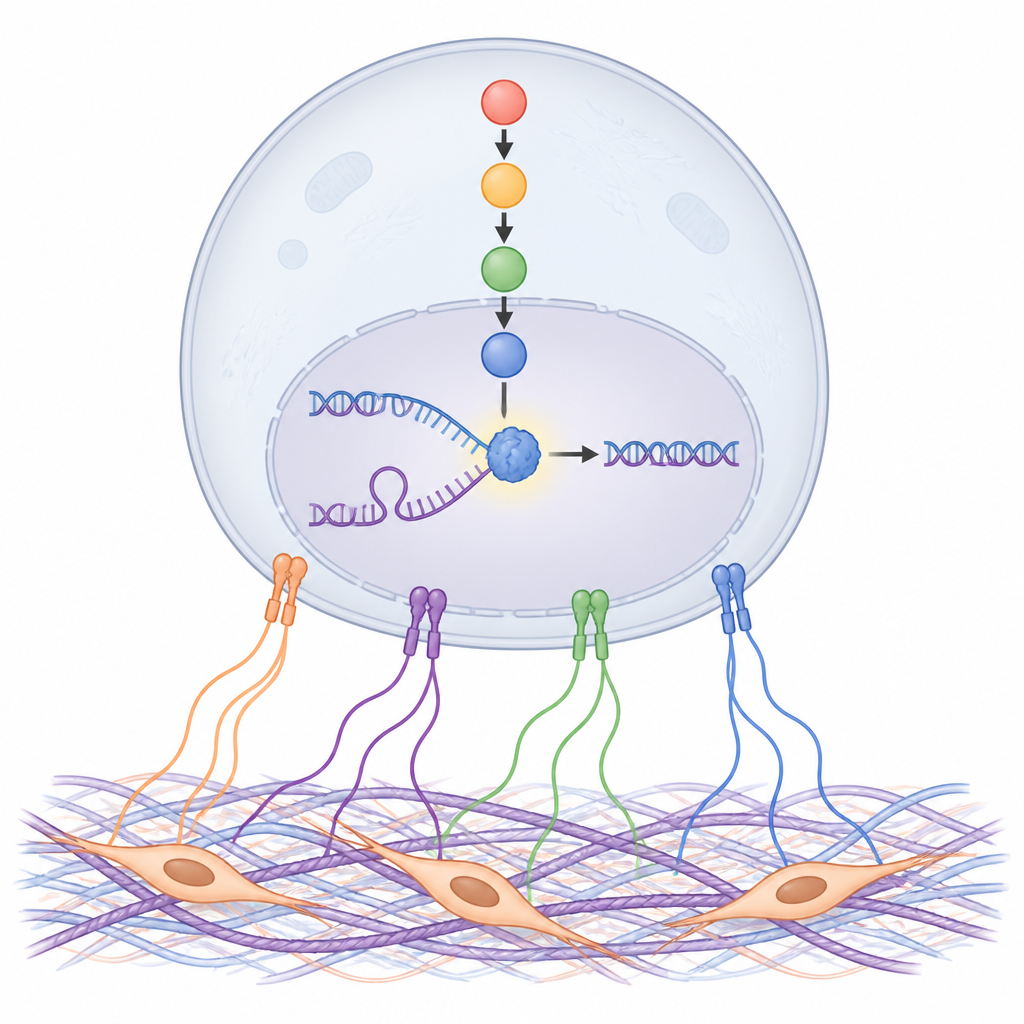
Para descobrir como os sinais da matriz são traduzidos dentro das células cancerosas, os autores examinaram centenas de proteínas. Uma se destacou: uma proteína de resposta ao estresse chamada NDRG1, especialmente em sua forma ativada por fosforilação. Proteínas da matriz e meio condicionado por CAFs aumentaram a atividade de NDRG1 por meio de receptores de adesão na superfície celular chamados integrinas e uma cadeia de proteínas de sinalização dentro da célula. Bloquear essa via, particularmente uma família de quinases chamada SGK, impediu a ativação de NDRG1. Em amostras tumorais de pacientes e modelos em camundongos, níveis elevados de NDRG1 foram mais proeminentes perto do estroma fibrótico e se associaram a crescimento tumoral mais rápido, maior divisão celular e pior sobrevida após quimioterapia.
NDRG1 mantém a cópia do DNA no caminho certo
O estudo então investigou mais de perto o que NDRG1 realmente faz ao DNA. Usando métodos sensíveis para marcar e isolar DNA recém-copiado, os pesquisadores encontraram NDRG1 diretamente nos locais onde o DNA está sendo replicado, especialmente quando forquilhas de replicação estavam paradas por drogas. Remover NDRG1, ou bloquear sua ativação por SGK, desacelerou a cópia do DNA, dificultou a retomada de forquilhas paradas e aumentou o dano ao DNA, tanto em culturas quanto em camundongos. Um resíduo específico de NDRG1, o aminoácido histidina na posição 194, mostrou-se essencial para esse papel protetor, sugerindo que a conformação de NDRG1 e sua possível atividade semelhante a enzima são críticas para estabilizar as forquilhas de replicação.
Eliminando emaranhados nocivos de RNA–DNA
Uma causa frequente de paralisação da cópia do DNA é a formação de R-loops, pequenos emaranhados onde o RNA recém-sintetizado se liga novamente ao molde de DNA. Os autores mostraram que células sem NDRG1 ou sem sua ativação acumulam esses híbridos RNA–DNA e experimentam mais colisões entre as máquinas que replicam o DNA e aquelas que transcrevem genes. Quando adicionaram uma enzima que remove especificamente R-loops, o movimento das forquilhas e o dano ao DNA retornaram próximo ao normal. Isso indica que NDRG1 ajuda a manter a replicação fluida ao limitar R-loops e amenizar esses conflitos transcrição–replicação.
O que isso significa para tratamentos futuros
Em termos simples, o tecido fibrótico que envolve tumores pancreáticos envia sinais que ativam NDRG1 dentro das células cancerosas, permitindo que elas consertem os danos ao DNA induzidos pela quimioterapia e continuem se dividindo. Pacientes cujos tumores expressam mais NDRG1 tendem a ter piores resultados com as drogas padrão que danificam o DNA. Alvo dessa via matriz–NDRG1, ou combinar quimioterapia com fármacos que enfraqueçam a função reparadora de NDRG1, pode tornar as células cancerosas mais vulneráveis sem aumentar a dose de tratamentos tóxicos.
Citação: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Palavras-chave: câncer de pâncreas, microambiente tumoral, reparo de DNA, fibroblastos associados ao câncer, R-loops