Clear Sky Science · es
Los fibroblastos asociados al cáncer regulan la reparación del ADN en el cáncer de páncreas mediante el procesamiento de R-loops mediado por NDRG1
Por qué importa el vecindario del tumor
El cáncer de páncreas es notoriamente difícil de tratar, en parte porque los tumores se alojan dentro de un entorno resistente y fibroso formado por células de soporte y proteínas. Este estudio revela que ese tejido similar a una cicatriz hace más que bloquear la entrada de fármacos: ayuda activamente a las células cancerosas a reparar el daño en el ADN causado por la quimioterapia, permitiendo que los tumores sobrevivan y reaparezcan. Comprender este sistema de protección oculto ofrece nuevas ideas para mejorar la eficacia de los tratamientos.
Un cáncer duro en un entorno hostil
El adenocarcinoma ductal pancreático crece en un entorno pobre en nutrientes y lleno de tejido conectivo conocido como estroma. Gran parte de este estroma lo producen los fibroblastos asociados al cáncer, o CAFs, que secretan grandes cantidades de proteínas de la matriz extracelular como colágeno y laminina. Desde hace tiempo se sabe que los tumores ricos en estroma resisten la quimioterapia, pero las razones exactas no estaban claras. Los investigadores se preguntaron si las señales procedentes de estos fibroblastos y su matriz cambian directamente la respuesta de las células cancerosas a los fármacos que dañan el ADN.
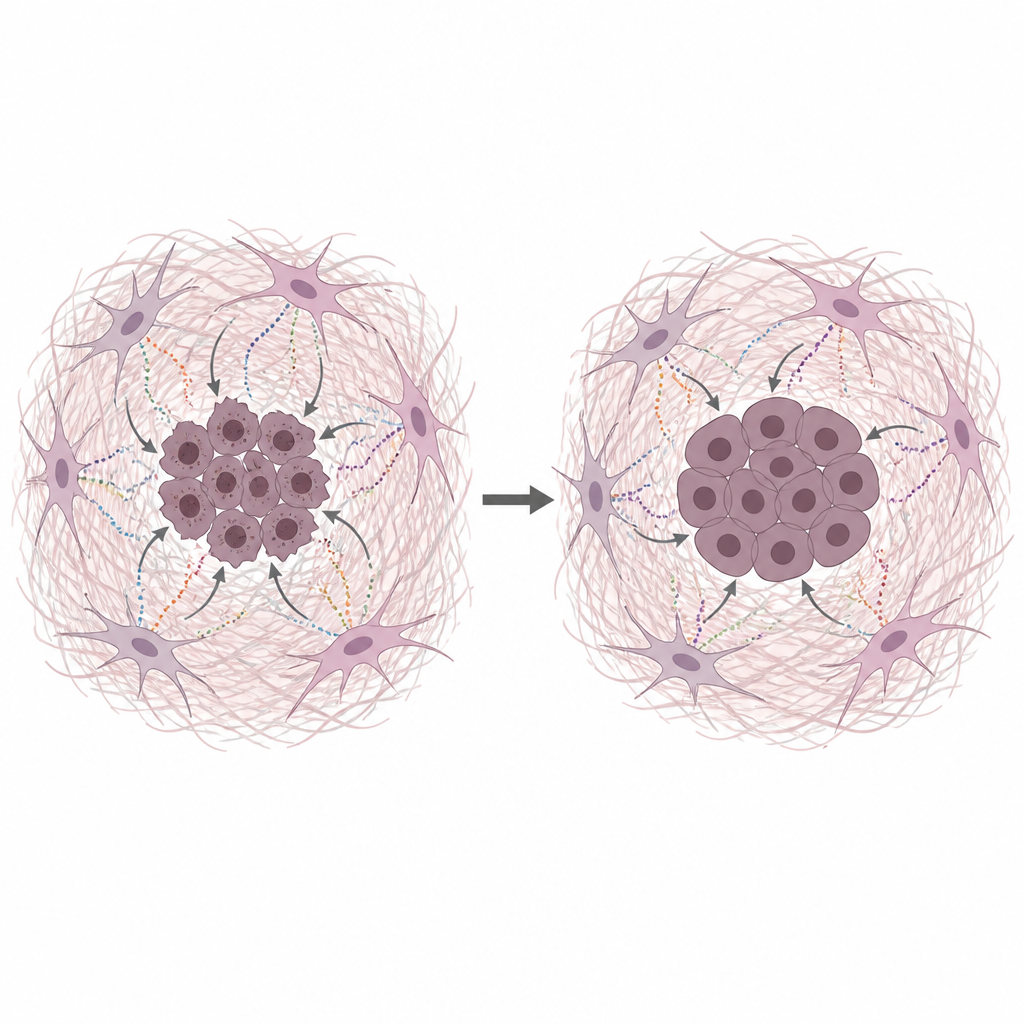
Las secreciones de los fibroblastos protegen el ADN canceroso
El equipo cultivó células humanas de cáncer de páncreas junto con medio tomado de CAFs privadas de nutrientes, que imita las condiciones pobres en nutrientes de los tumores reales. Este medio condicionado hizo que las células cancerosas crecieran más y resistieran varias quimioterapias comunes que actúan dañando el ADN o bloqueando su copia. Pruebas directas del daño en el ADN mostraron menos roturas cuando estaba presente el medio derivado de CAFs o proteínas matriciales purificadas. El colágeno, la fibronectina y la laminina redujeron cada una el daño en el ADN, lo que señala a la propia matriz, y no solo a pequeños nutrientes, como un protector clave.
Un sensor de estrés enlaza la matriz con la reparación del ADN
Para descubrir cómo se traducen las señales de la matriz dentro de las células cancerosas, los autores examinaron cientos de proteínas. Una destacó: una proteína de respuesta al estrés llamada NDRG1, especialmente en su forma activada por fosforilación. Las proteínas de la matriz y el medio condicionado por CAF aumentaron la actividad de NDRG1 mediante receptores de adhesión en la superficie celular llamados integrinas y una cadena de proteínas de señalización dentro de la célula. Bloquear esta cadena, en particular una familia de quinasas llamada SGK, impidió la activación de NDRG1. En muestras tumorales de pacientes y en modelos murinos, los niveles altos de NDRG1 fueron más prominentes cerca del estroma fibrótico y se asociaron con un crecimiento tumoral más rápido, mayor división celular y peor supervivencia tras la quimioterapia.
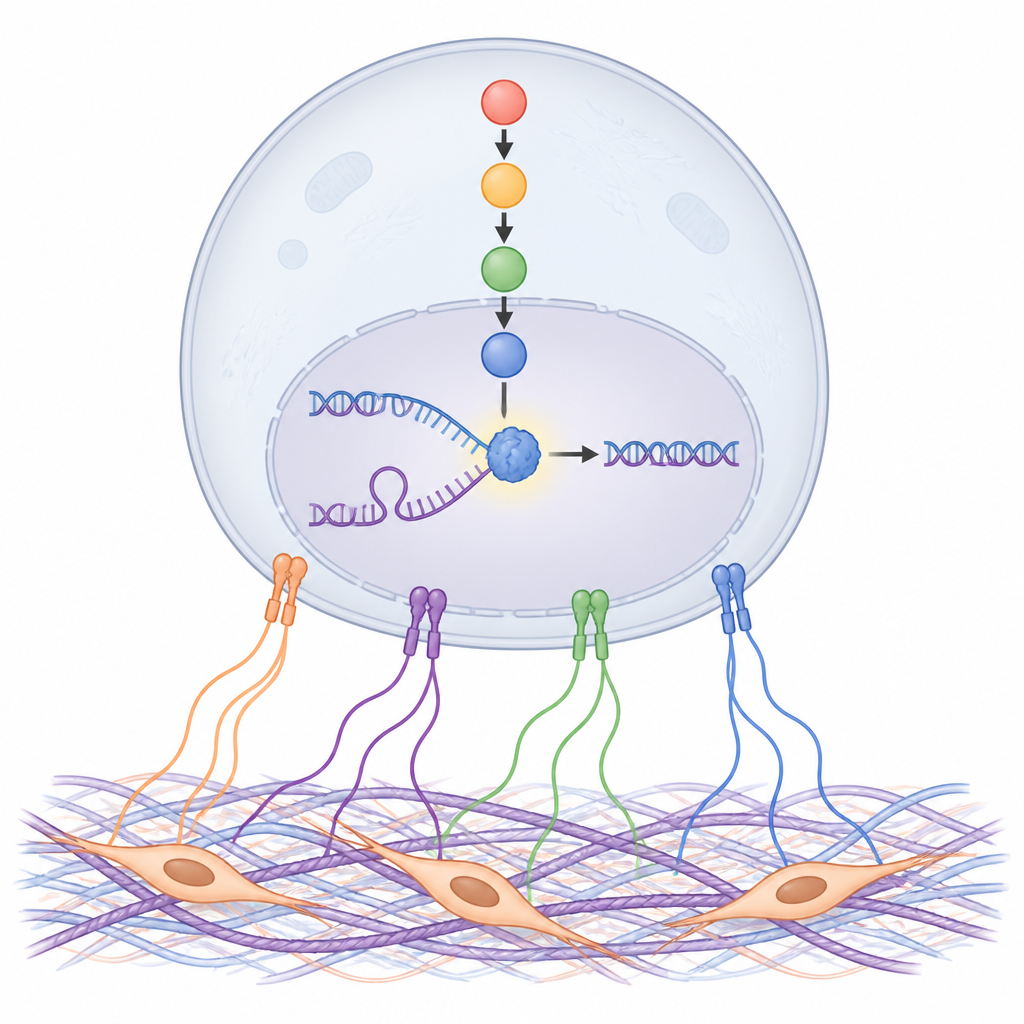
NDRG1 mantiene la copia del ADN en marcha
El estudio se centró después en lo que NDRG1 hace realmente sobre el ADN. Usando métodos sensibles para etiquetar y extraer ADN recién copiado, los investigadores encontraron NDRG1 directamente en los sitios donde se replica el ADN, especialmente cuando las horquillas de replicación se detienen por fármacos. Eliminar NDRG1, o bloquear su activación por SGK, ralentizó la copia del ADN, dificultó la reanudación de horquillas estancadas y aumentó el daño en el ADN, tanto en cultivos celulares como en ratones. Un componente específico de NDRG1, el aminoácido histidina en la posición 194, resultó esencial para este papel protector, lo que sugiere que la conformación de NDRG1 y su posible actividad tipo enzima son críticas para estabilizar las horquillas de replicación.
Eliminando los nudos perjudiciales ARN–ADN
Una causa frecuente de la detención de la copia del ADN es la formación de R-loops, pequeños enredos donde el ARN recién sintetizado se adhiere de nuevo a la plantilla de ADN. Los autores mostraron que las células sin NDRG1 o sin su activación acumulan estos híbridos ARN–ADN y experimentan más colisiones entre las máquinas que replican el ADN y las que transcriben genes. Cuando añadieron una enzima que elimina específicamente los R-loops, el movimiento de las horquillas y el daño en el ADN volvieron hacia la normalidad. Esto indica que NDRG1 ayuda a mantener la replicación en funcionamiento limitando los R-loops y aliviando estos conflictos entre transcripción y replicación.
Qué significa esto para tratamientos futuros
En términos sencillos, el tejido fibrótico que rodea los tumores pancreáticos envía señales que activan NDRG1 dentro de las células cancerosas, permitiéndoles reparar el daño en el ADN inducido por la quimioterapia y seguir dividiéndose. Los pacientes cuyos tumores expresan más NDRG1 tienden a responder peor a los fármacos convencionales que dañan el ADN. Apuntar a esta vía matriz–NDRG1, o combinar la quimioterapia con fármacos que debiliten la función reparadora de NDRG1, podría hacer a las células cancerosas más vulnerables sin aumentar la dosis de tratamientos tóxicos.
Cita: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Palabras clave: cáncer de páncreas, microambiente tumoral, reparación del ADN, fibroblastos asociados al cáncer, R-loops