Clear Sky Science · nl
Fibroblasten geassocieerd met kanker reguleren DNA-reparatie bij pancreaskanker via NDRG1-gemedieerde R-loopverwerking
Waarom de buurt van de tumor ertoe doet
Pancreaskanker is berucht moeilijk te behandelen, deels omdat de tumoren ingebed liggen in een taaie, vezelige omgeving van steuncellen en eiwitten. Deze studie laat zien dat dat littekenachtige weefsel meer doet dan alleen medicijnen tegenhouden. Het helpt actief kankercellen het DNA-schade veroorzaakt door chemotherapie te herstellen, waardoor tumoren kunnen overleven en terugkeren. Begrijpen van dit verborgen beschermingssysteem biedt nieuwe ideeën om behandelingen effectiever te maken.
Een hardnekkige kanker in een vijandige omgeving
Pancreasductaal adenocarcinoom groeit in een voedingsarme omgeving vol bindweefsel, bekend als stroma. Een groot deel van dit stroma wordt geproduceerd door kanker-geassocieerde fibroblasten, of CAFs, die veel extracellulaire matrixeiwitten afscheiden zoals collageen en laminine. Artsen weten al lang dat stroma-rijke tumoren resistent zijn tegen chemotherapie, maar de precieze redenen waren onduidelijk. De onderzoekers vroegen of signalen van deze fibroblasten en hun matrix direct veranderen hoe kankercellen reageren op DNA-schadigende geneesmiddelen.
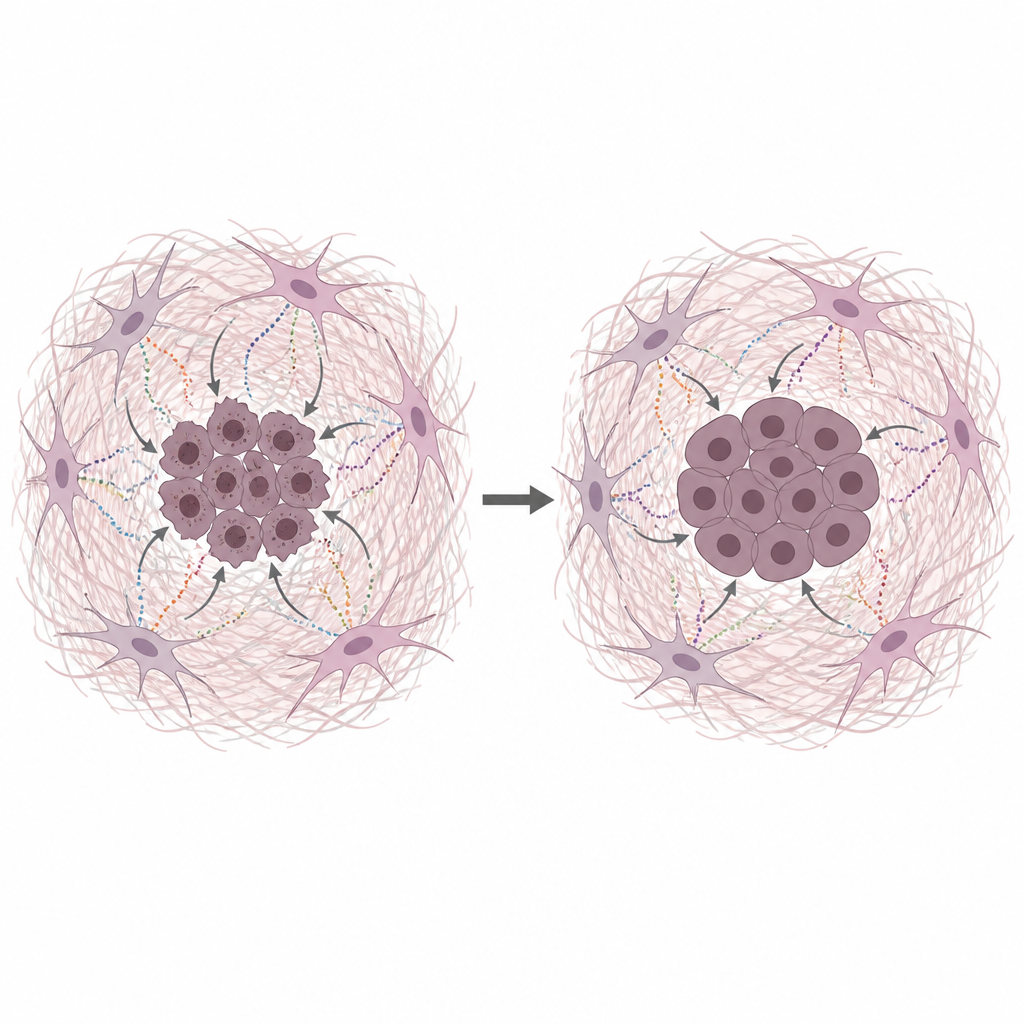
Secreties van fibroblasten beschermen kankerdna
Het team kweekte menselijke pancreaskankcellen samen met medium afkomstig van verhongerde CAFs, wat de voedingsarme omstandigheden in echte tumoren nabootst. Dit geconditioneerde medium liet kankercellen zowel beter groeien als bestand zijn tegen verschillende veelgebruikte chemotherapieën die werken door DNA te beschadigen of de replicatie stil te leggen. Directe tests op DNA-schade toonden minder breuken wanneer CAF-afgeleid medium of gezuiverde matrixeiwitten aanwezig waren. Collageen, fibronectine en laminine verminderden elk de DNA-schade, wat wijst op de matrix zelf, niet alleen op kleine voedingsstoffen, als een belangrijke beschermer.
Een stresssensor verbindt de matrix met DNA-reparatie
Om te achterhalen hoe matrixsignalen binnen kankercellen worden doorgegeven, namen de auteurs honderden eiwitten onder de loep. Eén eiwit sprong eruit: een stress-respons eiwit genaamd NDRG1, vooral in zijn geactiveerde, gefosforyleerde vorm. Matrixeiwitten en CAF-geconditioneerd medium verhoogden de NDRG1-activiteit via celoppervlakte-adhesiereceptoren genaamd integrines en een keten van signaalproteïnen binnen de cel. Het blokkeren van deze keten, met name een kinasefamilie genaamd SGK, verhinderde NDRG1-activatie. In tumormonsters van patiënten en muismodellen waren hoge NDRG1-niveaus het meest prominent nabij fibrotisch stroma en gekoppeld aan snellere tumorgroei, meer celdeling en slechtere overleving na chemotherapie.
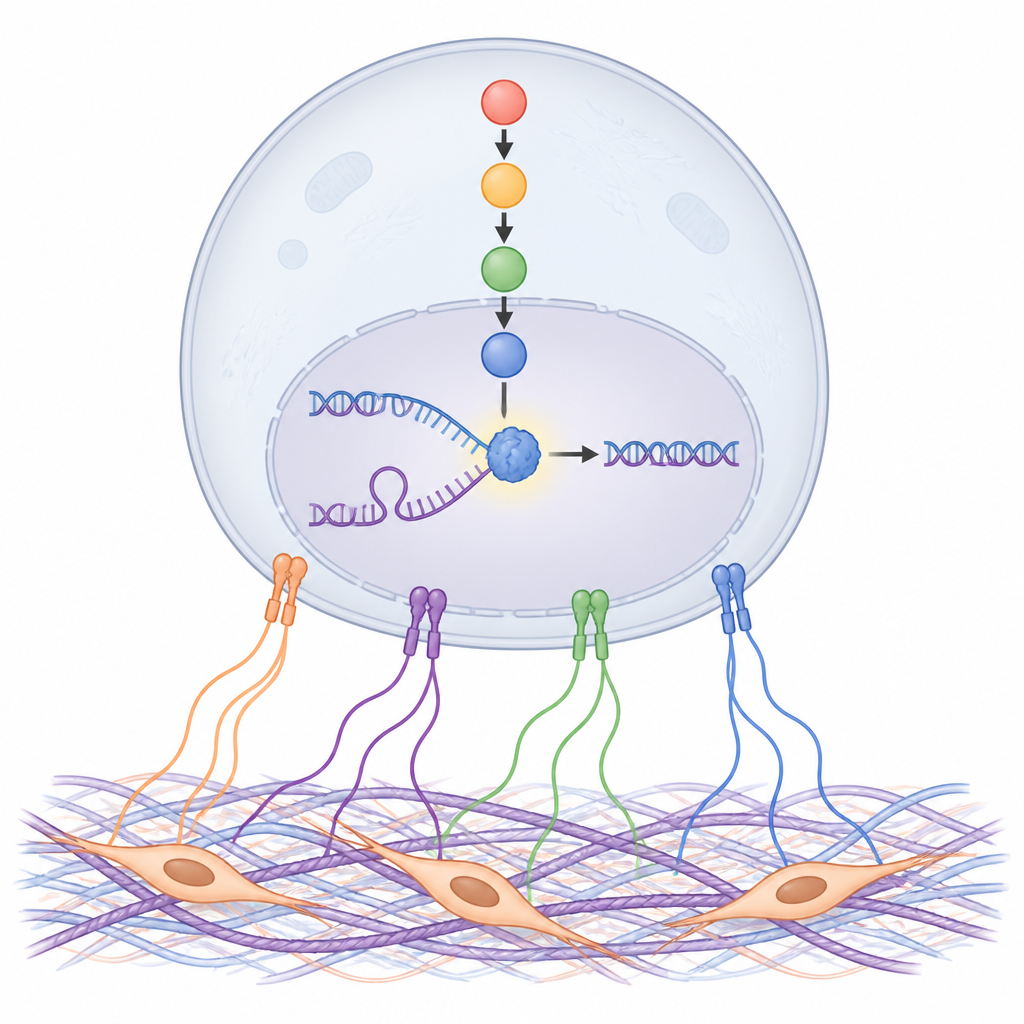
NDRG1 houdt DNA-replicatie op koers
De studie zoomde daarna in op wat NDRG1 daadwerkelijk doet met DNA. Met gevoelige methoden om nieuw gekopieerd DNA te labelen en uit te trekken, vonden de onderzoekers NDRG1 direct op de plaatsen waar DNA wordt gerepliceerd, vooral wanneer replicatievorken door geneesmiddelen worden stilgezet. Het wegnemen van NDRG1, of het blokkeren van zijn activatie door SGK, vertraagde DNA-replicatie, maakte het moeilijker voor gestopte vorken om te herstarten en verhoogde DNA-schade, zowel in kweek als in muismodellen. Een specifieke bouwsteen van NDRG1, het aminozuur histidine op positie 194, bleek essentieel voor deze beschermende rol, wat suggereert dat de vorm van NDRG1 en mogelijke enzymachtige activiteit cruciaal zijn voor het stabiliseren van replicatievorken.
Het opruimen van schadelijke RNA–DNA-knopen
Een veelvoorkomende oorzaak van stilgevallen DNA-replicatie is de vorming van R-loops, kleine knopen waarbij nieuwgemaakt RNA terug aan het DNA-sjabloon kleeft. De auteurs toonden aan dat cellen zonder NDRG1 of zonder zijn activatie deze RNA–DNA-hybriden ophopen en meer botsingen ervaren tussen de machines die DNA kopiëren en diegenen die genen aflezen. Wanneer zij een enzym toevoegden dat specifiek R-loops verwijdert, herstelde de voortgang van vorken en nam DNA-schade af naar meer normale niveaus. Dit geeft aan dat NDRG1 bijdraagt aan soepele replicatie door R-loops te beperken en deze transcriptie–replicatieconflicten te verminderen.
Wat dit betekent voor toekomstige behandelingen
In eenvoudige bewoordingen: het fibrotische weefsel rondom pancreastumoren zendt signalen uit die NDRG1 in kankercellen inschakelen, waardoor ze chemotherapie-geïnduceerde DNA-schade kunnen repareren en blijven delen. Patiënten van wie de tumoren meer NDRG1 tot expressie brengen, doen het doorgaans slechter bij standaard DNA-schadigende middelen. Het richten op deze matrix–NDRG1-route, of het combineren van chemotherapie met middelen die NDRG1’s reparatiefunctie verzwakken, zou kankercellen kwetsbaarder kunnen maken zonder de dosis van toxische behandelingen te verhogen.
Bronvermelding: Kozlova, N., Cruz, K.A., Ruzette, A.A. et al. Cancer-associated fibroblasts regulate DNA repair in pancreatic cancer through NDRG1-mediated R-loop processing. Nat Cell Biol 28, 986–999 (2026). https://doi.org/10.1038/s41556-026-01938-4
Trefwoorden: pancreaskanker, tumormicro-omgeving, DNA-reparatie, kanker-geassocieerde fibroblasten, R-loops