Clear Sky Science · zh
无义介导的mRNA降解在多能干细胞中保护端粒
细胞如何保护染色体末端的“帽子”
每次细胞分裂时,都必须复制并保护其DNA。我们的染色体末端由称为端粒的特殊结构覆盖,类似于鞋带上的塑料头,防止磨损和被误当作断裂而修复。本研究探讨了小鼠早期干细胞如何在一种主要保护蛋白缺失时,借助意想不到的备用系统——一种RNA“质量控制”通路——来保持这些端粒完整,揭示了RNA监视与染色体安全之间的惊人关联。
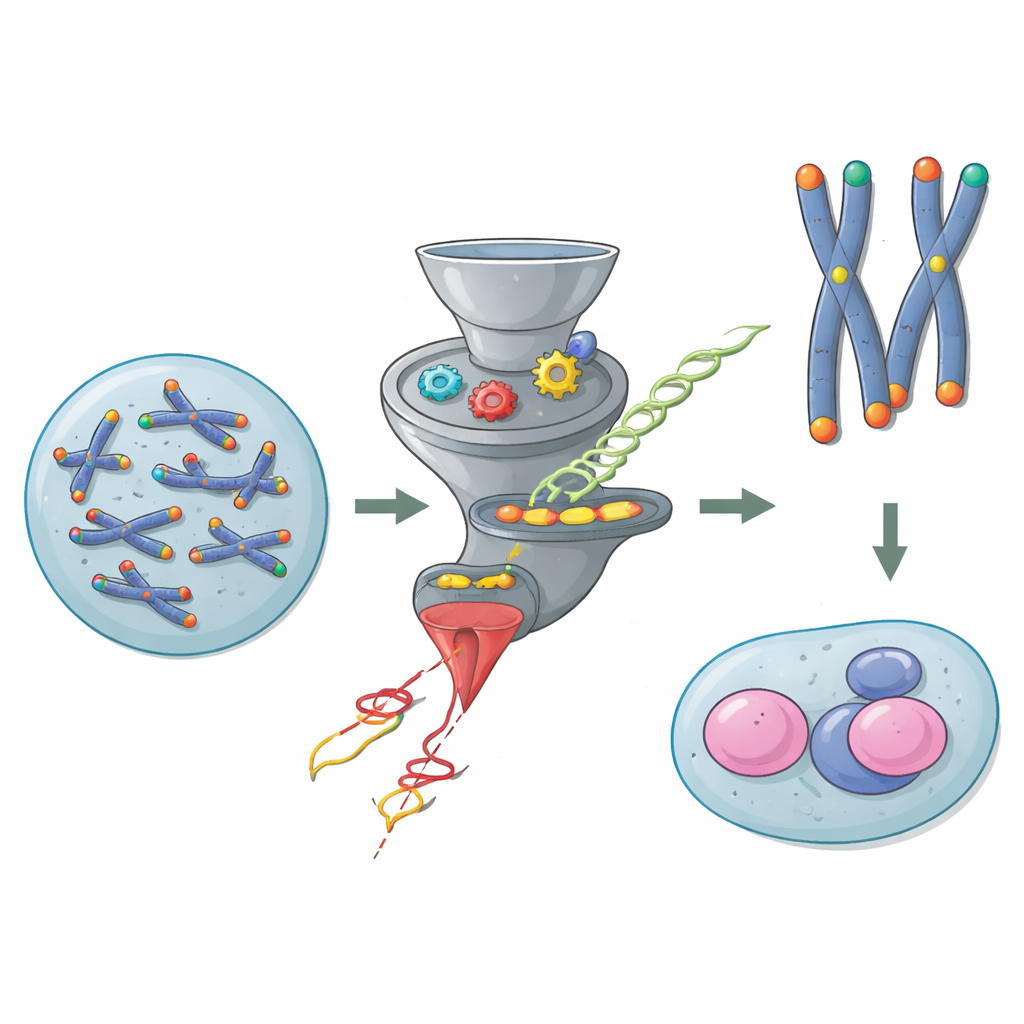
染色体末端的保护帽
染色体是很长的DNA分子,其末端需要保护,避免被误认作DNA断裂。端粒提供了这种保护,受一组称为Shelterin的蛋白帮助,这些蛋白覆盖末端并阻止危险的修复反应。在大多数体细胞中,一种名为TRF2的Shelterin蛋白至关重要:没有它,染色体末端会互相融合,DNA损伤反应会被触发,基因组变得不稳定。然而小鼠胚胎干细胞打破了这一规则。以往工作显示,这些幼稚细胞即便在去除TRF2后仍能存活并分裂,暗示存在某条隐藏的通路来守护它们的端粒。
全基因组筛选寻找隐藏的帮手
为了发现这一隐藏的保障机制,研究者使用了强大的遗传筛选。他们在小鼠胚胎干细胞中使Trf2基因失能,然后用CRISPR–Cas9逐一破坏数千个其他基因。如果丢失第二个基因会导致已经缺失TRF2的细胞突然死亡,那么该第二基因就被标记为“合成致死”的伙伴——表明它在补偿TRF2丢失方面发挥作用。筛选回收到了预期的端粒因子,但也突出了若干看似无关通路的组分:无义介导的mRNA降解(NMD),这是一套以清除含有过早终止信号的有缺陷RNA为人所知的系统。
当RNA清理失败时,染色体末端会破裂
团队随后测试了在缺乏TRF2的干细胞中去除NMD因子会发生什么。单独缺失TRF2或单独缺失NMD都导致的端粒损伤很少:染色体末端看起来大体正常,细胞继续生长。但当TRF2和NMD同时被破坏时,情况发生了显著变化。DNA损伤标志物在端粒处聚集,染色体经常发生末端对末端的融合。这些融合染色体伴随明显的生长缺陷、细胞死亡增加和细胞周期停滞,尽管细胞仍保留核心的干细胞特征。急性化学抑制或基于降解子(degron)的NMD关闭也产生了相同的端粒融合表型,排除了长期适应的可能,证实持续的NMD活性对保护缺少TRF2的端粒是直接必需的。
有害的截短蛋白削弱端粒守护者
进一步深入研究时,研究者检查了这些干细胞中哪些RNA信息由NMD控制。他们发现Trf1基因(编码另一个端粒结合蛋白TRF1)在NMD受损时产生异常的剪接变体。这种改变的RNA跳过了一个内部片段并携带过早终止密码子,导致生成一种缺失DNA结合末端的截短TRF1蛋白,但该截短蛋白仍能与正常TRF1配对。在NMD缺陷细胞中,这种截短形式积累并将全长TRF1从端粒处拉走。实验证明,在这些条件下,TRF1在染色体末端的占有明显下降,仅让细胞表达该截短蛋白就足以触发端粒融合,尤其是在同时缺失TRF2时。相反,在NMD缺陷细胞中提高全长TRF1水平则在很大程度上恢复了端粒保护,强调了端粒上有效TRF1丧失是关键问题。
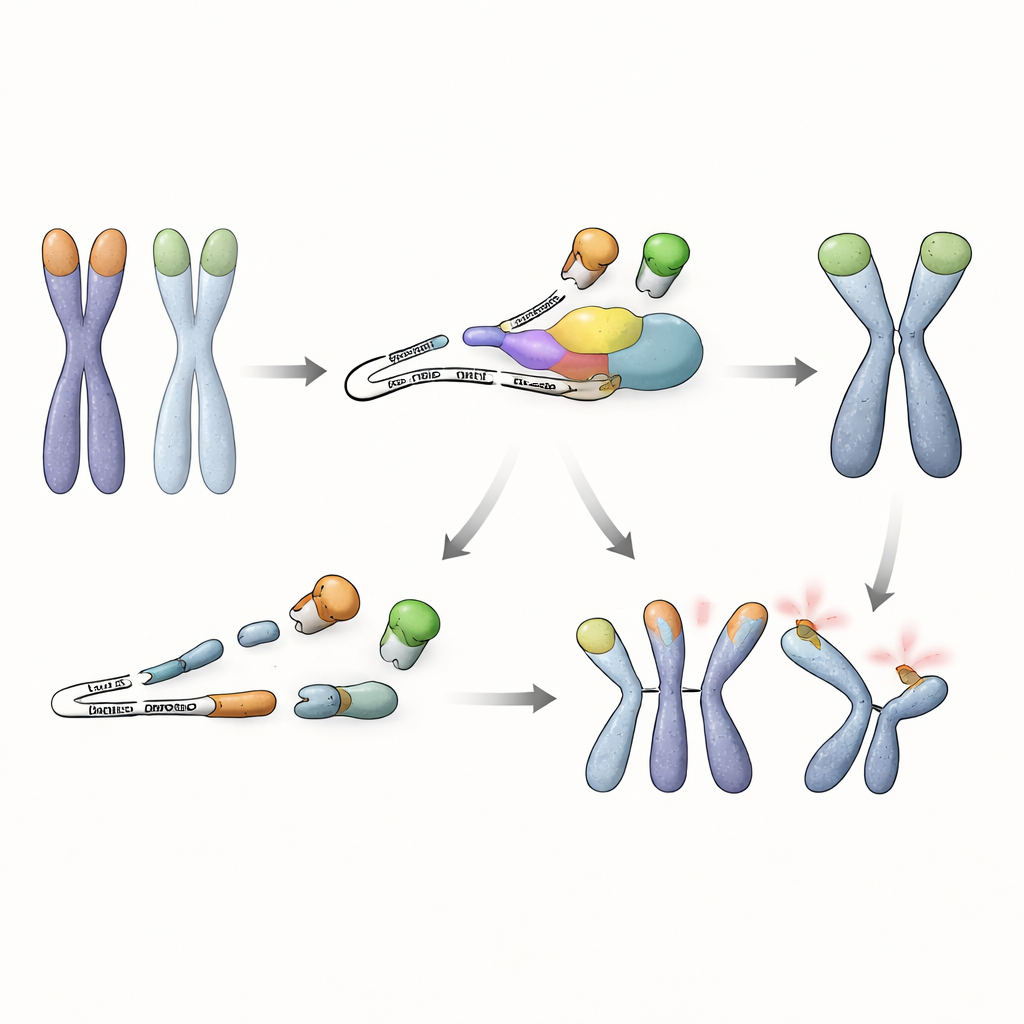
RNA监视与基因组安全之间的新联系
综上所述,这项工作表明,胚胎干细胞依赖的不仅是结合DNA末端的蛋白来保护染色体。它们还需要一条RNA质量控制通路,以防止有害的截短TRF1蛋白积累并取代其保护性的全长同源物。只要NMD活跃,这类有缺陷的RNA就会被迅速降解,TRF1维持在端粒上,干细胞就能在缺失TRF2的情况下避免灾难性的染色体融合。这一发现揭示了早期干细胞如何将RNA监视与端粒保护联系起来的先前未识别策略,凸显了多层控制如何协同以在生命最早期阶段维护基因组稳定性。
引用: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
关键词: 端粒, 多能干细胞, RNA质量控制, 无义介导的降解, 基因组稳定性