Clear Sky Science · de
Die nonsense-vermittelte mRNA‑Abbau schützt Telomere in pluripotenten Stammzellen
Wie Zellen ihre Chromosomen‑Kappen schützen
Jedes Mal, wenn sich eine Zelle teilt, muss sie ihre DNA kopieren und schützen. Die Enden unserer Chromosomen sind durch spezielle Strukturen, sogenannte Telomere, gekappt; sie wirken wie Plastikspitzen an Schnürsenkeln und verhindern Ausfransen sowie fehlerhafte Reparaturen. Diese Studie untersucht, wie frühe Maus‑Stammzellen ein unerwartetes Backup‑System — einen RNA‑„Qualitätskontroll“‑Weg — nutzen, um diese Kappen intakt zu halten, wenn ein wichtiges Schutzprotein fehlt, und zeigt damit eine überraschende Verbindung zwischen RNA‑Überwachung und Chromosomen‑Sicherheit.
Die schützenden Kappen an den Chromosomenenden
Chromosomen sind lange DNA‑Moleküle, die an ihren Spitzen geschützt werden müssen, damit sie nicht mit gebrochener DNA verwechselt werden. Telomere bieten diesen Schutz, unterstützt von einer Proteingruppe namens Shelterin, die die Enden umhüllt und gefährliche Reparaturreaktionen blockiert. In den meisten Körperzellen ist ein Shelterin‑Protein namens TRF2 entscheidend: Fehlt es, fusionieren Chromosomenenden, DNA‑Schadensantworten laufen an und Genome werden instabil. Maus‑embryonale Stammzellen folgen dieser Regel jedoch nicht. Frühere Arbeiten zeigten, dass diese jungen Zellen überleben und sich teilen können, selbst wenn TRF2 entfernt ist, was darauf hindeutet, dass ein verborgener Weg einspringt, um ihre Telomere zu schützen.
Eine genomweite Suche nach einem verborgenen Helfer
Um diese versteckte Schutzfunktion aufzuspüren, nutzten die Forschenden einen leistungsfähigen genetischen Screen. Sie inaktivierten das Trf2‑Gen in Maus‑embryonalen Stammzellen und setzten dann CRISPR–Cas9 ein, um tausende anderer Gene nacheinander zu stören. Wenn der Verlust eines zweiten Gens die Zellen, denen bereits TRF2 fehlte, plötzlich abtötete, wurde dieses zweite Gen als Partner in „synthetischer Letalität“ identifiziert — ein Hinweis darauf, dass es den Verlust von TRF2 kompensiert. Der Screen förderte erwartete Telomer‑Faktoren zutage, hob aber auch mehrere Komponenten eines scheinbar nicht verwandten Wegs hervor: den nonsense‑vermittelten mRNA‑Abbau (NMD), ein System, das vor allem dafür bekannt ist, fehlerhafte RNA‑Botschaften mit vorzeitigen Stoppsignalen zu eliminieren.
Wenn die RNA‑Bereinigung ausfällt, brechen Chromosomenenden
Das Team prüfte dann, was geschieht, wenn NMD‑Faktoren in TRF2‑defizienten Stammzellen entfernt werden. Weder der alleinige Verlust von TRF2 noch der alleinige Ausfall von NMD verursachte starke Telomer‑Schäden: Die Chromosomenenden wirkten größtenteils normal und die Zellen teilten sich weiter. Wurden jedoch TRF2 und NMD gemeinsam gestört, änderte sich das Bild dramatisch. Marker für DNA‑Schäden häuften sich spezifisch an Telomeren, und Chromosomen fusionierten häufig Ende‑zu‑Ende. Diese Fusionen gingen mit starken Wachstumsdefekten, vermehrtem Zelltod und blockiertem Zellzyklus einher, obwohl die Zellen zentrale Stammzell‑Eigenschaften beibehielten. Eine akute chemische oder degronbasierte Abschaltung von NMD erzeugte dasselbe Telomer‑Fusionsphänomen, wodurch eine langfristige Anpassung ausgeschlossen und bestätigt wurde, dass fortlaufende NMD‑Aktivität direkt erforderlich ist, um TRF2‑freie Telomere zu schützen.
Ein schädliches, verkürztes Protein untergräbt Telomer‑Wächter
Bei tieferer Analyse untersuchten die Forschenden, welche RNA‑Botschaften in diesen Stammzellen durch NMD kontrolliert werden. Sie fanden, dass das Trf1‑Gen, das ein weiteres telomerbindendes Protein TRF1 kodiert, eine abnorme Spleißvariante produziert, wenn NMD gestört ist. Diese veränderte RNA überspringt ein internes Segment und enthält ein vorzeitiges Stoppsignal, was zur Herstellung eines verkürzten TRF1‑Proteins führt, dem die DNA‑Bindungs‑Spitze fehlt, das sich aber noch mit normalem TRF1 paaren kann. In NMD‑defizienten Zellen reichert sich diese verkürzte Variante an und verdrängt das volle TRF1 von den Telomeren. Experimente zeigten, dass die TRF1‑Belegung an Chromosomenenden unter diesen Bedingungen stark abnimmt, und allein das erzwungene Herstellen des verkürzten Proteins genügte, um Telomer‑Fusionen auszulösen — besonders wenn auch TRF2 fehlte. Umgekehrt stellte eine Erhöhung der vollen TRF1‑Menge in NMD‑defekten Zellen den Telomerenschutz größtenteils wieder her, was unterstreicht, dass der Verlust effektiven TRF1 an Telomeren das zentrale Problem ist.
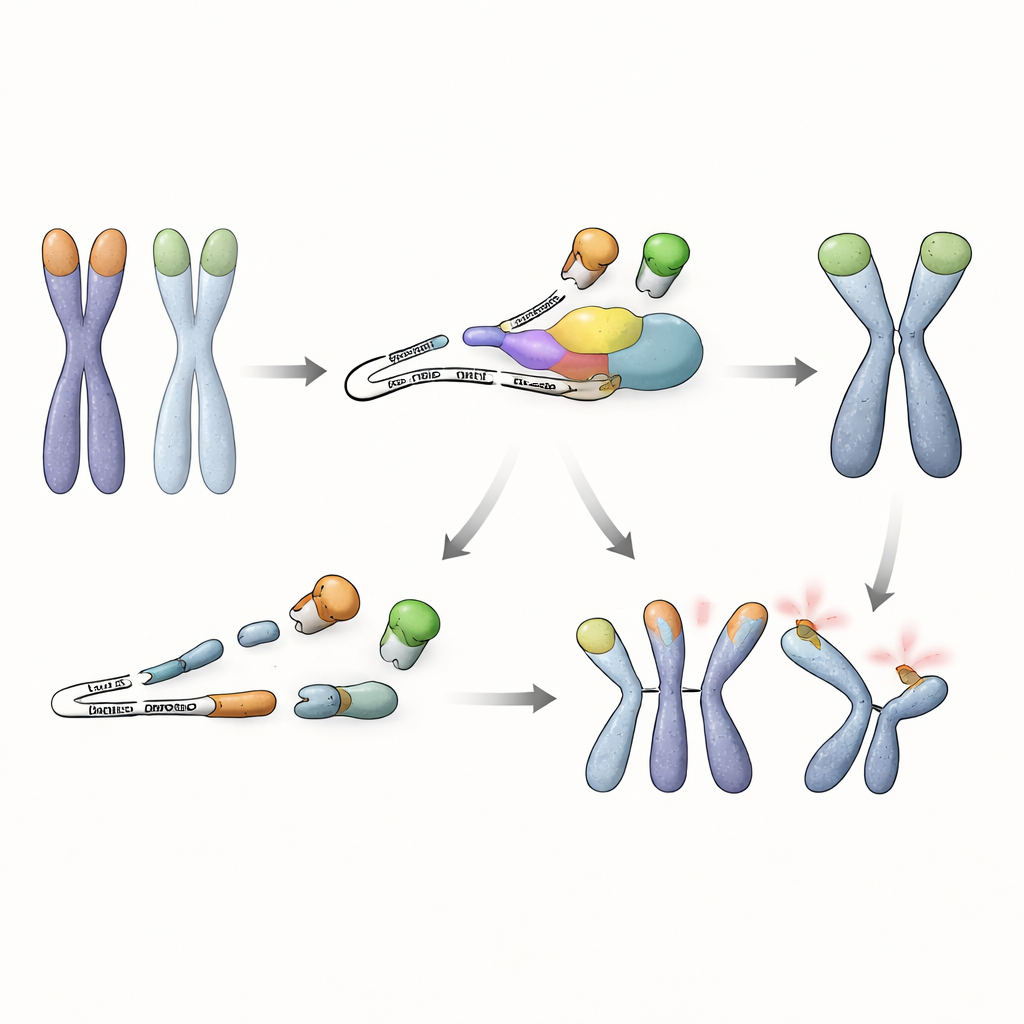
Eine neue Verbindung zwischen RNA‑Überwachung und Genomsicherheit
Zusammengefasst zeigt die Arbeit, dass embryonale Stammzellen sich nicht nur auf DNA‑End‑bindende Proteine verlassen, um ihre Chromosomen zu schützen. Sie benötigen zusätzlich einen RNA‑Qualitätskontrollweg, um die Anhäufung eines schädlichen, verkürzten TRF1‑Proteins zu verhindern, das sein schützendes Vollformat verdrängt. Solange NMD aktiv ist, wird diese fehlerhafte RNA schnell abgebaut, TRF1 bleibt an den Telomeren, und Stammzellen können den Verlust von TRF2 tolerieren, ohne katastrophale Chromosomenfusionen zu erleiden. Diese Entdeckung offenbart eine zuvor unerkannte Strategie, mit der frühe Stammzellen RNA‑Überwachung mit Telomer‑Schutz verknüpfen, und hebt hervor, wie mehrere Kontrollebenen zusammenwirken, um die Genomstabilität in den frühesten Lebensstadien zu bewahren.
Zitation: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Schlüsselwörter: Telomere, pluripotente Stammzellen, RNA‑Qualitätskontrolle, nonsense-vermittelte Elimination, Genomstabilität