Clear Sky Science · pl
Mechanizm niszczenia mRNA z przedwczesnym końcem chroni telomery w komórkach pluripotentnych
Jak komórki chronią nasadki chromosomów
Za każdym razem, gdy komórka się dzieli, musi skopiować i zabezpieczyć swoje DNA. Końce naszych chromosomów są zakończone przez specjalne struktury zwane telomerami, które działają jak plastikowe zakończenia sznurówek, zapobiegając strzępieniu i błędnym naprawom. W badaniu tym pokazano, jak wczesne mysie komórki macierzyste wykorzystują niespodziewany system zapasowy — ścieżkę „kontroli jakości” RNA — by utrzymać te nasadki w stanie nienaruszonym, gdy brak jest kluczowego białka ochronnego, odkrywając zaskakujące powiązanie między nadzorem RNA a bezpieczeństwem chromosomów.
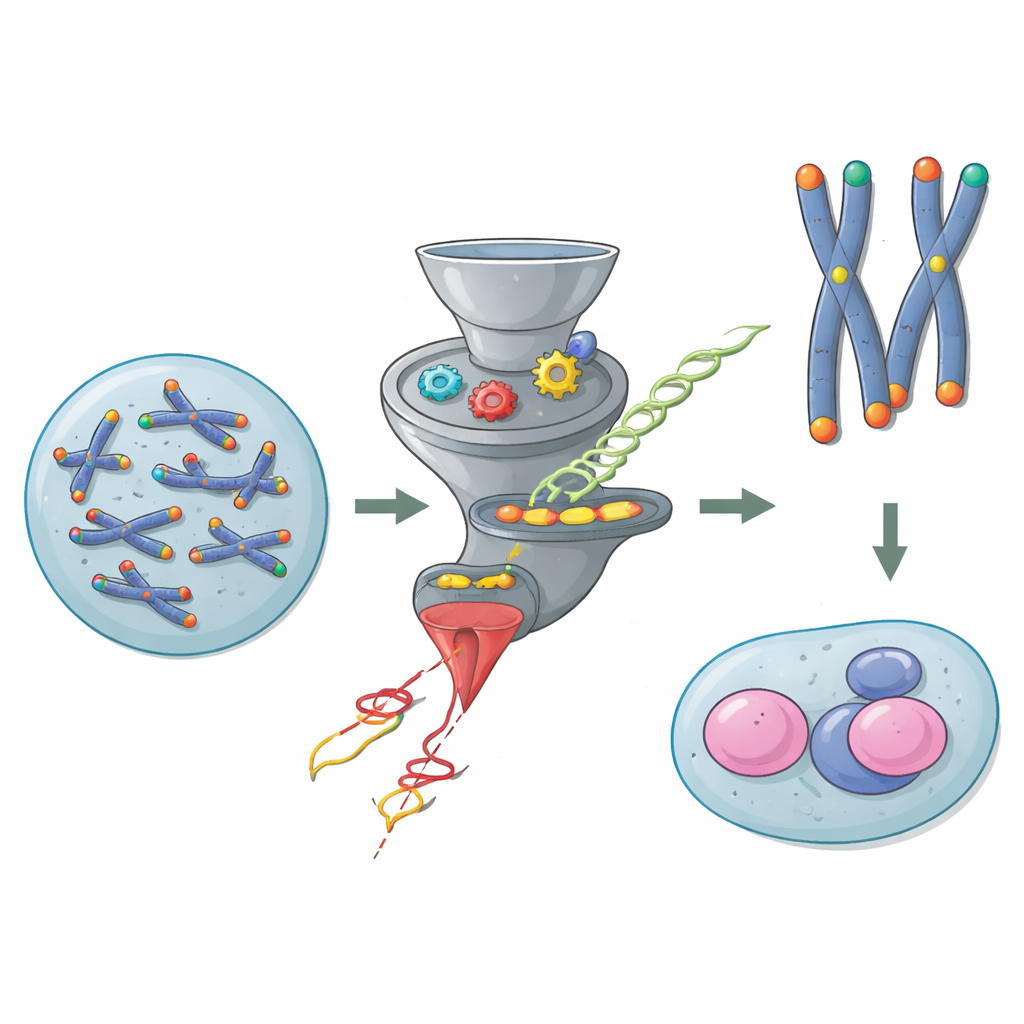
Ochronne nasadki na końcach chromosomów
Chromosomy to długie cząsteczki DNA, które wymagają ochrony na końcach, by nie zostały pomylone z pękniętym DNA. Telomery zapewniają tę ochronę, przy wsparciu grupy białek znanych jako Shelterin, które okrywają końce i blokują niebezpieczne reakcje naprawcze. W większości komórek somatycznych jedno białko Shelterin, zwane TRF2, jest niezbędne: bez niego końce chromosomów zlewają się ze sobą, uruchamiają się odpowiedzi na uszkodzenia DNA, a genom staje się niestabilny. Jednak mysie embrionalne komórki macierzyste łamią tę zasadę. Wcześniejsze prace wykazały, że te młode komórki mogą przetrwać i dzielić się nawet po usunięciu TRF2, co sugeruje, że istnieje ukryta ścieżka zastępcza chroniąca ich telomery.
Poszukiwanie ukrytego pomocnika w całym genomie
Aby odkryć tego ukrytego strażnika, badacze wykorzystali potężny ekran genetyczny. Wyłączyli gen Trf2 w mysich embrionalnych komórkach macierzystych, a następnie użyli CRISPR–Cas9 do zakłócenia tysięcy innych genów pojedynczo. Jeśli utrata drugiego genu nagle zabijała komórki już pozbawione TRF2, drugi gen był oznaczany jako partner w „syntetycznej śmiertelności” — sygnał, że pomaga on kompensować brak TRF2. Ekran wyłonił oczekiwane czynniki telomerowe, ale także uwypuklił kilka składników wydawałoby się niepowiązanej ścieżki: mechanizmu niszczenia mRNA zawierających przedwczesne kodony stop (nonsense-mediated mRNA decay, NMD), systemu znanego głównie z eliminowania wadliwych komunikatów RNA z wczesnymi sygnałami stop.
Kiedy porządek RNA zawodzi, końce chromosomów pękają
Zespół następnie zbadał, co się dzieje, gdy czynniki NMD są usuwane w komórkach macierzystych pozbawionych TRF2. Samo usunięcie TRF2 lub sam brak NMD powodowały niewielkie uszkodzenia telomerów: końce chromosomów wyglądały przeważnie normalnie, a komórki nadal się dzieliły. Jednak gdy TRF2 i NMD zostały jednocześnie zakłócone, sytuacja zmieniła się dramatycznie. Markery uszkodzeń DNA gromadziły się specyficznie przy telomerach, a chromosomy często się ze sobą zlewały. Te zlane chromosomy wiązały się z silnymi defektami wzrostu, zwiększoną śmiercią komórek oraz zatrzymaniem cyklu komórkowego, mimo że komórki zachowywały podstawowe cechy macierzyste. Nagłe chemiczne lub degronowe wyłączenie NMD dało tę samą fenotypową fuzję telomerów, wykluczając długoterminową adaptację i potwierdzając, że ciągła aktywność NMD jest bezpośrednio wymagana do ochrony telomerów pozbawionych TRF2.
Szkodliwe skrócone białko podważa strażników telomerów
Pogłębiając badania, naukowcy sprawdzili, które komunikaty RNA są kontrolowane przez NMD w tych komórkach macierzystych. Odkryli, że gen Trf1, kodujący inne białko wiążące telomery — TRF1, produkuje nieprawidłowy wariant splicingowy, gdy NMD jest upośledzone. Zmienione RNA pomija wewnętrzny fragment i zawiera przedwczesny kodon stop, co prowadzi do powstania skróconego białka TRF1 pozbawionego końcówki wiążącej DNA, ale wciąż zdolnego do parowania z normalnym TRF1. W komórkach defektywnych pod względem NMD ta zredukowana forma się akumuluje i odciąga pełnej długości TRF1 od telomerów. Doświadczenia wykazały, że zajętość TRF1 na końcach chromosomów spada gwałtownie w tych warunkach, a wymuszone wytwarzanie skróconego białka wystarczało, by wywołać fuzje telomerów, szczególnie gdy brakowało również TRF2. Z drugiej strony, zwiększenie poziomów pełnej długości TRF1 w komórkach z zaburzoną NMD w dużej mierze przywracało ochronę telomerów, podkreślając, że kluczowym problemem jest utrata efektywnego TRF1 na telomerach.
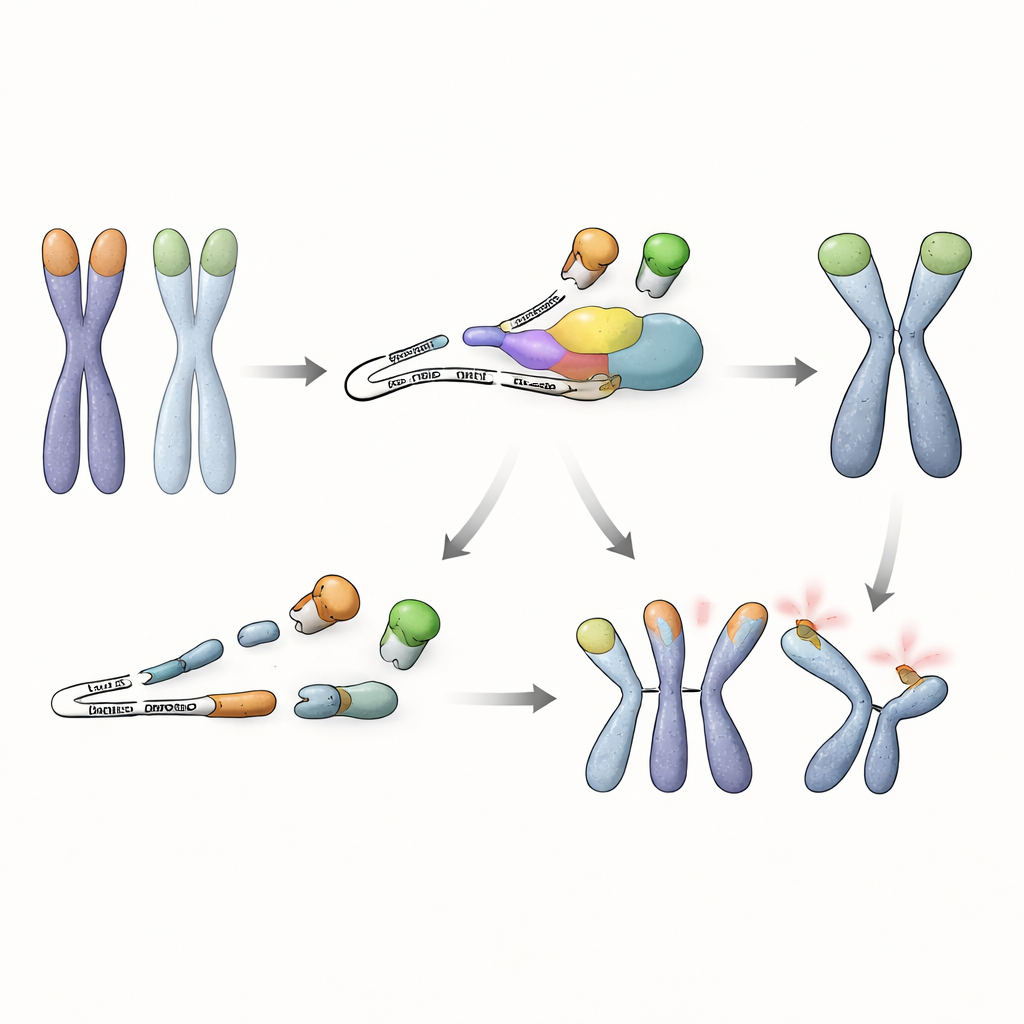
Nowe powiązanie nadzoru RNA z ochroną genomu
Podsumowując, praca ujawnia, że komórki embrionalne macierzyste polegają nie tylko na białkach wiążących końce DNA do ochrony swoich chromosomów. Potrzebują także ścieżki kontroli jakości RNA, aby zapobiec nagromadzeniu szkodliwego, skróconego białka TRF1, które wypiera funkcjonalny wariant o pełnej długości. Dopóki NMD działa, wadliwe RNA jest szybko niszczone, TRF1 pozostaje na telomerach, a komórki macierzyste mogą tolerować utratę TRF2 bez katastrofalnych fuzji chromosomów. Odkrycie to ujawnia wcześniej nieznaną strategię, dzięki której wczesne komórki macierzyste łączą nadzór RNA z ochroną telomerów, podkreślając, jak wielowarstwowe mechanizmy współpracują, by zachować stabilność genomu na najwcześniejszych etapach życia.
Cytowanie: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Słowa kluczowe: telomery, komórki pluripotentne, kontrola jakości RNA, nonsense-mediated decay, stabilność genomu