Clear Sky Science · tr
Sağlıksız mRNA bozunumu, pluripotent kök hücrelerde telomerleri koruyor
Hücreler kromozom uçlarını nasıl güvende tutar
Bir hücre her bölündüğünde DNA’sını kopyalamalı ve korumalıdır. Kromozomlarımızın uçları, püskül oluşumunu ve yanlış onarım girişimlerini önleyen ayakkabı bağcığı uçlarındaki plastik kapaklara benzeyen telomer adlı özel yapılarla kaplanır. Bu çalışma, fare embriyonik kök hücrelerinin büyük bir koruyucu protein eksik olduğunda telomerleri sağlam tutmak için beklenmedik bir yedek sistem—bir RNA “kalite kontrol” yolu—kullandığını inceliyor ve RNA gözetimi ile kromozom güvenliği arasında şaşırtıcı bir bağlantı ortaya koyuyor.
Kromozom uçlarındaki koruyucu kapaklar
Kromozomlar uzun DNA molekülleridir ve uçlarının kırık DNA ile karışmaması için korunması gerekir. Telomerler bu korumayı sağlar; uçları kaplayan ve tehlikeli onarım reaksiyonlarını engelleyen Shelterin adlı bir protein grubunun yardımıyla işler. Çoğu vücut hücresinde TRF2 adlı bir Shelterin proteini hayati önemdedir: yokluğunda kromozom uçları birbirine kaynaşır, DNA hasar tepkileri ortaya çıkar ve genomlar kararsız hale gelir. Yine de fare embriyonik kök hücreleri bu kuralı bozuyor. Önceki çalışmalar, bu genç hücrelerin TRF2 ortadan kaldırıldığında bile hayatta kalıp bölünebildiğini gösterdi; bu da telomerlerini korumak için bilinmeyen bir yolun devreye girdiğine işaret ediyordu.
Gizli bir yardımcı için genom çapında arama
Bu gizli korumayı ortaya çıkarmak için araştırmacılar güçlü bir genetik ekran kullandılar. Fare embriyonik kök hücrelerinde Trf2 genini işlevsizleştirip ardından CRISPR–Cas9 ile binlerce başka geni tek tek bozarak tarama yaptılar. İkinci bir genin yokluğu, zaten TRF2 eksik olan hücreleri ani ölümle karşılaştırıyorsa, o gen “sentetik ölüm” işaretçisi olarak işaretlendi—yani TRF2 kaybına karşı telafi edici bir yardımı olduğunu gösterir. Tarama beklenen telomer faktörlerini yakaladı ama aynı zamanda görünüşte alakasız bir yolun birkaç bileşenini de öne çıkardı: sağlıksız mRNA bozunumu (NMD), erken durdurma sinyali içeren kusurlu RNA mesajlarını ortadan kaldırmasıyla bilinen bir sistem.
RNA temizliği başarısız olunca kromozom uçları kopuyor
Araştırma ekibi sonra TRF2 eksik kök hücrelerinde NMD faktörleri kaldırıldığında ne olduğunu test etti. Ne TRF2 eksikliği ne de tek başına NMD kaybı çok telomer hasarına neden oldu: kromozom uçları büyük ölçüde normal görünüyordu ve hücreler büyümeyi sürdürdü. Ancak TRF2 ve NMD birlikte bozulduğunda tablo dramatik biçimde değişti. DNA hasar belirteçleri özellikle telomerlerde birikti ve kromozomlar sıkça uçtan uca kaynaştı. Bu kaynaşmış kromozomlar güçlü büyüme kusurları, artmış hücre ölümü ve hücre döngüsü ilerlemesinde tıkanma ile çakıştı; bunlara rağmen hücreler temel kök hücre özelliklerini koruyordu. NMD’nin kimyasal veya degron temelli ani kapatılması da aynı telomer kaynaşma fenotipini üretti; bu, uzun süreli adaptasyonu dışladı ve sürekli NMD aktivitesinin TRF2’siz telomerleri güvenli tutmak için doğrudan gerekli olduğunu doğruladı.
Zararlı kısalmış bir protein telomer koruyucularını zayıflatıyor
Daha derine inen araştırmacılar, bu kök hücrelerde NMD tarafından hangi RNA mesajlarının kontrol edildiğini incelediler. NMD bozulduğunda başka bir telomer-bağlayıcı protein olan TRF1’i kodlayan Trf1 geninin anormal bir eşleme varyantı ürettiğini buldular. Bu değişmiş RNA, iç bir segmenti atlıyor ve erken bir durdurma sinyali taşıyor; bunun sonucu DNA-bağlayıcı ucunu kaybetmiş ancak normal TRF1 ile eşleşebilen kısalmış bir TRF1 proteini üretildi. NMD yetersiz hücrelerde bu kırpılmış versiyon birikiyor ve tam boy TRF1’i telomerlerden uzaklaştırıyordu. Deneyler, bu koşullar altında TRF1’in kromozom uçlarındaki varlığının keskin biçimde düştüğünü gösterdi ve hücreleri zorla bu kırpılmış proteini üretmeye zorlamak, özellikle TRF2 de eksikse, telomer kaynaşmalarını tetikleyecek kadar yeterliydi. Tersine, NMD kusurlu hücrelerde tam boy TRF1 düzeylerini artırmak telomer korumasını büyük ölçüde geri getirdi; bu da telomerlerde etkili TRF1 kaybının temel sorun olduğunu vurguluyor.
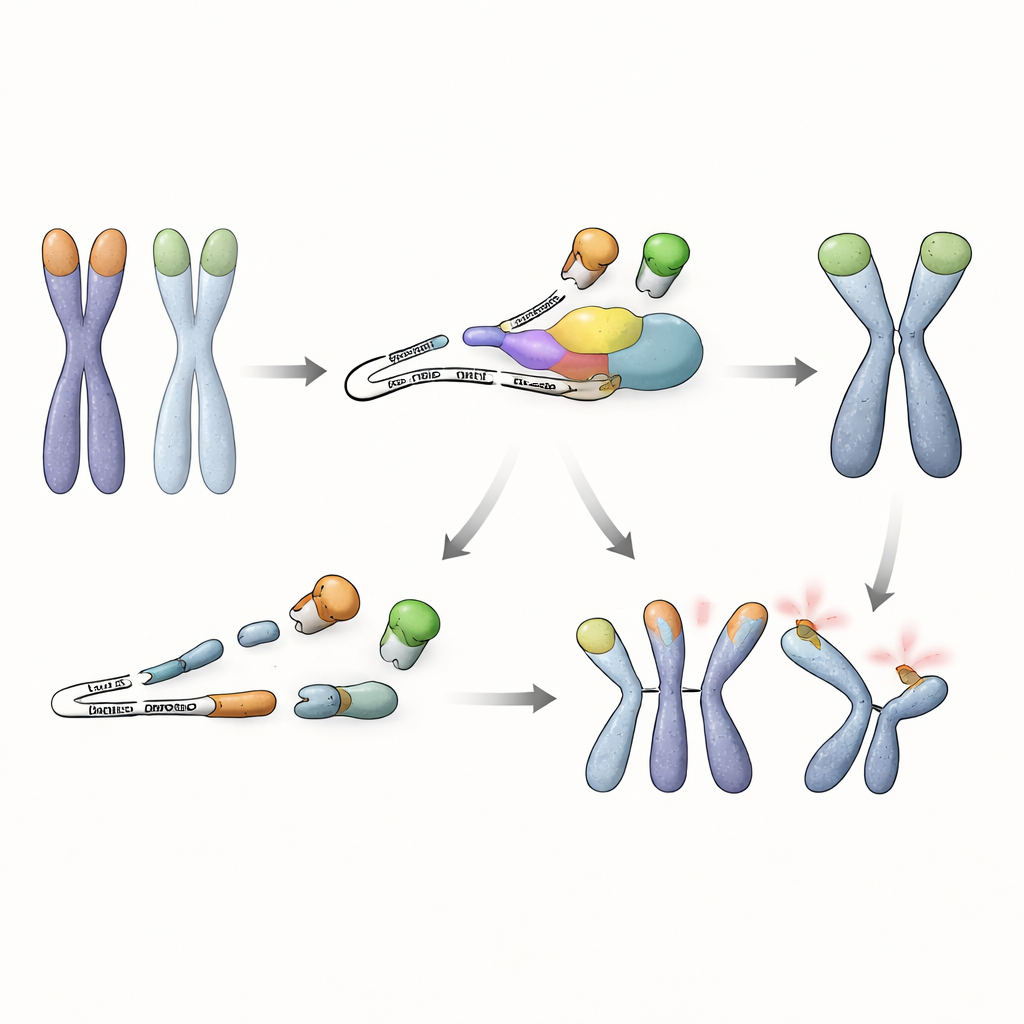
RNA gözetimi ile genom güvenliği arasında yeni bir bağ
Bir arada ele alındığında bu çalışma, embriyonik kök hücrelerinin kromozomlarını korumak için yalnızca DNA ucu bağlayıcı proteinlere dayanmadığını ortaya koyuyor. Ayrıca, koruyucu tam boy eşini yerinden eden zararlı, kısalmış bir TRF1 proteininin birikmesini önlemek için bir RNA kalite kontrol yoluna ihtiyaçları var. NMD aktif olduğu sürece bu hatalı RNA hızla yok ediliyor, TRF1 telomerlerde kalıyor ve kök hücreleri TRF2 kaybını yıkıcı kromozom kaynaşmaları olmadan tolere edebiliyor. Bu keşif, erken kök hücrelerin RNA gözetimini telomer korumasına bağladığı daha önce tanınmamış bir stratejiyi ortaya koyuyor ve yaşamın en erken aşamalarında genom kararlılığını korumak için birden çok kontrol katmanının nasıl işbirliği yaptığını vurguluyor.
Atıf: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Anahtar kelimeler: telomerler, pluripotent kök hücreler, RNA kalite kontrolü, sağlıksız mRNA bozunumu, genom kararlılığı