Clear Sky Science · ar
تحلل الرنا الرسول غير الحتمي يحمي التيلوميرات في الخلايا الجذعية متعددة القدرات
كيف تحافظ الخلايا على أغطية كروموسوماتها
في كل مرة تنقسم فيها الخلية، يجب عليها نسخ وإبقاء حمضها النووي محميًا. تُغطَّى نهايات كروموسوماتنا بهياكل خاصة تُدعى التيلوميرات تعمل مثل أطراف البلاستيك في أربطة الحذاء، فتمنع التفكك والإصلاح الخاطئ. تستكشف هذه الدراسة كيف تستخدم خلايا جذعية ماوسية مبكرة نظامًا احتياطيًا غير متوقع—ممر لمراقبة جودة الرنا—للحفاظ على هذه الأغطية عندما يغيب بروتين واقٍ رئيسي، كاشفةً عن صلة مفاجئة بين مراقبة الرنا وسلامة الكروموسوم.
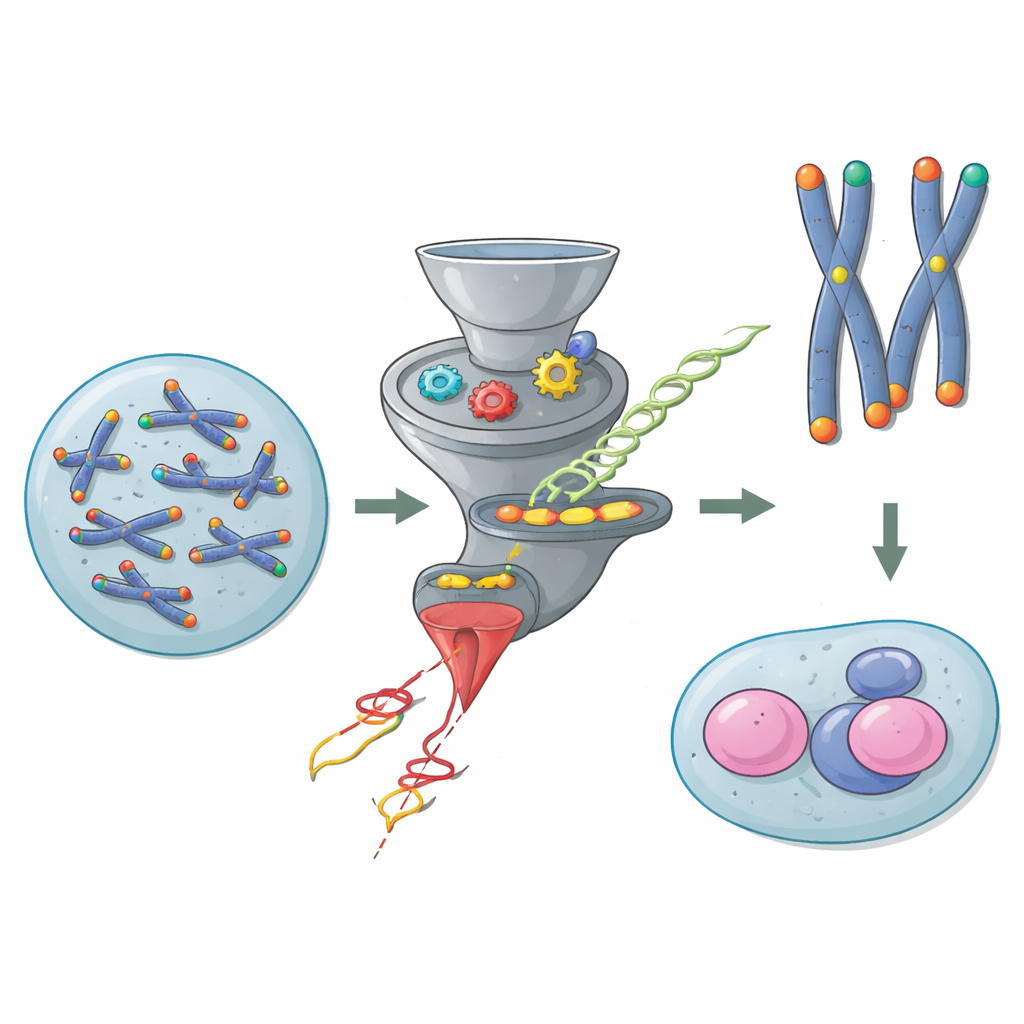
الأغطية الواقية في نهايات الكروموسومات
الكروموسومات هي جزيئات DNA طويلة تحتاج إلى حماية عند أطرافها حتى لا تُخطئ على أنها قطع مكسورة من الحمض النووي. توفر التيلوميرات هذه الحماية بمساعدة مجموعة من البروتينات المعروفة باسم شيلترين التي تغطي النهايات وتمنع تفاعلات إصلاح خطرة. في معظم خلايا الجسم، يُعد بروتين شيلترين واحد يُسمى TRF2 حاسمًا: بدونه، تلتحم نهايات الكروموسومات معًا، وتندلع استجابات تلف الحمض النووي، ويصبح الجينوم غير مستقر. ومع ذلك، تتجاوز خلايا الجنين المبكرة في الفئران هذه القاعدة. أظهرت أعمال سابقة أن هذه الخلايا الشابة تستطيع النجاة والانقسام حتى عندما يُزال TRF2، مشيرةً إلى أن هناك مسارًا مخفيًا يتدخل لحماية تيلوميراتها.
بحث شامل على مستوى الجينوم عن مساعد خفي
لكشف هذا الحارس المخفي، استخدم الباحثون شاشة جينية قوية. عطلوا جين Trf2 في خلايا جذعية جنينية ماوسية ثم استخدموا CRISPR–Cas9 لتعطيل آلاف الجينات الأخرى واحدًا تلو الآخر. إذا تسبب فقدان الجين الثاني فجأة في موت الخلايا التي كانت تفتقد TRF2 بالفعل، عُدَّ ذلك علامة «موت صناعي مشترك»—دليلًا على أنه يساعد في تعويض غياب TRF2. أعادت الشاشة عوامل تيلومير متوقعة لكنها أيضًا أظهرت عدة مكونات لمسار يبدو غير ذي صلة: التحلل غير الحتمي للرنا الرسول (NMD)، وهو نظام معروف أساسًا لإزالة رسائل الرنا المعيبة التي تحتوي إشارات توقف مبكرة.
عندما يفشل تنظيف الرنا، تنهار نهايات الكروموسومات
اختبر الفريق بعد ذلك ما يحدث عندما تُزال عوامل NMD في خلايا جذعية تفتقر إلى TRF2. أدى فقدان TRF2 وحده أو فقدان NMD وحده إلى ضرر طفيف في التيلوميرات: بدت النهايات الكروموسومية طبيعية إلى حد كبير، واستمرت الخلايا في النمو. لكن عندما تعطَّل TRF2 وNMD معًا، تغيَّر المشهد بشكل كبير. تراكمت علامات تلف الحمض النووي تحديدًا عند التيلوميرات، وغالبًا ما التحمت الكروموسومات رأسًا برأس. تزامنت هذه التحامّات مع عيوب نمو قوية، وزيادة في موت الخلايا، وعرقلة تقدم دورة الخلية، على الرغم من أن الخلايا احتفظت بسمات أساسية للخلايا الجذعية. أدى إيقاف NMD كيميائيًا أو عبر نظام التخلص السريع للبروتين إلى نفس ظاهرة التحام التيلوميرات، مما يستبعد التكيف طويل الأمد ويؤكد أن نشاط NMD المستمر مطلوب مباشرة للحفاظ على سلامة التيلوميرات في غياب TRF2.
بروتين مختصر ضار يقوض حراس التيلومير
في تحليل أعمق، فحص الباحثون أية رسائل رنا يتحكم فيها NMD في هذه الخلايا الجذعية. وجدوا أن جين Trf1، الذي يشفر بروتينًا آخر رابطًا للتيلومير يُدعى TRF1، ينتج متغير سبايليسي غير طبيعي عندما يتعرض NMD للخلل. هذا الرنا المُعدَّل يتخطى مقطعًا داخليًا ويحمل إشارة توقف مبكرًا، مما يؤدي إلى إنتاج بروتين TRF1 مختصر يفتقد طرفه القادر على ربط الـDNA لكنه لا يزال يستطيع الاقتران مع TRF1 الطبيعي. في الخلايا المعيبة في NMD، يتراكم هذا النسخة المقتطعة ويسحب TRF1 كامل الطول بعيدًا عن التيلوميرات. أظهرت التجارب أن احتلال TRF1 لنهايات الكروموسومات ينخفض بشدة في هذه الظروف، وأن إجبار الخلايا على إنتاج النسخة المقتطعة كان كافيًا لتحفيز التحامات التيلوميرات، خاصة عندما يغيب TRF2 أيضًا. وعلى النقيض، أعاد رفع مستويات TRF1 كامل الطول في الخلايا المعيبة في NMD حماية التيلوميرات إلى حد كبير، ما يؤكد أن فقدان TRF1 الفعال عند التيلوميرات هو المشكلة الأساسية.
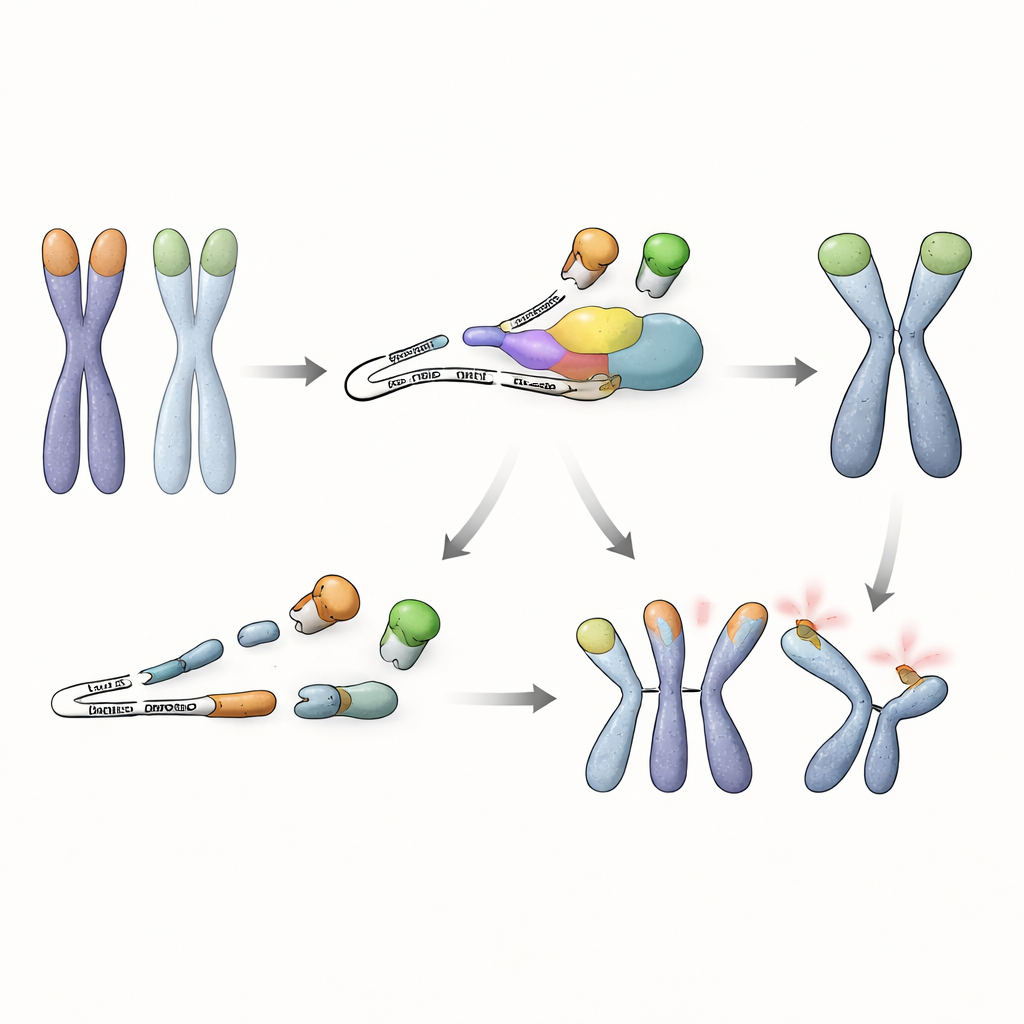
صلة جديدة بين مراقبة الرنا وسلامة الجينوم
مجتمعةً، تكشف هذه النتائج أن خلايا الجنين الجذعية تعتمد على أكثر من بروتينات ربط نهايات الـDNA لحماية كروموسوماتها. فهي تحتاج أيضًا إلى مسار مراقبة جودة الرنا لمنع تراكم بروتين TRF1 المختصر الضار الذي يزيح نظيره الوقائي كامل الطول. ما دام NMD نشطًا، يُدمر هذا الرنا الخاطئ بسرعة، ويظل TRF1 عند التيلوميرات، ويمكن للخلايا الجذعية تحمل فقدان TRF2 دون تحامّات كارثية في الكروموسومات. تكشف هذه الاكتشافات عن استراتيجية لم تكن معروفة سابقًا تربط مراقبة الرنا بحماية التيلوميرات، مسلطةً الضوء على كيف تتعاون طبقات متعددة من الضوابط للحفاظ على استقرار الجينوم خلال المراحل الأولى من الحياة.
الاستشهاد: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
الكلمات المفتاحية: التيلوميرات, الخلايا الجذعية متعددة القدرات, مراقبة جودة الرنا, التحلل غير الحتمي, استقرار الجينوم