Clear Sky Science · nl
Onzinige mRNA-afbraak bewaakt telomeren in pluripotente stamcellen
Hoe cellen hun chromosoomkapjes veilig houden
Elke keer dat een cel zich deelt, moet zij haar DNA kopiëren en beschermen. De uiteinden van onze chromosomen zijn afgedekt met speciale structuren, telomeren genoemd, die werken als plastic uiteinden van veters en voorkomen dat ze rafelen of ten onrechte worden gerepareerd. Deze studie onderzoekt hoe vroege muizenstamcellen een onverwacht achtervangsysteem gebruiken — een RNA-"kwaliteitscontrole"-route — om deze kapjes intact te houden wanneer een belangrijk beschermend eiwit ontbreekt, en onthult daarmee een verrassende koppeling tussen RNA-toezicht en chromosoomveiligheid.
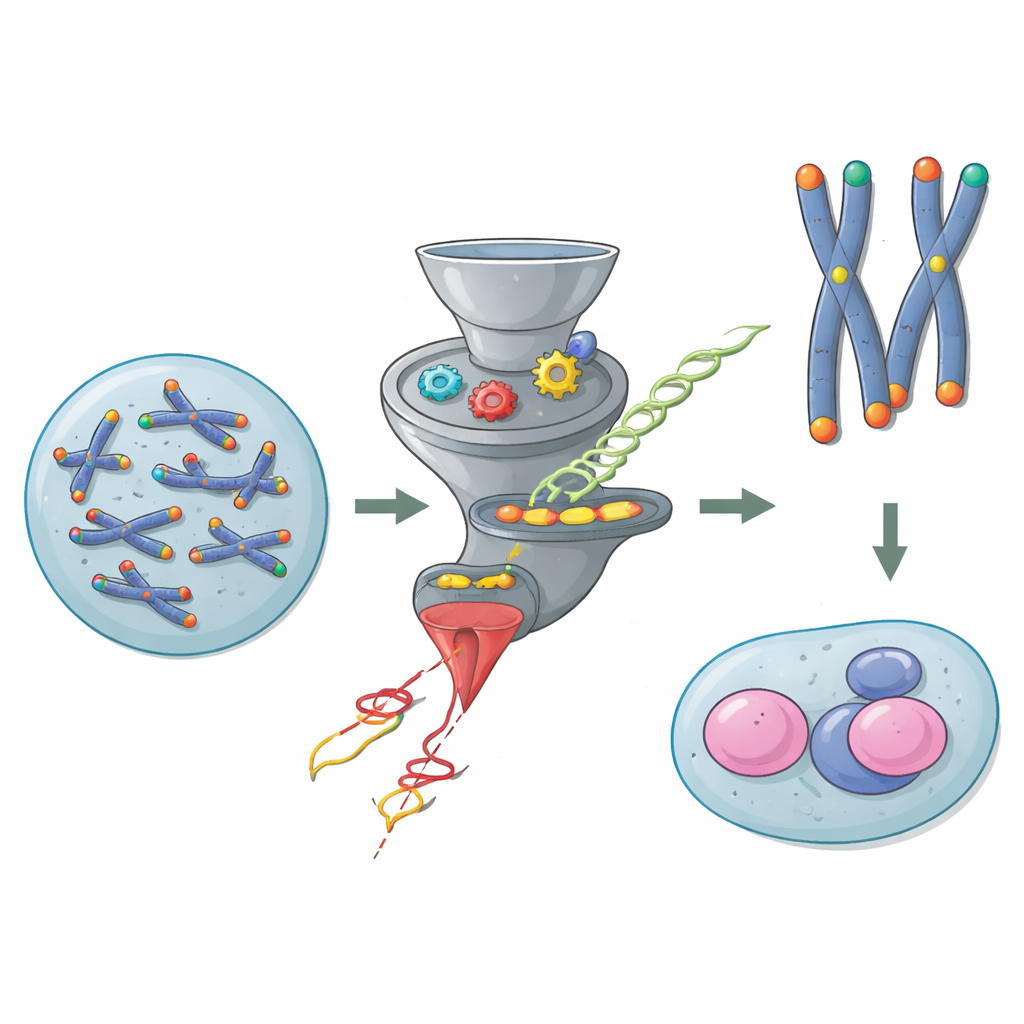
De beschermende kapjes aan de uiteinden van chromosomen
Chromosomen zijn lange DNA-moleculen die bescherming aan hun uiteinden nodig hebben zodat ze niet worden aangezien voor gebroken DNA. Telomeren bieden deze bescherming, met hulp van een groep eiwitten die Shelterin wordt genoemd en die de uiteinden bedekken en gevaarlijke reparatiereacties blokkeren. In de meeste lichaamscellen is één Shelterin-eiwit, TRF2, cruciaal: zonder dit eiwit fuseren chromosoomuiteinden, laait de DNA-schaderespons op en raakt het genoom instabiel. Muizenembryonale stamcellen doorbreken deze regel echter. Vorig werk toonde aan dat deze jonge cellen kunnen overleven en delen zelfs wanneer TRF2 is verwijderd, wat suggereert dat een verborgen route inspringt om hun telomeren te beschermen.
Een genoomwijde zoektocht naar een verborgen helper
Om deze verborgen beveiliging te ontdekken, gebruikten de onderzoekers een krachtige genetische screen. Ze schakelden het Trf2-gen uit in muizenembryonale stamcellen en gebruikten vervolgens CRISPR–Cas9 om duizenden andere genen één voor één te verstoren. Als het verliezen van een tweede gen de al TRF2-misende cellen plotseling deed sterven, werd dat tweede gen gemarkeerd als partner in "synthetische lethale" interactie — een teken dat het compenseert voor het verlies van TRF2. De screen bracht verwachte telomeerfactoren aan het licht maar benadrukte ook verschillende componenten van een schijnbaar niet-verwante route: onzinige mRNA-afbraak (NMD), een systeem dat vooral bekend is om het elimineren van foutieve RNA-berichten met voortijdige stopcodons.
Wanneer RNA-opruiming faalt, breken chromosoomuiteinden
Het team testte vervolgens wat er gebeurt wanneer NMD-factoren worden verwijderd in TRF2-deficiënte stamcellen. Ofwel veroorzaakte het verlies van TRF2 alleen, of het verlies van NMD alleen, weinig telomeerschade: chromosoomuiteinden zagen er grotendeels normaal uit en cellen bleven doorgroeien. Maar wanneer TRF2 en NMD samen werden verstoord, veranderde het beeld drastisch. Markers van DNA-schade stapelden zich specifiek bij telomeren op, en chromosomen fuseerden vaak eind-aan-eind. Deze gefuseerde chromosomen gingen gepaard met sterke groeidefecten, toegenomen celdood en geblokkeerde celcyclusvoortgang, ook al behielden de cellen kernkenmerken van stamcellen. Acute chemische of degron-gebaseerde uitschakeling van NMD gaf hetzelfde telomeer-fusiefenotype, waarmee langdurige aanpassing werd uitgesloten en bevestigd dat voortdurende NMD-activiteit direct vereist is om TRF2-vrije telomeren veilig te houden.
Een schadelijk verkort eiwit ondermijnt telomeerbescherming
Dieper grävend onderzochten de onderzoekers welke RNA-berichten door NMD in deze stamcellen worden gecontroleerd. Ze ontdekten dat het Trf1-gen, dat codeert voor een ander telomeerbindend eiwit, TRF1, een abnormale splice-variant produceert wanneer NMD is aangetast. Dit gewijzigde RNA slaat een intern segment over en draagt een voortijdig stopcodon, wat leidt tot de productie van een verkorte TRF1 die de DNA-bindende punt mist maar nog wel met normale TRF1 kan samengaan. In NMD-deficiënte cellen hoopt deze ingekorte versie zich op en onttrekt ze volwaardige TRF1 aan de telomeren. Experimenten toonden aan dat de bezetting van TRF1 aan chromosoomuiteinden scherp daalt onder deze omstandigheden, en het simpelweg dwingen van cellen om het verkorte eiwit te maken was voldoende om telomeerfusies teweeg te brengen, vooral wanneer TRF2 ook ontbrak. Omgekeerd herstelde het verhogen van de niveaus van volwaardige TRF1 in NMD-defecte cellen grotendeels de telomeerbescherming, wat benadrukt dat verlies van effectieve TRF1 aan telomeren het kernprobleem is.
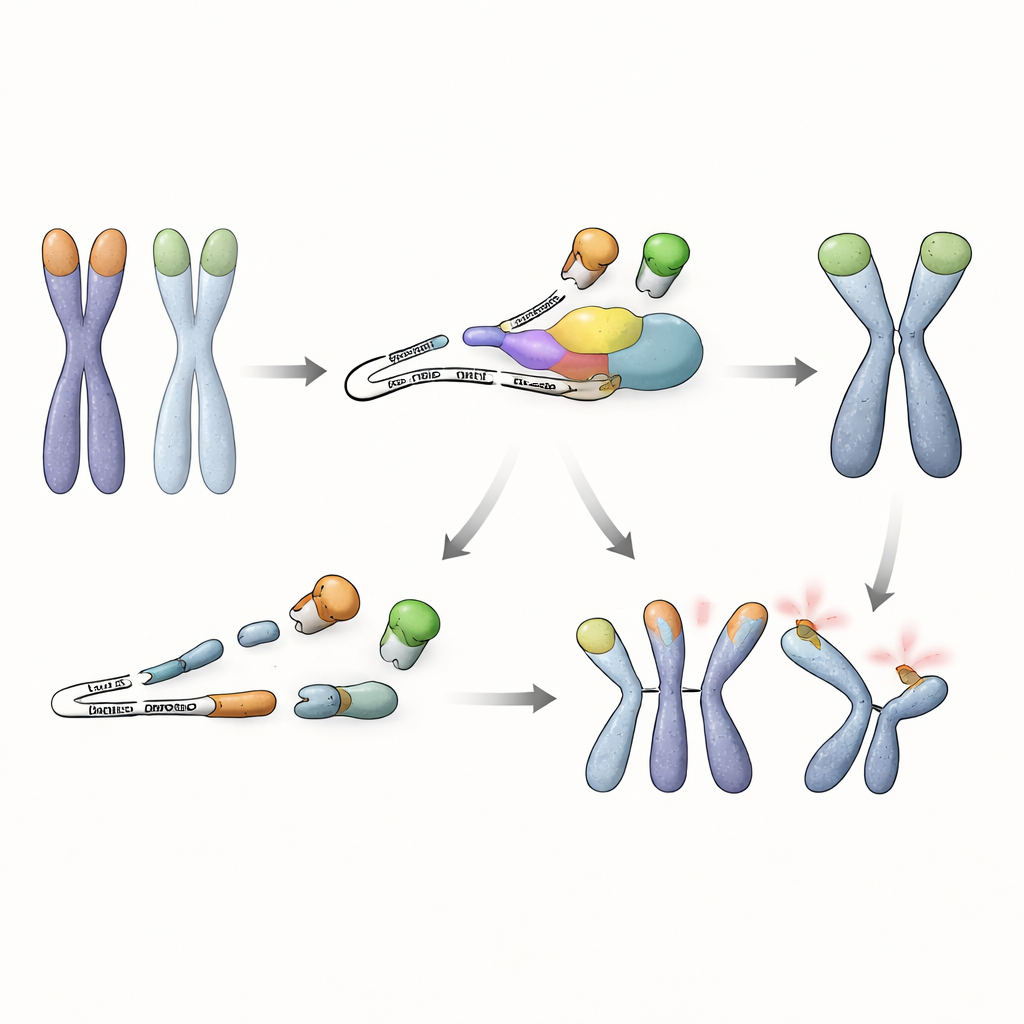
Een nieuwe koppeling tussen RNA-toezicht en genoomveiligheid
Gezamenlijk onthult dit werk dat embryonale stamcellen vertrouwen op meer dan alleen DNA-uiteinden-bindende eiwitten om hun chromosomen te beschermen. Ze hebben ook een RNA-kwaliteitscontroleroute nodig om de ophoping van een schadelijke, ingekorte TRF1 te voorkomen die zijn beschermende full-length tegenhanger verdringt. Zolang NMD actief is, wordt dit foutieve RNA snel afgebroken, blijft TRF1 aan telomeren aanwezig en kunnen stamcellen het verlies van TRF2 verdragen zonder catastrofale chromosoomfusies. Deze ontdekking onthult een eerder over het hoofd gezien mechanisme waarmee vroege stamcellen RNA-toezicht koppelen aan telomeerbescherming en benadrukt hoe meerdere controlelagen samenwerken om genoomstabiliteit in de vroegste stadia van het leven te bewaren.
Bronvermelding: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Trefwoorden: telomeren, pluripotente stamcellen, RNA-kwaliteitscontrole, onzinige-afbraak, genoomstabiliteit