Clear Sky Science · es
La degradación de ARNm mediada por nonsense protege los telómeros en células madre pluripotentes
Cómo las células mantienen a salvo las tapas de sus cromosomas
Cada vez que una célula se divide, debe copiar y proteger su ADN. Los extremos de nuestros cromosomas están rematados por estructuras especiales llamadas telómeros, que actúan como las puntas de plástico de los cordones, evitando que se deshilachen o se reparen por error. Este estudio explora cómo las células madre tempranas de ratón usan un sistema de respaldo inesperado —una vía de “control de calidad” del ARN— para mantener intactas estas tapas cuando falta una proteína protectora principal, revelando una conexión sorprendente entre la vigilancia del ARN y la seguridad cromosómica.
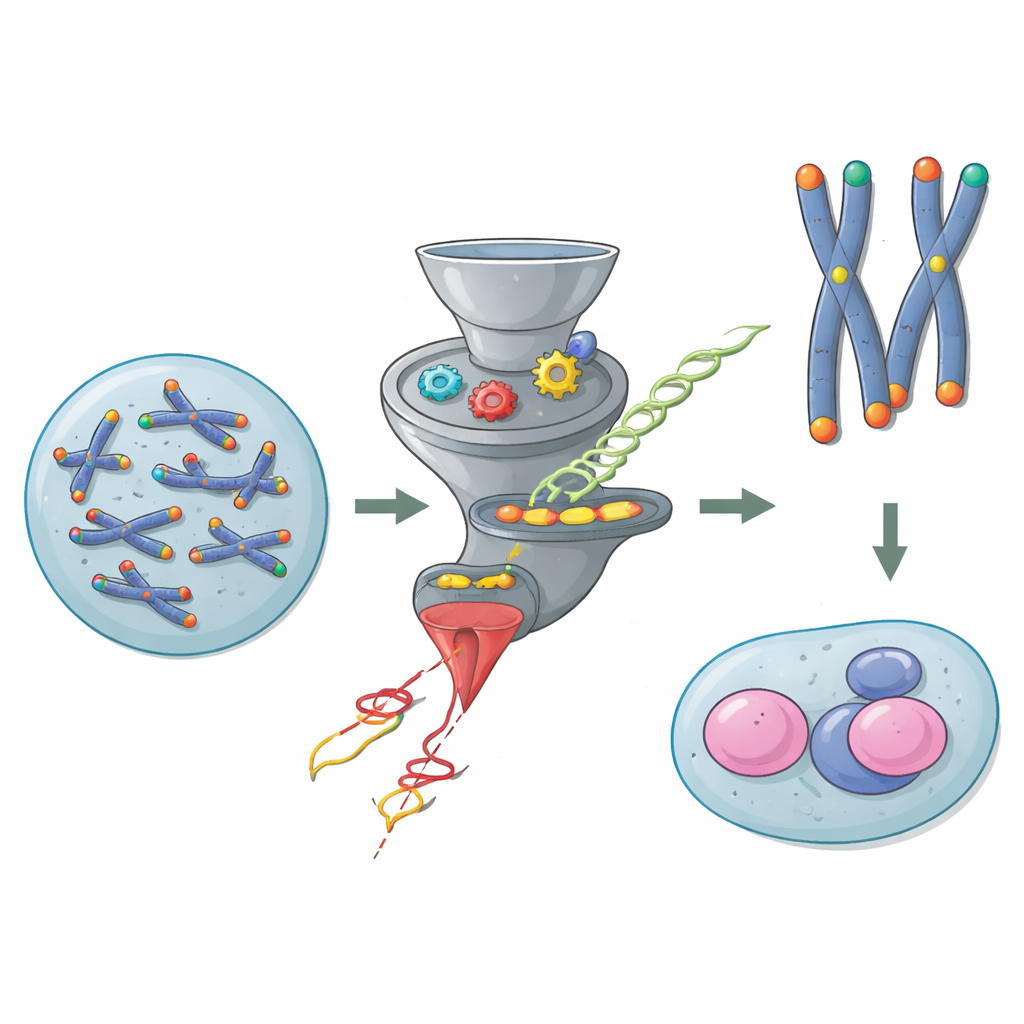
Las tapas protectoras en los extremos de los cromosomas
Los cromosomas son largas moléculas de ADN que necesitan protección en sus extremos para no confundirse con ADN roto. Los telómeros proporcionan esa protección, ayudados por un conjunto de proteínas conocido como Shelterin, que recubren los extremos y bloquean reacciones de reparación peligrosas. En la mayoría de las células del organismo, una proteína de Shelterin llamada TRF2 es crucial: sin ella, los extremos cromosómicos se fusionan, se activan respuestas de daño en el ADN y los genomas se vuelven inestables. Sin embargo, las células madre embrionarias de ratón desafían esta regla. Trabajos previos mostraron que estas células jóvenes pueden sobrevivir y dividirse incluso cuando se elimina TRF2, lo que sugiere que una vía oculta interviene para proteger sus telómeros.
Una búsqueda a escala genómica de un ayudante oculto
Para descubrir este salvaguarda oculto, los investigadores emplearon una potente criba genética. Anularon el gen Trf2 en células madre embrionarias de ratón y luego utilizaron CRISPR–Cas9 para alterar miles de otros genes uno por uno. Si la pérdida de un segundo gen mataba repentinamente a las células que ya carecían de TRF2, ese segundo gen se marcaba como socio en una “letalidad sintética”, señal de que ayuda a compensar la pérdida de TRF2. La criba recuperó factores de telómero esperados, pero también destacó varios componentes de una vía aparentemente no relacionada: la degradación de ARNm mediada por nonsense (NMD), un sistema conocido por eliminar mensajes ARN defectuosos que contienen señales de paro prematuro.
Cuando la limpieza del ARN falla, los extremos cromosómicos se rompen
El equipo probó entonces qué ocurre cuando se eliminan factores de NMD en células madre deficientes en TRF2. La pérdida de TRF2 sola o la pérdida de NMD sola provocaron poco daño en los telómeros: los extremos cromosómicos parecían mayormente normales y las células seguían proliferando. Pero cuando TRF2 y NMD se interrumpieron simultáneamente, el panorama cambió drásticamente. Marcadores de daño en el ADN se acumularon específicamente en los telómeros y los cromosomas con frecuencia se fusionaron extremo con extremo. Estas fusiones coincidieron con fuertes defectos de crecimiento, aumento de la muerte celular y bloqueo de la progresión del ciclo celular, aunque las células aún conservaban rasgos centrales de células madre. El cierre agudo de la NMD mediante compuestos químicos o degradación por degrón produjo el mismo fenotipo de fusión de telómeros, descartando una adaptación a largo plazo y confirmando que la actividad continua de NMD es directamente necesaria para mantener seguros los telómeros sin TRF2.
Una proteína acortada y dañina socava las defensas de los telómeros
Profundizando, los investigadores examinaron qué mensajes de ARN controla la NMD en estas células madre. Encontraron que el gen Trf1, que codifica otra proteína que se une a los telómeros, TRF1, genera una variante de empalme anómala cuando la NMD está comprometida. Este ARN alterado omite un segmento interno y lleva una señal de paro prematura, lo que conduce a la producción de una proteína TRF1 acortada que carece de su punta de unión al ADN pero aún puede emparejarse con la TRF1 normal. En las células deficientes en NMD, esta versión truncada se acumula y desplaza a la TRF1 de longitud completa fuera de los telómeros. Los experimentos mostraron que la ocupación de TRF1 en los extremos cromosómicos cae bruscamente en estas condiciones, y simplemente forzar la expresión de la proteína truncada fue suficiente para desencadenar fusiones de telómeros, especialmente cuando también faltaba TRF2. Por el contrario, aumentar los niveles de TRF1 de longitud completa en células con NMD defectuosa restauró en gran medida la protección de los telómeros, subrayando que la pérdida de TRF1 funcional en los telómeros es el problema clave.
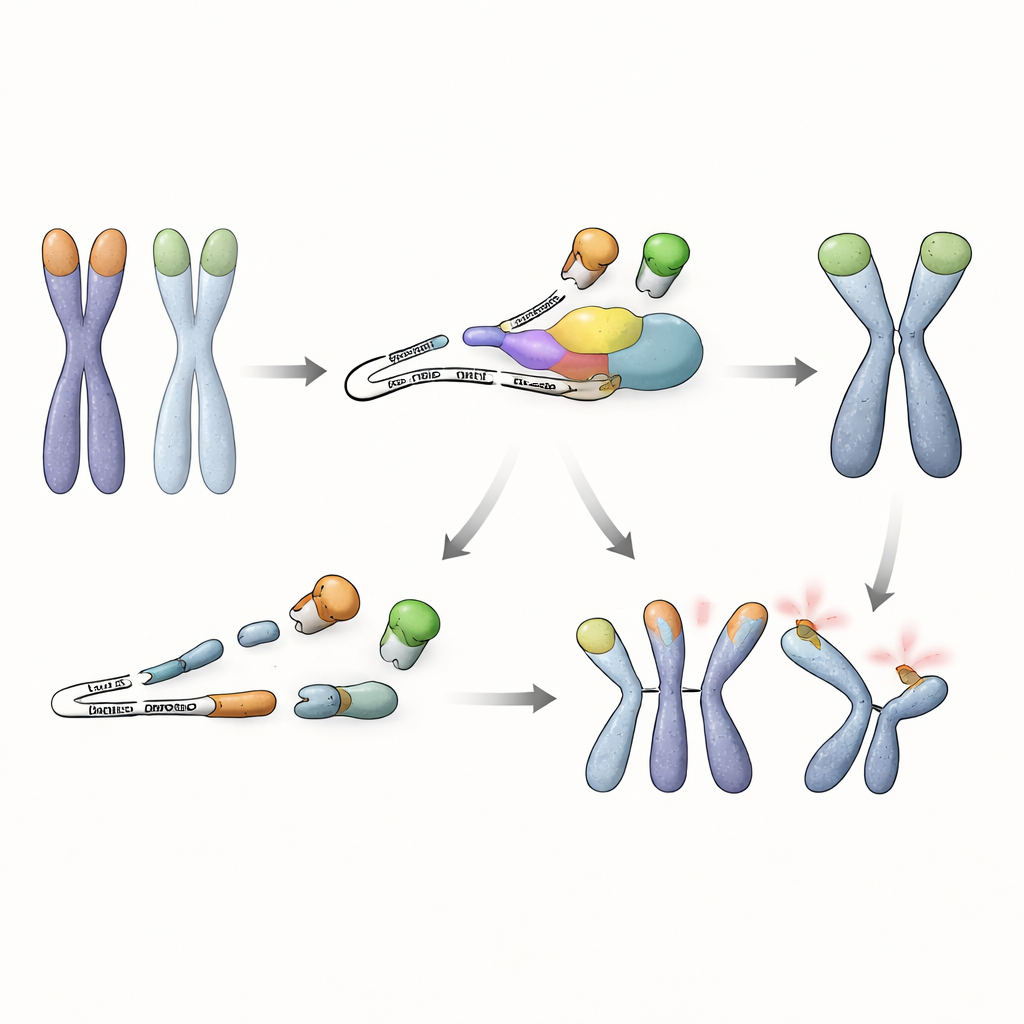
Un nuevo vínculo entre la vigilancia del ARN y la seguridad del genoma
En conjunto, el trabajo revela que las células madre embrionarias dependen de algo más que proteínas que se unen a los extremos del ADN para proteger sus cromosomas. También necesitan una vía de control de calidad del ARN para evitar la acumulación de una TRF1 acortada y dañina que desplaza a su contraparte protectora de longitud completa. Mientras la NMD esté activa, este ARN defectuoso se destruye rápidamente, TRF1 permanece en los telómeros y las células madre pueden tolerar la pérdida de TRF2 sin fusiones cromosómicas catastróficas. Este descubrimiento desvela una estrategia hasta ahora no reconocida por la cual las células madre tempranas conectan la vigilancia del ARN con la protección de los telómeros, y pone de relieve cómo múltiples capas de control cooperan para preservar la estabilidad del genoma durante las primeras etapas de la vida.
Cita: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Palabras clave: telómeros, células madre pluripotentes, control de calidad del ARN, degradación por nonsense, estabilidad del genoma