Clear Sky Science · sv
Avfallshantering av mRNA skyddar telomerer i pluripotenta stamceller
Hur celler skyddar sina kromosomändar
Varje gång en cell delar sig måste den kopiera och skydda sitt DNA. Kromosomernas ändar är försedda med särskilda strukturer som kallas telomerer och fungerar som plastspetsar på skosnören för att förhindra att de fransar sig eller repareras felaktigt. Denna studie undersöker hur tidiga musstamceller använder ett oväntat reservsystem — en RNA "kvalitetskontroll"-väg — för att hålla dessa skydd intakta när ett viktigt skyddsprotein saknas, och visar på en överraskande koppling mellan RNA-övervakning och kromosomsäkerhet.
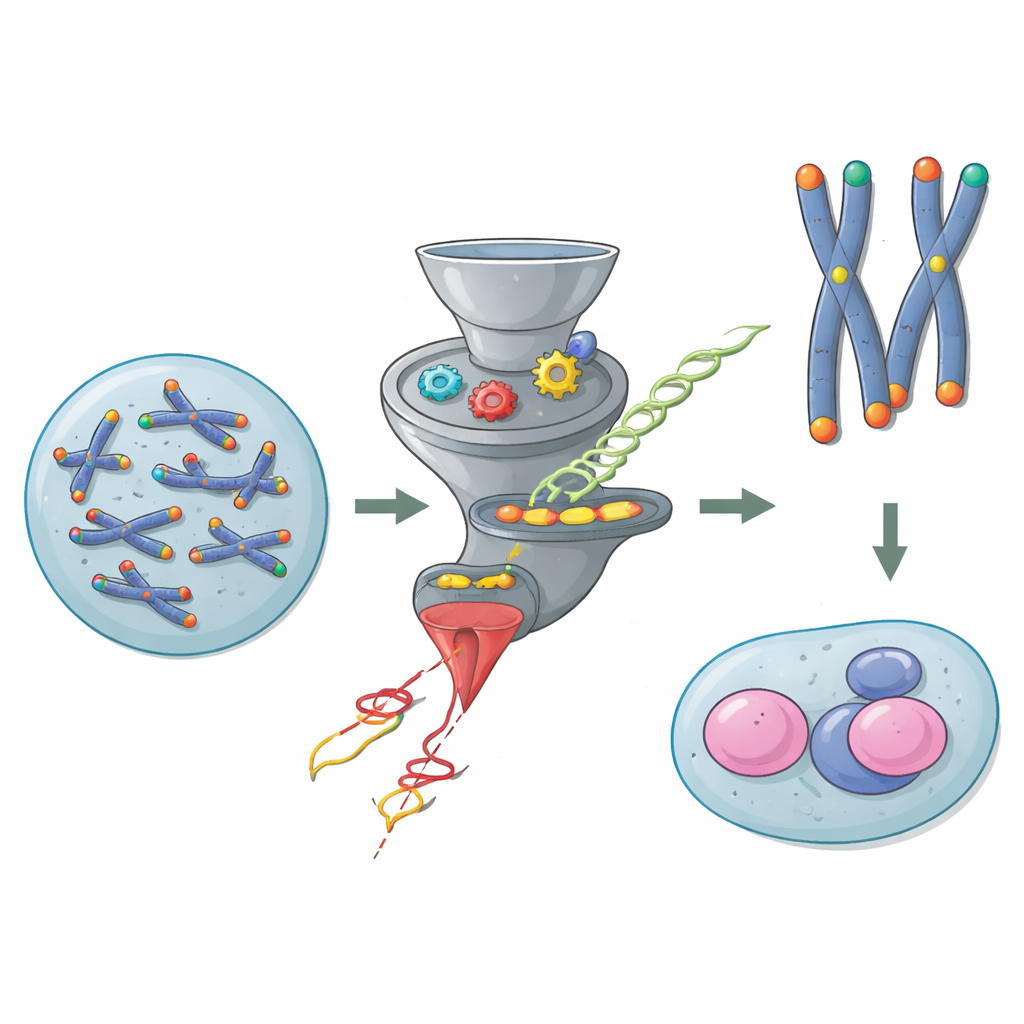
Skyddande spetsar i kromosomernas ändar
Kromosomer är långa DNA-molekyler som behöver skydd vid sina ändar för att inte förväxlas med brutet DNA. Telomerer ger detta skydd, understödda av en grupp proteiner kända som Shelterin som bekläder ändarna och blockerar farliga reparationsreaktioner. I de flesta kroppsceller är ett Shelterin-protein som heter TRF2 avgörande: utan det fusionerar kromosomändar, DNA-skaderesponsen aktiveras och genomet blir instabilt. Men musens embryonala stamceller bryter mot denna regel. Tidigare arbete visade att dessa unga celler kan överleva och dela sig även när TRF2 tas bort, vilket tyder på att någon dold väg träder in för att skydda deras telomerer.
En genombredd sökning efter en dold hjälpare
För att hitta detta dolda skydd använde forskarna en kraftfull genetisk skärm. De inaktiverade genen Trf2 i musens embryonala stamceller och använde sedan CRISPR–Cas9 för att störa tusentals andra gener en efter en. Om förlusten av en andra gen plötsligt dödade celler som redan saknade TRF2 markerades den andra genen som ett partner i "syntetisk letalitet" — ett tecken på att den hjälper till att kompensera för TRF2-bortfallet. Skärmen återfann förväntade telomerfaktorer men framhävde också flera komponenter i en till synes orelaterad väg: nonsense-medierad mRNA-nedbrytning (NMD), ett system mest känt för att eliminera felaktiga RNA-meddelanden som innehåller tidiga stoppkodon.
När RNA-städningen misslyckas bryts kromosomändarna
Teamet testade sedan vad som händer när NMD-faktorer tas bort i TRF2-defekta stamceller. Antingen TRF2-förlust ensam eller NMD-förlust ensam ledde till lite telomeriskada: kromosomändarna såg mestadels normala ut och cellerna fortsatte växa. Men när både TRF2 och NMD stördes samtidigt förändrades bilden dramatiskt. Markörer för DNA-skada byggdes upp specifikt vid telomererna, och kromosomer fusionerade ofta ända till ände. Dessa fusionerade kromosomer sammanföll med kraftiga tillväxthämningar, ökad celldöd och blockerad cellcykelprogression, även om cellerna fortfarande behöll grundläggande stamcellsegenskaper. Akut kemisk eller degron-baserad nedstängning av NMD gav samma telomerfusionsfenotyp, vilket uteslöt långsiktig anpassning och bekräftade att pågående NMD-aktivitet direkt krävs för att hålla TRF2-fria telomerer säkra.
Ett skadligt förkortat protein underminerar telomerskyddet
Djupare analys visade vilka RNA-meddelanden som kontrolleras av NMD i dessa stamceller. Forskarna fann att Trf1-genen, som kodar för ett annat telomerbindande protein, TRF1, producerar en onormal splitsvariant när NMD är nedsatt. Detta förändrade RNA hoppar över ett internt segment och bär en tidig stoppkodon, vilket leder till produktion av ett förkortat TRF1-protein som saknar sin DNA-bindande spets men fortfarande kan paras med normalt TRF1. I NMD-defekta celler ackumuleras denna trunkerade variant och drar fullängds-TRF1 bort från telomererna. Experiment visade att TRF1-occupancy vid kromosomändarna faller markant under dessa förhållanden, och att enbart att tvinga celler att producera det trunkerade proteinet var tillräckligt för att utlösa telomerfusioner, särskilt när TRF2 också saknades. Omvänt återställde ökade nivåer av fullängds-TRF1 i NMD-defekta celler i stor utsträckning telomerskyddet, vilket betonar att förlusten av effektiv TRF1 vid telomererna är den centrala orsaken.
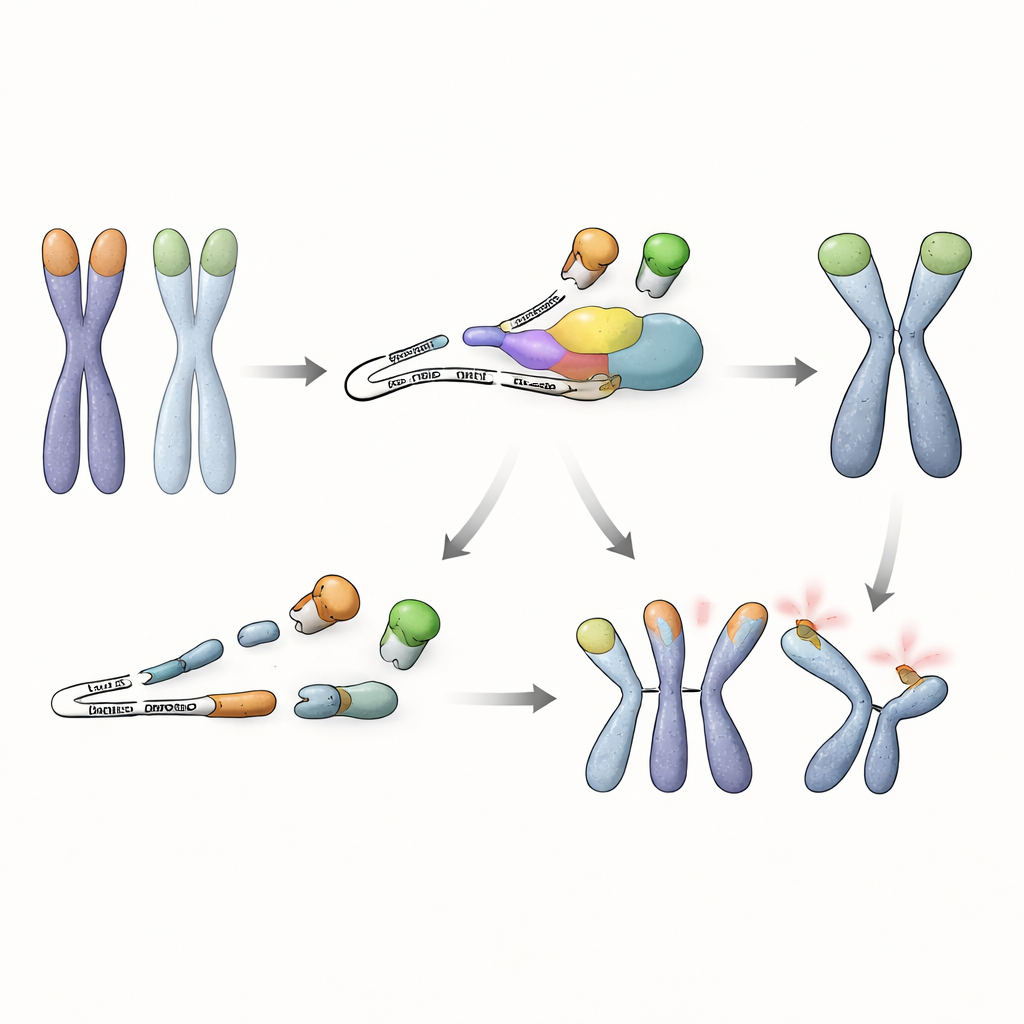
En ny koppling mellan RNA-övervakning och genomsäkerhet
Sammantaget visar arbetet att embryonala stamceller är beroende av mer än bara DNA-ändbindande proteiner för att skydda sina kromosomer. De behöver också en RNA-kvalitetskontrollväg för att förhindra uppbyggnad av ett skadligt, förkortat TRF1-protein som tränger ut dess skyddande fullängds-motsvarighet. Så länge NMD är aktiv förstörs detta felaktiga RNA snabbt, TRF1 stannar vid telomererna och stamceller kan tolerera förlust av TRF2 utan katastrofala kromosomfusioner. Denna upptäckt blottlägger en tidigare okänd strategi där tidiga stamceller kopplar RNA-övervakning till telomerskydd och belyser hur flera kontrolllager samarbetar för att bevara genomstabilitet under livets tidigaste skeden.
Citering: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Nyckelord: telomerer, pluripotenta stamceller, RNA-kvalitetskontroll, nonsense-medierad nedbrytning, genomstabilitet