Clear Sky Science · pt
A degradação de mRNA mediada por nonsense protege telômeros em células-tronco pluripotentes
Como as células mantêm seguras as tampas dos cromossomos
Cada vez que uma célula se divide, ela precisa copiar e proteger seu DNA. As extremidades dos nossos cromossomos são protegidas por estruturas especiais chamadas telômeros que funcionam como ponteiras plásticas em cadarços, impedindo que se desgastem ou sejam confundidas com quebras. Este estudo explora como células-tronco embrionárias de camundongo utilizam um sistema de reserva inesperado — uma via de “controle de qualidade” do RNA — para manter essas tampas intactas quando uma proteína protetora principal está ausente, revelando uma ligação surpreendente entre vigilância de RNA e segurança dos cromossomos.
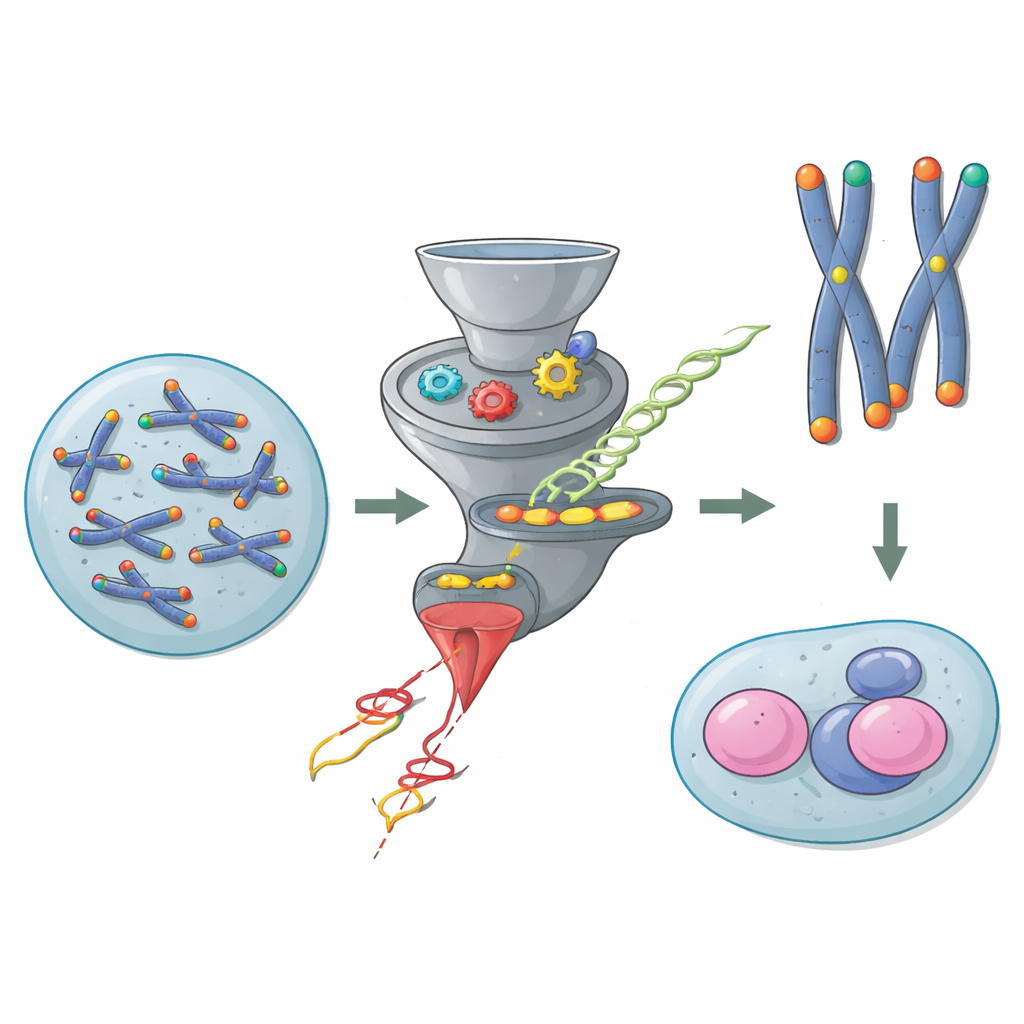
As tampas protetoras nas extremidades dos cromossomos
Cromossomos são longas moléculas de DNA que precisam de proteção em suas pontas para não serem confundidas com DNA quebrado. Os telômeros fornecem essa proteção, auxiliados por um conjunto de proteínas conhecido como Shelterin, que recobre as extremidades e bloqueia reações de reparo perigosas. Na maioria das células do corpo, uma proteína do Shelterin chamada TRF2 é crucial: sem ela, as extremidades cromossômicas se fundem, respostas de dano ao DNA disparam e os genomas se tornam instáveis. Ainda assim, células-tronco embrionárias de camundongo quebram essa regra. Trabalhos anteriores mostraram que essas células jovens conseguem sobreviver e se dividir mesmo quando TRF2 é removida, sugerindo que alguma via oculta assume a proteção dos telômeros.
Uma busca genômica por um ajudante oculto
Para descobrir esse salvaguarda oculto, os pesquisadores usaram uma triagem genética poderosa. Eles inativaram o gene Trf2 em células-tronco embrionárias de camundongo e então empregaram CRISPR–Cas9 para perturbar milhares de outros genes um a um. Se a perda de um segundo gene matasse subitamente células que já estavam sem TRF2, esse segundo gene era marcado como parceiro em “letalidade sintética” — um indício de que ele ajuda a compensar a perda de TRF2. A triagem recuperou fatores de telômero esperados, mas também destacou vários componentes de uma via aparentemente não relacionada: a degradação mediada por nonsense (NMD), um sistema mais conhecido por eliminar mensagens de RNA defeituosas que contêm sinais de parada prematuros.
Quando a limpeza de RNA falha, as extremidades cromossômicas se rompem
A equipe então testou o que ocorre quando fatores da NMD são removidos em células-tronco deficientes em TRF2. A perda isolada de TRF2 ou a perda isolada de NMD causaram pouco dano aos telômeros: as extremidades cromossômicas pareciam em sua maior parte normais e as células continuavam a proliferar. Mas quando TRF2 e NMD foram perturbados em conjunto, o quadro mudou dramaticamente. Marcadores de dano ao DNA se acumularam especificamente nos telômeros, e os cromossomos frequentemente se fundiram extremidade a extremidade. Essas fusões cromossômicas coincidiram com fortes defeitos de crescimento, aumento da morte celular e bloqueio da progressão do ciclo celular, embora as células ainda preservassem características fundamentais de células-tronco. A desativação aguda da NMD por vias químicas ou por degrons produziu o mesmo fenótipo de fusão de telômeros, descartando adaptação a longo prazo e confirmando que a atividade contínua da NMD é diretamente necessária para manter seguros os telômeros na ausência de TRF2.
Uma proteína encurtada e prejudicial compromete os guardiões dos telômeros
Avançando mais, os pesquisadores examinaram quais mensagens de RNA são controladas pela NMD nessas células-tronco. Eles descobriram que o gene Trf1, que codifica outra proteína que se liga aos telômeros, TRF1, produz uma variante de splicing anômala quando a NMD está comprometida. Esse RNA alterado pula um segmento interno e carrega um sinal de parada precoce, resultando na produção de uma proteína TRF1 encurtada que carece da ponta de ligação ao DNA, mas ainda pode se emparelhar com a TRF1 normal. Em células com deficiência de NMD, essa versão truncada se acumula e afasta a TRF1 de comprimento completo dos telômeros. Experimentos mostraram que a ocupação de TRF1 nas extremidades cromossômicas cai acentuadamente nessas condições, e simplesmente forçar a expressão da proteína truncada foi suficiente para desencadear fusões de telômeros, especialmente quando TRF2 também estava ausente. Por outro lado, aumentar os níveis de TRF1 de comprimento completo em células defeituosas para NMD restaurou em grande parte a proteção dos telômeros, ressaltando que a perda da TRF1 funcional nos telômeros é o problema central.
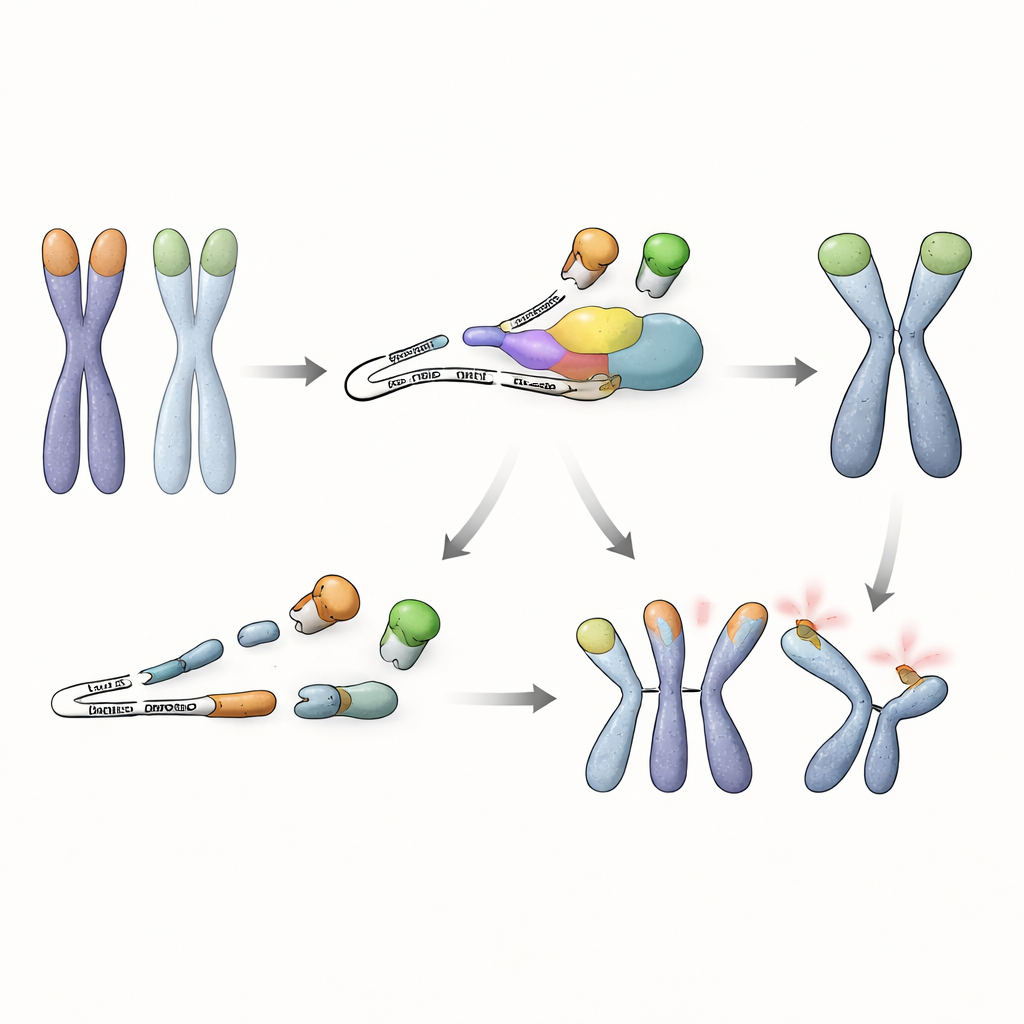
Uma nova ligação entre vigilância de RNA e segurança do genoma
Em conjunto, o trabalho revela que células-tronco embrionárias dependem de mais do que apenas proteínas que se ligam às extremidades do DNA para proteger seus cromossomos. Elas também precisam de uma via de controle de qualidade do RNA para evitar o acúmulo de uma TRF1 encurtada e prejudicial que desloca sua contraparte protetora de comprimento completo. Enquanto a NMD estiver ativa, esse RNA defeituoso é rapidamente degradado, TRF1 permanece nos telômeros e as células-tronco conseguem tolerar a perda de TRF2 sem fusões catastróficas de cromossomos. Essa descoberta revela uma estratégia até então não reconhecida pela qual células-tronco precoces vinculam vigilância de RNA à proteção dos telômeros, destacando como múltiplas camadas de controle cooperam para preservar a estabilidade do genoma nas fases mais iniciais da vida.
Citação: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Palavras-chave: telômeros, células-tronco pluripotentes, controle de qualidade de RNA, degradação mediada por nonsense, estabilidade do genoma