Clear Sky Science · fr
La dégradation des ARNm par le NMD protège les télomères dans les cellules souches pluripotentes
Comment les cellules protègent les extrémités de leurs chromosomes
À chaque division, une cellule doit copier et protéger son ADN. Les extrémités de nos chromosomes sont coiffées par des structures spéciales appelées télomères, qui fonctionnent comme des embouts plastiques sur des lacets pour éviter l'effilochage et les réparations inappropriées. Cette étude explore comment des cellules souches embryonnaires de souris utilisent un système de secours inattendu — une voie de « contrôle qualité » de l'ARN — pour maintenir ces coiffes intactes lorsqu'une protéine protectrice majeure fait défaut, révélant un lien surprenant entre la surveillance de l'ARN et la sécurité des chromosomes.
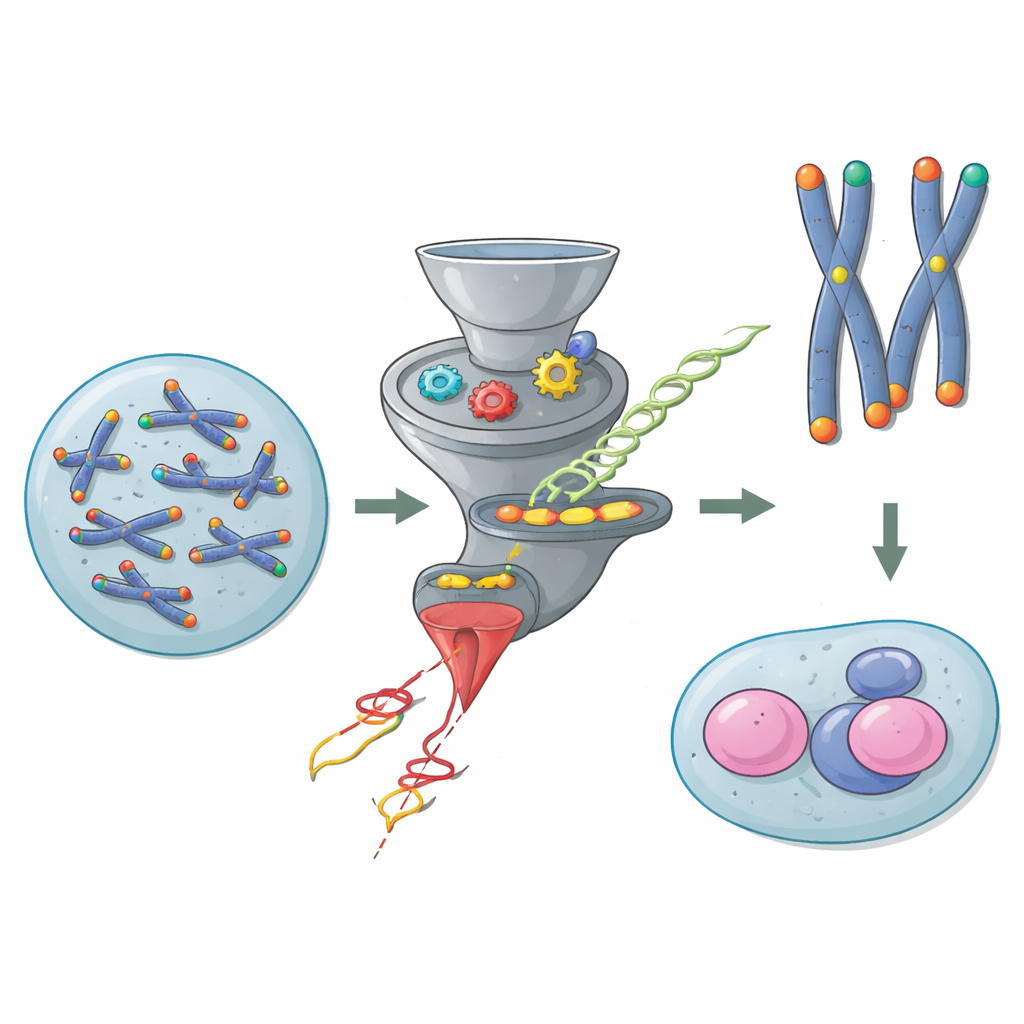
Les coiffes protectrices aux extrémités des chromosomes
Les chromosomes sont de longues molécules d'ADN qui ont besoin d'une protection à leurs extrémités pour ne pas être confondues avec de l'ADN cassé. Les télomères assurent cette protection, aidés par un groupe de protéines nommé Shelterin qui revêt les extrémités et empêche des réactions de réparation dangereuses. Dans la plupart des cellules somatiques, une protéine Shelterin appelée TRF2 est cruciale : sans elle, les extrémités chromosomiques fusionnent, les réponses aux dommages de l'ADN s'enflamment et les génomes deviennent instables. Pourtant, les cellules souches embryonnaires de souris transgressent cette règle. Des travaux antérieurs ont montré que ces cellules jeunes peuvent survivre et se diviser même lorsque TRF2 est supprimée, ce qui suggère qu'une voie cachée prend le relais pour protéger leurs télomères.
Une recherche à l'échelle du génome pour trouver un « assistant » caché
Pour découvrir ce mécanisme de secours, les chercheurs ont utilisé un criblage génétique puissant. Ils ont inactivé le gène Trf2 dans des cellules souches embryonnaires de souris puis employé CRISPR–Cas9 pour perturber des milliers d'autres gènes un par un. Si la perte d'un deuxième gène tuait soudainement des cellules déjà dépourvues de TRF2, ce deuxième gène était signalé comme participant à une « létalité synthétique » — indice qu'il aide à compenser l'absence de TRF2. Le criblage a retrouvé des facteurs télomériques attendus mais a aussi mis en évidence plusieurs composants d'une voie a priori non liée : la dégradation des ARNm par les non-sens (NMD), un système surtout connu pour éliminer les messages ARN défectueux contenant des signaux d'arrêt prématurés.
Quand le nettoyage des ARN échoue, les extrémités chromosomiques se brisent
L'équipe a ensuite testé ce qui se passe lorsque les facteurs NMD sont supprimés dans des cellules souches dépourvues de TRF2. La perte de TRF2 seule ou la perte du NMD seule causaient peu de dommages aux télomères : les extrémités chromosomiques paraissaient majoritairement normales et les cellules continuaient de croître. Mais lorsque TRF2 et le NMD étaient perturbés simultanément, le tableau changeait radicalement. Des marqueurs de dommages à l'ADN s'accumulaient spécifiquement aux télomères, et les chromosomes fusionnaient fréquemment bout à bout. Ces chromosomes fusionnés coïncidaient avec de forts défauts de croissance, une augmentation de la mort cellulaire et un blocage de la progression du cycle cellulaire, même si les cellules conservaient des caractéristiques fondamentales de cellules souches. Une inhibition aiguë du NMD, chimique ou via un système de dégradation ciblée (degron), produisait le même phénotype de fusion des télomères, excluant une adaptation à long terme et confirmant que l'activité continue du NMD est directement nécessaire pour maintenir en sécurité des télomères dépourvus de TRF2.
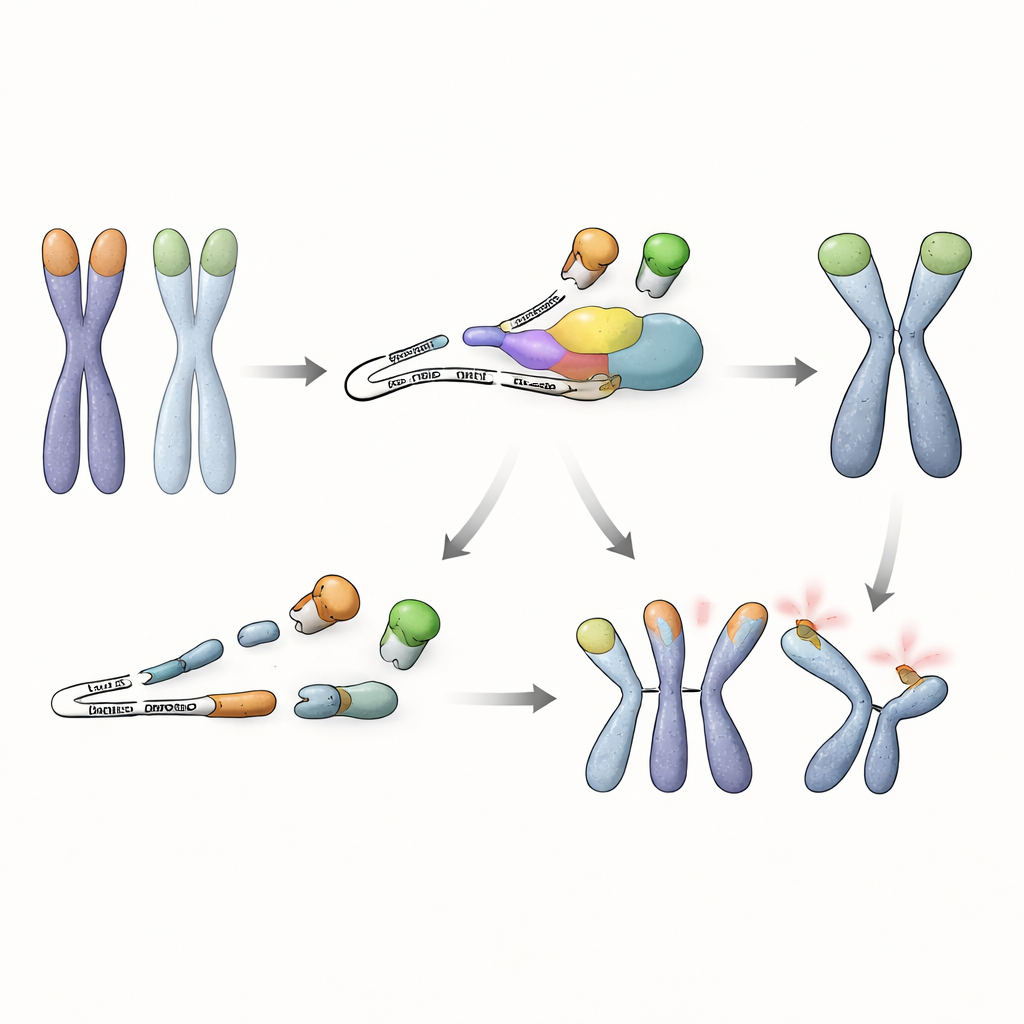
Une protéine raccourcie nuisible compromet les gardiens des télomères
En approfondissant, les chercheurs ont examiné quels messages ARN sont contrôlés par le NMD dans ces cellules souches. Ils ont découvert que le gène Trf1, qui code pour une autre protéine liant les télomères, TRF1, produit un variant d'épissage anormal lorsque le NMD est altéré. Cet ARN modifié saute un segment interne et porte un signal d'arrêt prématuré, conduisant à la production d'une protéine TRF1 raccourcie qui lui fait défaut l'extrémité de liaison à l'ADN mais qui peut encore s'associer avec la TRF1 normale. Dans les cellules déficientes en NMD, cette version tronquée s'accumule et éloigne la TRF1 pleine longueur des télomères. Les expériences ont montré que l'occupation de TRF1 aux extrémités chromosomiques chute fortement dans ces conditions, et le fait de forcer l'expression de la protéine tronquée suffisait à déclencher des fusions de télomères, en particulier lorsque TRF2 était également absent. À l'inverse, augmenter les niveaux de TRF1 pleine longueur dans des cellules déficientes en NMD rétablissait en grande partie la protection des télomères, soulignant que la perte d'une TRF1 efficace aux télomères est le problème central.
Un nouveau lien entre la surveillance de l'ARN et la sécurité du génome
Dans l'ensemble, ce travail révèle que les cellules souches embryonnaires ne dépendent pas uniquement de protéines liant les extrémités de l'ADN pour protéger leurs chromosomes. Elles ont aussi besoin d'une voie de contrôle qualité de l'ARN pour empêcher l'accumulation d'une TRF1 raccourcie et nocive qui déloge sa contrepartie protectrice en pleine longueur. Tant que le NMD est actif, cet ARN défectueux est rapidement éliminé, TRF1 reste aux télomères et les cellules souches peuvent tolérer la perte de TRF2 sans subir de fusions chromosomiques catastrophiques. Cette découverte dévoile une stratégie jusque-là méconnue par laquelle les cellules souches précoces lient la surveillance de l'ARN à la protection des télomères, mettant en lumière la coopération de multiples couches de contrôle pour préserver la stabilité du génome aux premiers stades de la vie.
Citation: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Mots-clés: télomères, cellules souches pluripotentes, contrôle de qualité de l'ARN, dégradation médiée par les non-sens, stabilité du génome