Clear Sky Science · it
La degradazione dell’mRNA mediata da nonsense protegge i telomeri nelle cellule staminali pluripotenti
Come le cellule mantengono sicuri i cappucci dei cromosomi
Ogni volta che una cellula si divide, deve copiare e proteggere il proprio DNA. Le estremità dei nostri cromosomi sono rivestite da strutture speciali chiamate telomeri che funzionano come le punte di plastica dei lacci, impedendo che si sfilaccino o vengano interpretate come rotture. Questo studio esplora come le cellule staminali precoci di topo utilizzino un sistema di riserva inaspettato — una via di “controllo di qualità” dell’RNA — per mantenere intatti questi cappucci quando manca una proteina protettiva principale, rivelando un legame sorprendente tra sorveglianza dell’RNA e sicurezza dei cromosomi.
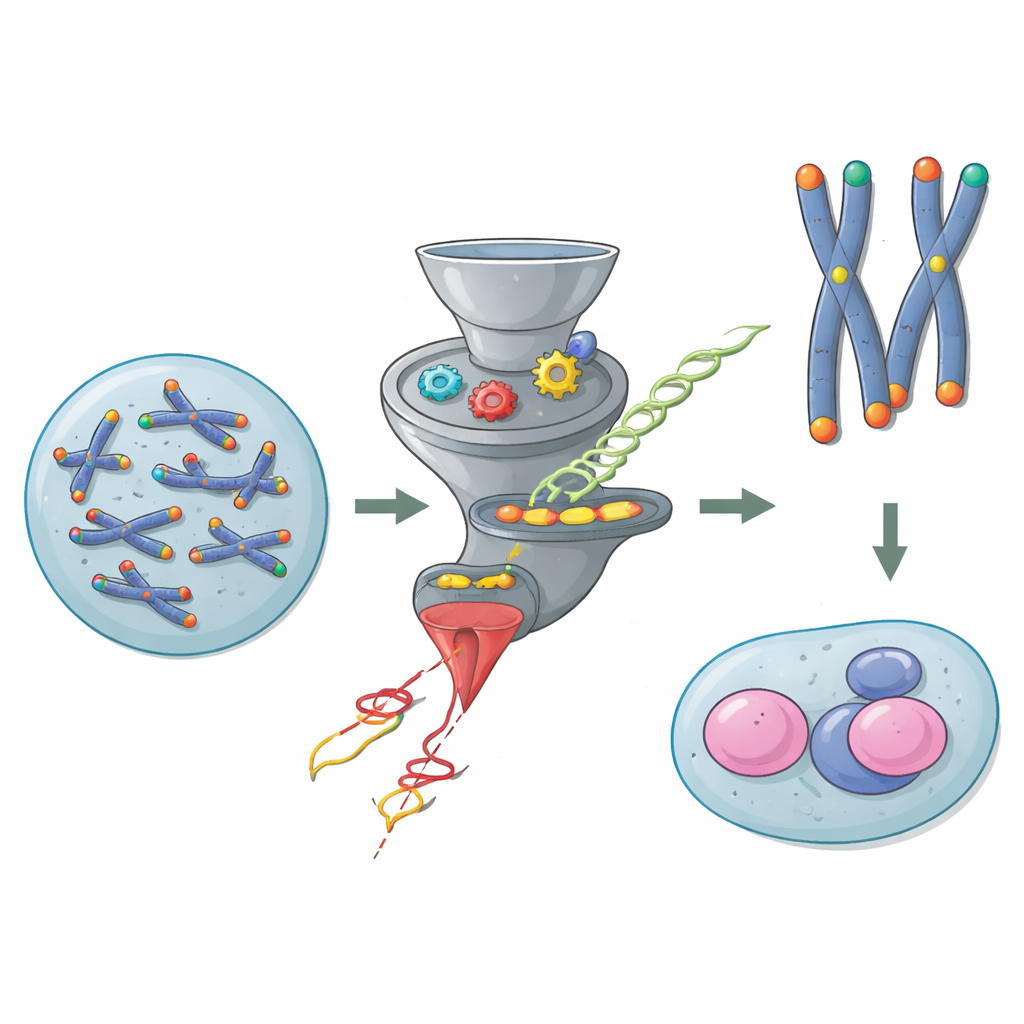
I cappucci protettivi alle estremità dei cromosomi
I cromosomi sono lunghe molecole di DNA che richiedono protezione alle loro punte per non essere confuse con DNA rotto. I telomeri forniscono questa protezione, coadiuvati da un gruppo di proteine noto come Shelterin che riveste le estremità e impedisce reazioni di riparazione pericolose. Nella maggior parte delle cellule dell’organismo, una proteina di Shelterin chiamata TRF2 è cruciale: senza di essa, le estremità cromosomiche si fondono, le risposte al danno del DNA si attivano e i genomi diventano instabili. Tuttavia le cellule staminali embrionali di topo infrangono questa regola. Lavori precedenti hanno mostrato che queste cellule giovani possono sopravvivere e dividersi anche quando TRF2 viene rimosso, suggerendo che qualche via nascosta intervenga a proteggere i loro telomeri.
Una ricerca su tutto il genoma per trovare un aiuto nascosto
Per scoprire questa salvaguardia nascosta, i ricercatori hanno usato uno schermo genetico potente. Hanno disattivato il gene Trf2 nelle cellule staminali embrionali di topo e poi usato CRISPR–Cas9 per perturbare migliaia di altri geni uno per uno. Se la perdita di un secondo gene uccideva improvvisamente cellule già prive di TRF2, quel secondo gene veniva segnalato come partner in una “letalità sintetica” — un indizio che aiuta a compensare la perdita di TRF2. Lo schermo ha recuperato fattori telomerici attesi ma ha anche evidenziato diversi componenti di una via apparentemente non correlata: la degradazione mediata da nonsense (NMD), un sistema noto soprattutto per eliminare messaggi di RNA difettosi che contengono segnali di stop prematuri.
Quando la pulizia dell’RNA fallisce, le estremità dei cromosomi si rompono
Il gruppo ha quindi testato cosa accade quando fattori dell’NMD vengono rimossi in cellule staminali prive di TRF2. La perdita di TRF2 da sola o l’eliminazione dell’NMD da sola causava poco danno ai telomeri: le estremità cromosomiche apparivano per lo più normali e le cellule continuavano a proliferare. Ma quando TRF2 e l’NMD venivano interrotti insieme, lo scenario cambiava drasticamente. Marcatori di danno al DNA si accumulavano specificamente ai telomeri e i cromosomi si fondevano frequentemente estremità contro estremità. Queste fusioni cromosomiche coincidono con forti difetti di crescita, aumento della morte cellulare e blocco della progressione del ciclo cellulare, nonostante le cellule mantenessero le caratteristiche fondamentali di staminalità. L’arresto acuto dell’NMD tramite inibitori chimici o sistemi degron produceva lo stesso fenotipo di fusione dei telomeri, escludendo adattamenti a lungo termine e confermando che l’attività continua dell’NMD è direttamente richiesta per mantenere sicuri i telomeri privi di TRF2.
Una proteina accorciata e dannosa mina le guardie dei telomeri
Approfondendo, i ricercatori hanno esaminato quali messaggi di RNA sono controllati dall’NMD in queste cellule staminali. Hanno scoperto che il gene Trf1, che codifica per un’altra proteina legante i telomeri, TRF1, produce una variante di splicing anomala quando l’NMD è compromessa. Questo RNA alterato salta un segmento interno e porta un segnale di stop precoce, portando alla produzione di una proteina TRF1 accorciata che non possiede la punta per il legame al DNA ma può comunque dimerizzare con la TRF1 normale. Nelle cellule prive di NMD, questa versione tronca si accumula e sottrae la TRF1 a lunghezza intera dai telomeri. Gli esperimenti hanno mostrato che l’occupazione di TRF1 alle estremità cromosomiche diminuisce drasticamente in queste condizioni, e il semplice forzare l’espressione della proteina truncata era sufficiente a indurre fusioni telomeriche, soprattutto quando anche TRF2 era assente. Viceversa, aumentare i livelli di TRF1 a lunghezza intera in cellule difettose per l’NMD ristabiliva in gran parte la protezione dei telomeri, sottolineando che la perdita di TRF1 efficace ai telomeri è il problema chiave.
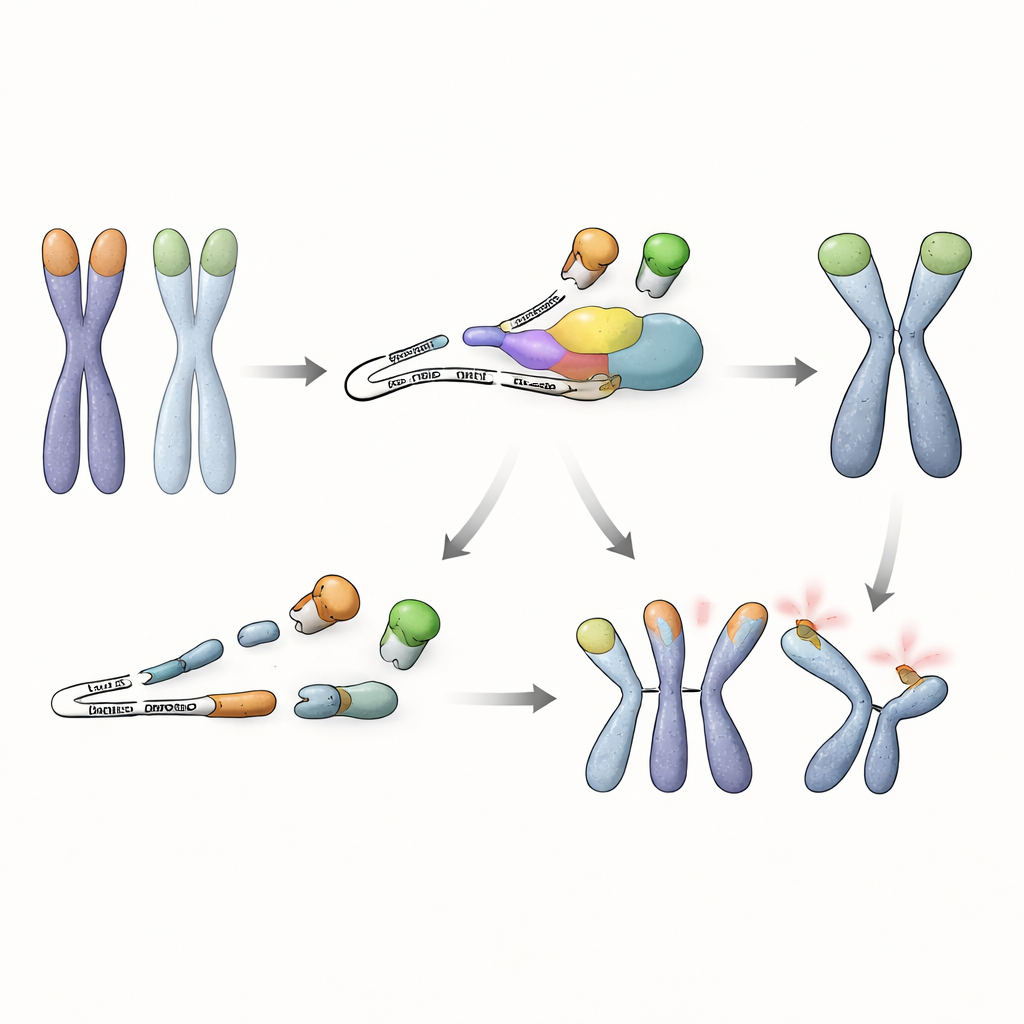
Un nuovo legame tra sorveglianza dell’RNA e sicurezza del genoma
Nel complesso, il lavoro rivela che le cellule staminali embrionali fanno affidamento su più che semplici proteine che si legano alle estremità del DNA per proteggere i loro cromosomi. Hanno anche bisogno di una via di controllo di qualità dell’RNA per prevenire l’accumulo di una versione dannosa e accorciata di TRF1 che spiazza la sua controparte protettiva a lunghezza intera. Finché l’NMD è attiva, questo RNA difettoso viene rapidamente distrutto, TRF1 rimane ai telomeri e le cellule staminali possono tollerare la perdita di TRF2 senza fusioni cromosomiche catastrofiche. Questa scoperta mette in luce una strategia precedentemente non riconosciuta con cui le cellule staminali precoci collegano la sorveglianza dell’RNA alla protezione dei telomeri, evidenziando come più livelli di controllo cooperino per preservare la stabilità del genoma nelle prime fasi della vita.
Citazione: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Parole chiave: telomeri, cellule staminali pluripotenti, controllo di qualità dell'RNA, degradazione mediata da nonsense, stabilità del genoma