Clear Sky Science · ru
Деградация мРНК, обусловленная выходом за стоп-кодон, защищает теломеры в плюрипотентных стволовых клетках
Как клетки защищают «насадки» хромосом
Каждый раз при делении клетка должна скопировать и защитить свою ДНК. Концы наших хромосом покрыты особыми структурами — теломерами, которые действуют как пластиковые наконечники на шнурках, предотвращая «распускание» и ошибочные реакции ремонта. В этом исследовании показано, как ранние мышиные стволовые клетки используют неожиданный резервный механизм — путь «контроля качества» РНК — чтобы сохранять эти крышки целыми при отсутствии одного из основных защитных белков, что выявляет удивительную связь между надзором за РНК и безопасностью хромосом.
Защитные «насадки» на концах хромосом
Хромосомы — это длинные молекулы ДНК, которым нужна защита на концах, чтобы их не принимали за разрывы. Теломеры обеспечивают эту защиту при помощи комплекса белков Shelterin, которые покрывают концы и блокируют опасные реакции ремонта. В большинстве соматических клеток один белок Shelterin — TRF2 — имеет решающее значение: при его отсутствии концы хромосом сливаются, запускаются ответы на повреждение ДНК, и геномы становятся нестабильными. Тем не менее эмбриональные стволовые клетки мыши нарушают это правило. Предыдущие исследования показали, что эти молодые клетки могут выживать и делиться даже при удалении TRF2, что указывает на существование скрытого пути, который берёт на себя охрану теломер.
Геномный поиск скрытого помощника
Чтобы обнаружить этот резерв, исследователи провели масштабный генетический скрининг. Они инактивировали ген Trf2 в эмбриональных стволовых клетках мыши, а затем с помощью CRISPR–Cas9 поочерёдно нарушали тысячи других генов. Если потеря второго гена внезапно убивала клетки, уже лишённые TRF2, такой ген фиксировался как участник «синтетической летальности» — признак того, что он компенсирует потерю TRF2. Скрининг выявил ожидаемые факторы теломер, но также выделил несколько компонентов, казалось бы, не связанного пути: nonsense-mediated mRNA decay (NMD) — системы, известной уничтожением дефектных РНК-сообщений с преждевременными стоп-кодонами.
Когда очистка РНК даёт сбой, ломаются концы хромосом
Команда проверила, что происходит при удалении факторов NMD в клетках, лишённых TRF2. Само по себе отсутствие TRF2 или сам по себе дефект NMD вызывали мало повреждений теломер: концы хромосом выглядели в основном нормально, и клетки продолжали расти. Но при одновременном нарушении TRF2 и NMD картина резко менялась. Маркеры повреждения ДНК накапливались специфически на теломерах, и хромосомы часто срастались «конец в конец». Эти слияния сопровождались серьёзными нарушениями роста, увеличением гибели клеток и задержкой прогрессии клеточного цикла, хотя клетки сохраняли ключевые признаки стволовых клеток. Быстрая химическая или дегрон-опосредованная блокада NMD вызывала тот же фенотип слияния теломер, исключая адаптацию при длительном дефиците и подтверждая, что активность NMD постоянно требуется для защиты теломер при отсутствии TRF2.
Вредный укороченный белок подрывает защиту теломер
Углубившись, исследователи изучили, какие РНК-копии контролируются NMD в этих стволовых клетках. Они обнаружили, что ген Trf1, кодирующий другой белок, связывающий теломеры — TRF1, — даёт аномальный сплайс-вариант при нарушении NMD. Эта изменённая РНК пропускает внутренний участок и несёт преждевременный стоп-кодон, в результате чего образуется укороченная версия белка TRF1, лишённая ДНК-связывающего домена, но всё ещё способная димеризоваться с нормальным TRF1. В клетках с дефицитом NMD эта усечённая форма накапливается и «оттягивает» полноразмерный TRF1 с теломер. Эксперименты показали резкое снижение занятости TRF1 на концах хромосом в таких условиях, а принудительная экспрессия укороченного белка была достаточна, чтобы вызвать слияния теломер, особенно при отсутствии TRF2. Наоборот, повышение уровней полноразмерного TRF1 в клетках с дефектом NMD в значительной степени восстанавливало защиту теломер, подчёркивая, что ключевая проблема — потеря эффективного TRF1 на теломерах.
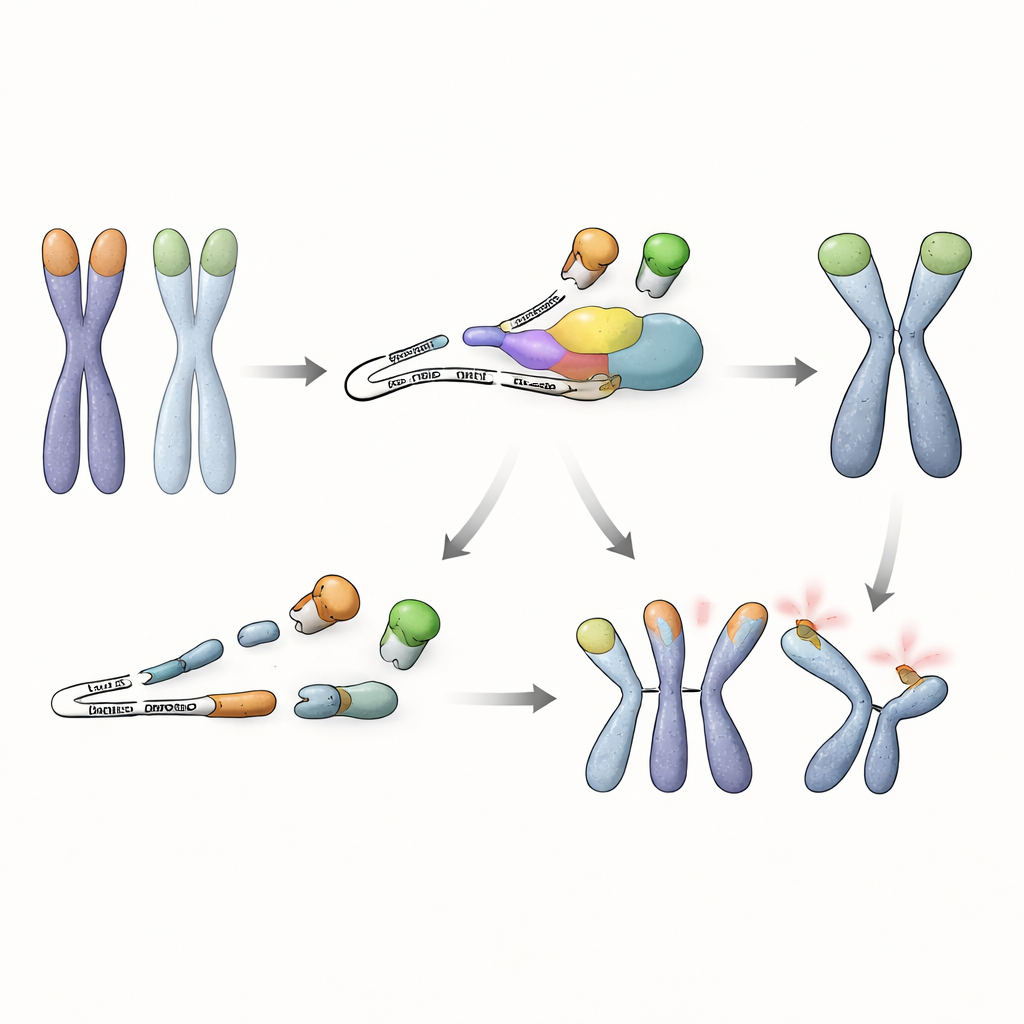
Новая связь между надзором за РНК и безопасностью генома
В целом работа показывает, что эмбриональные стволовые клетки полагаются не только на белки, связывающие концы ДНК, для охраны своих хромосом. Им также необходим путь контроля качества РНК, чтобы предотвратить накопление вредного укороченного белка TRF1, вытесняющего его защитную полноформатную версию. Пока NMD активен, эта ошибочная РНК быстро разрушается, TRF1 остаётся на теломерах, и стволовые клетки могут переносить утрату TRF2 без катастрофического слияния хромосом. Это открытие выявляет ранее не признанную стратегию, при которой ранние стволовые клетки связывают надзор за РНК с защитой теломер, подчёркивая, как несколько уровней контроля сотрудничают для сохранения стабильности генома на самых ранних этапах жизни.
Цитирование: Markiewicz-Potoczny, M., Lee, S.Y., Chatterjee, S. et al. Nonsense-mediated mRNA decay safeguards telomeres in pluripotent stem cells. Nat Cell Biol 28, 674–683 (2026). https://doi.org/10.1038/s41556-026-01912-0
Ключевые слова: теломеры, плюрипотентные стволовые клетки, контроль качества РНК, nonsense-mediated decay, стабильность генома