Clear Sky Science · zh
签署、封存、递送:一种可泛化的活体生物治疗剂量与代谢模型
将有益微生物变成药物
许多人知道肠道微生物会影响健康,但要把这些微小的“乘客”转化为精确、可靠的药物却远非易事。本研究处理了一个非常实际的问题:如果我们吞下一粒含有工程化“有益菌”的胶囊,目的是在肠道中清除有害化学物质,那么应服用多少以及何时服用?作者建立了一个将食物在胃肠通过过程、我们常驻微生物对其的作用,以及外加益生菌株如何介入并保护机体连接起来的数学框架。
以体味障碍为测试案例
研究者关注三甲胺尿症,有时称为“鱼腥味综合征”。在这种情况下,肝脏一种酶的突变导致一种强烈气味的化合物三甲胺(TMA)无法被有效中和,进而在汗液、呼气和尿液中积累。TMA主要在肠道中由细菌分解食物中的胆碱等营养物质产生,这些营养物质存在于鸡蛋和肉类等常见食物中。现有治疗尝试通过限制这些营养物质或用抗生素杀灭肠道细菌,但这些策略难以长期维持且可能引发副作用。作者探讨了另一种思路:添加一种活体生物治疗产品——一种携带能将TMA在进入血液前直接在肠道内转化为无害、无气味形式的工程化细菌。
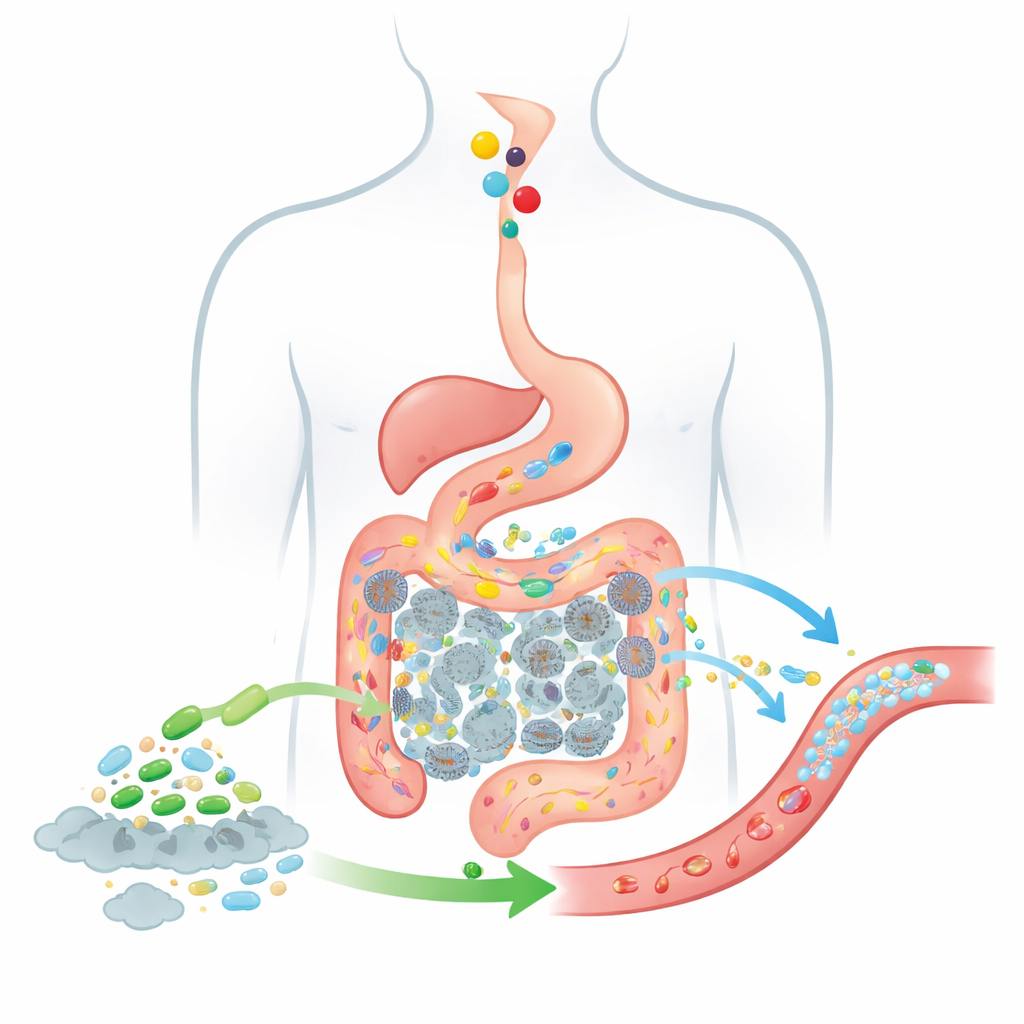
追踪食物与细菌通过肠道的过程
为预测这种活体疗法的效果,作者扩展了经典的药物吸收模型CAT模型,该模型追踪吞服物如何从胃进入小肠各段并进入结肠。他们更新的BCAT模型将肠道划分为多个相连的“箱子”,每个箱子代表一段肠道或结肠,具有各自的液体体积、典型细菌数量和吸收行为。随着食物从一格移动到下一格,模型跟踪胆碱的含量、肠道细菌产生的TMA量、穿过血液的TMA分量,以及外加益生菌细胞沿相同路线的迁移与作用。与早期模型不同,该模型将益生菌群体视为一个移动且不断变化的细胞云,而非固定背景,并明确纳入了结肠——TMA绝大多数产生的部位。
用真实世界数据检验模型
模型只有与现实相符才有用,因此团队用人类数据检验了BCAT。首先,他们考察模型是否能重现1950年代到1990年代的经典营养学研究,在这些研究中,受试者摄入已知剂量的胆碱,研究者随后收集并分析尿液中的TMA及其被中和的形式。在多个剂量水平和独立研究中,被转化为三甲胺的胆碱比例大约在三分之二附近;BCAT成功再现了这一模式。接着,他们将该框架应用于另一种用于遗传病苯丙酮尿症的工程化益生菌SYNB1618。使用临床试验中受试者尿液中诊断性分解产物的浓度数据,BCAT的预测仅差约5%,远优于分辨率较低的简单模型。
需要多少益生菌以及何时服用?
有了这些验证,作者将BCAT应用于三甲胺尿症问题。他们询问:能将血液中总TMA暴露减少95%(大致相当于健康肝酶的天然清除能力)的最小益生菌剂量是多少?当益生菌与含胆碱餐同时服用时,模型建议的剂量约为一百亿个细胞,类似于典型非处方益生菌胶囊可容纳的量。但时间安排很重要。由于常驻肠道细菌已在结肠各处定植,而吞服的益生菌必须从胃出发到达那里,因此疗法到位存在延迟。模拟显示,在含胆碱餐前大约三到四小时服用益生菌可以让它“提前到达”、在结肠内扩散并更有效地截获TMA。在这种时间安排下,所需剂量大约减少四倍,这可能降低对极高微生物负荷的安全担忧。
哪些因素在幕后最重要
并非每个生物学细节对结果的影响都相同,作者因此使用一种全局敏感性分析来识别哪些模型成分真正决定成功。明显的关键是每个益生菌细胞能携带的活性酶量。肠道通过时间、吸收速率,甚至总体细菌密度在现实范围内的变化影响相对较小。这意味着在设计此类活体生物制剂时,工程化细胞提高关键酶的产量可能远比微调其在肠道中移动速度更为重要。也表明BCAT给出的剂量建议应在不同个体之间相对稳健,尽管他们的消化速度和微生物组存在差异。
从一种疾病到更多适应症
归根结底,这项工作不仅为一种罕见且在社交上令人苦恼的体味障碍提供了指导。它引入了一个通用、可适配的框架,用于规划和优化那些肠道微生物会将饮食或体内源性化合物转化为有害副产物的任何疾病的活微生物疗法。通过将肠道运输、原生微生物化学反应与工程化酶清除整合到一个定量图景中,BCAT模型可以在菌株进入临床试验之前就提出现实的剂量目标和时间策略。对于患者和临床医生来说,这意味着未来的益生菌药物不仅听起来更天然、更友好,而且也将更加可预测、可调节,并以与常规药物相同的严谨规划为基础。
引用: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
关键词: 肠道微生物组, 益生菌疗法, 三甲胺尿症, 数学建模, 活体生物治疗剂