Clear Sky Science · he
חתום, מאושר, מסופק: מודל כללי למתן ובי־חילוף חומרים של תרופות ביולוגיות חיות
להפוך חיידקים מועילים לתרופה
רבים יודעים שמיקרובים במעי משפיעים על הבריאות, אך קשה למדי להפוך אותם לתרופה מדויקת ואמינה. המחקר הזה מתמודד עם שאלה פרקטית מאוד: אם נבלע קפסולה של "חיידקים טובים" מהונדסים שנועדו לנקות חומר מזיק במעי, כמה כדאי ליטול ומתי? המחברים בונים מסגרת מתמטית שמחברת בין מה שקורה למזון כשהוא נע בקיבה ובמעי, מה שעושים המיקרובים המקומיים שלנו, וכיצד זן פרוביוטי נוסף יכול להתערב ולהגן על הגוף.
הפרעת ריח גוף כמקרה מבחן
החוקרים מתמקדים בטרימתילאמינוריה, שלעתים מכונה "תסמונת ריח דג". במצב זה, מוטציות באנזים כבד מובילות לכך שהתרכובת הריחנית טרימתילאמין (TMA) אינה מנוטרלת כראוי ומצטברת בזיעה, בנשימה ובשתן. TMA מיוצר בעיקר במעי כאשר חיידקים מפרקים מזונות המכילים כולין, כגון ביצים ובשר. הטיפולים הנוכחיים מנסים להרעיב את המערכת מהחומר המגיב או להרוג חיידקי מעי באמצעות אנטיביוטיקה — אסטרטגיות שקשות לאחיזה ועלולות לגרום לתופעות לוואי. המחברים בוחנים רעיון שונה: להוסיף מוצר ביותרפויטי חי — חיידק מותאם הנושא אנזים שממיר TMA לצורה בלתי ריחנית וחסרת נזק ישירות במעי לפני שהוא נכנס למחזור הדם.
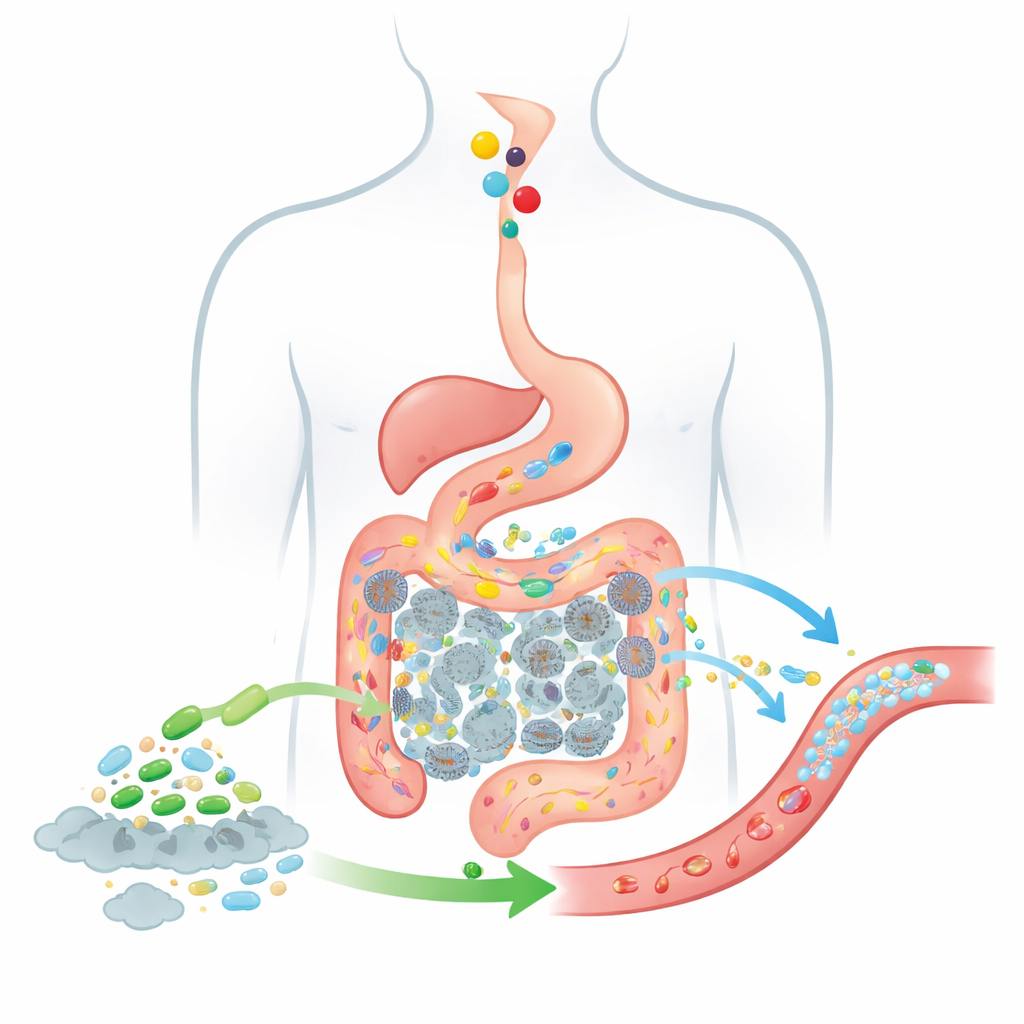
לעקוב אחרי מזון וחיידקים לאורך המעי
כדי לחזות עד כמה טיפול חי כזה עלול לעבוד, המחברים מרחיבים מודל קלאסי לספיגת תרופות הידוע כמודל CAT, שמנטר כיצד חומרים נבלעים ונעים מהקיבה דרך מקטעי המעי הדק אל המעי הגס. מודל BCAT המעודכן שלהם מחלק את המעי למספר "תאים" מקושרים, שלכל אחד מהם נפח נוזלים משלו, מספר חיידקים טיפוסי והתנהגות ספיגה משלו. כשהמזון עובר מתא לתא, המודל עוקב כמה כולין נוכח, כמה TMA מייצרים חיידקי המעי, כמה ממנו חוצה לדם וכיצד תאים פרוביוטיים שהוספו נעים ופועלים באותו מסלול. בשונה ממודלים מוקדמים, זה מטפל באוכלוסיית הפרוביוטיקה כעננה ניידת ומשתנה של תאים ולא כרקע קבוע, והוא כולל במפורש את המעי הגס, שבו מיוצר רוב ה־TMA.
בדיקת המודל מול נתוני אמת
מודל שימושי רק אם הוא מתאים למציאות, ולכן הצוות בדק את BCAT מול נתונים אנושיים. ראשית, הם שאלו האם המודל יכול לשחזר מחקרי תזונה קלאסיים משנות ה־50 עד ה־90, שבהם נבדקים אכלו כמויות מדודות של כולין וחוקרים אספו וניתחו אחר־כך את ה־TMA וצורתו המנוטרלת בשתן. ברמות מינון שונות ובמחקרים עצמאיים, החלק של הכולין שהפך לטרימתילאמינים נע סביב שני שלישים; BCAT תפס בהצלחה דפוס זה. לאחר מכן הם יישמו את המסגרת על פרוביוטיקה מהונדסת אחרת, SYNB1618, שנועדה למחלה תורשתית — פנילקטונוריה. בעזרת נתוני ניסוי קליני לגבי כמה מוצרי פירוק אבחון הופיעו בשתן הנבדקים, תחזיות BCAT שונות בכעשירית בלבד, דרגה שהפגינה ביצועים טובים בהרבה ממודלים פשוטים ורחבי־רזולוציה נמוכה.
כמה פרוביוטיקה ומתי ליטול?
עם האימות הזה, המחברים החילו את BCAT על טרימתילאמינוריה. הם שאלו: מה המינון הקטן ביותר של פרוביוטיקה שיכול להפחית את כל חשיפת ה־TMA בדם ב־95 אחוז — קירוב לכוח הניקוי הטבעי של אנזים כבד תקין? כאשר הפרוביוטיקה נלקחת יחד עם הארוחה, המודל מציע מינון של סדר גודל עשר מיליארד תאים, דומה למה שנכנס בקפסולה פרוביוטית רגילה ללא מרשם. אך הזמן חשוב. מכיוון שחיידקי המיקרופלורה המקומיים כבר מפוזרים במעי הגס בעוד שהפרוביוטיקה הנבלעת צריכה להגיע לשם מהקיבה, יש עיכוב עד שהטיפול נמצא במקום הנכון. סימולציות מראות כי נטילת הפרוביוטיקה כשלוש עד ארבע שעות לפני ארוחה עשירה בכולין מאפשרת לה "להגיע מוקדם", להתפשט במעי הגס וליירט TMA ביעילות רבה יותר. בלוח זמנים כזה המינון הדרוש קטן בכ־פקטור של כארבעה, מה שיכול להפחית חששות בטיחותיים הקשורים לעומסי מיקרוביות מאוד גבוהים.
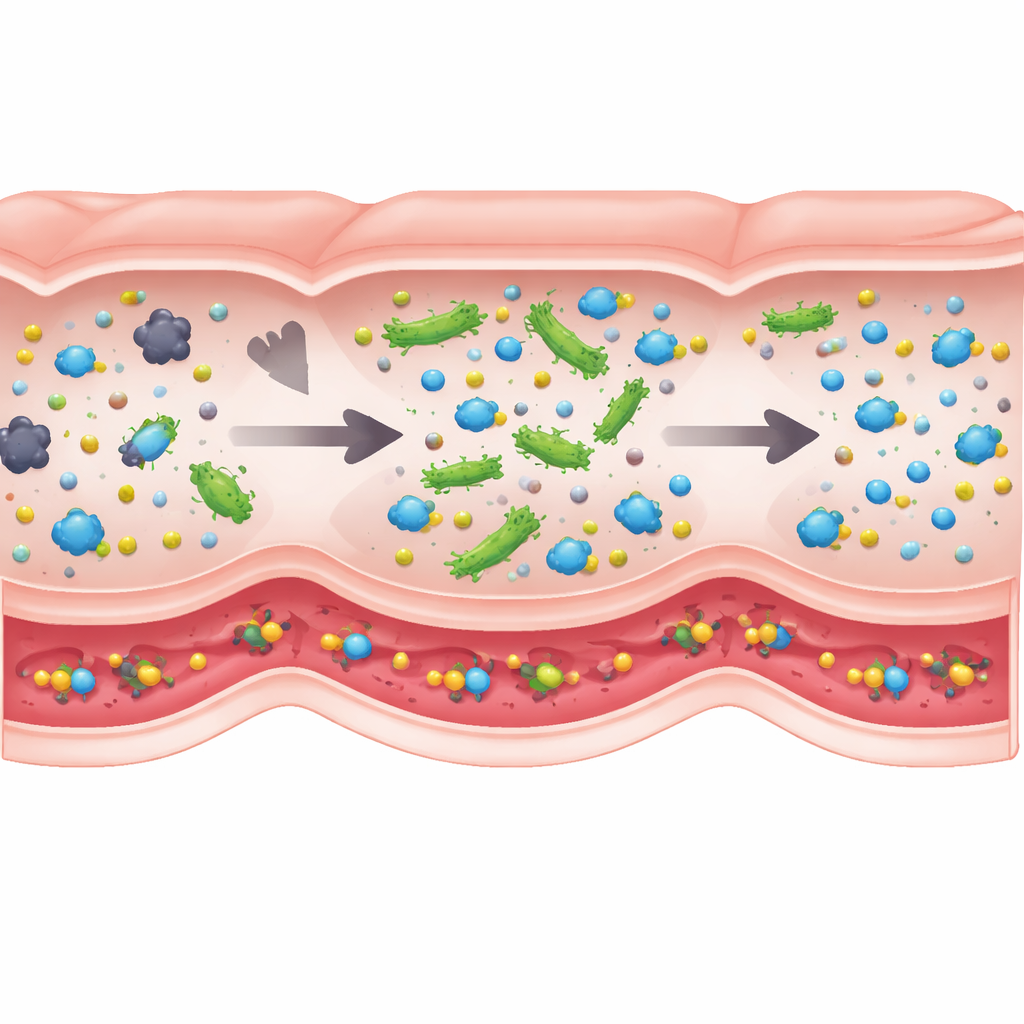
מה חשוב מאחורי הקלעים
לא כל פרט ביולוגי משפיע באותה מידה על התוצאה, ולכן המחברים השתמשו בסוג של ניתוח רגישות גלובלי כדי לראות אילו מרכיבים של המודל באמת מניעים את ההצלחה. המנצח הברור היה כמות האנזים הפעיל שכל תא פרוביוטי יכול לשאת. שינויים בזמני מעבר במעי, בקצבי ספיגה או אפילו בצפיפות החיידקים הכוללת השפיעו באופן יחסי פחות בטווחים ריאליסטיים. משמעות הדבר היא שבעיצוב ביותרפויטיקה חיה, הנדסת תאים שמייצרים יותר מהאנזים המרכזי עשויה להיות חשובה יותר מכיול מהירות התנועה שלהם דרך המעי. זה גם מרמז שהמלצות מינון מ‑BCAT אמורות להיות יציבות יחסית בין אנשים שונים, אף על פי שקצב העיכול והמיקרוביומות שלהם משתנים.
ממקרה בודד לרבים
לסיכום, עבודה זו לא רק מספקת קווים מנחים עבור הפרעה נדירה ומטרידה חברתית. היא מציגה מסגרת כללית ומותאמת לתכנון ואופטימיזציה של טיפולים מיקרוביאליים חיים לכל מצב שבו מיקרוביוטת המעי ממירה תרכובות תזונתיות או גוף־מוצא לתוצרי לוואי מזיקים. על ידי קישור בין מעבר במעי, כימיה מיקרוביאלית מקומית וניקוי אנזימטי מהונדס לתמונה כמותית אחת, מודל BCAT יכול להציע יעדי מינון ואסטרטגיות תזמון ריאליסטיות הרבה לפני שזן מגיע לניסויים קליניים. עבור מטופלים ורופאים, זה מקרב את הבטחה שתרופות פרוביוטיות עתידיות לא יהיו רק "ידידותיות" ומושמעות לטבע — אלא גם צפויות, ניתנות לכיול ומבוססות על תכנון קפדני כזהה לזה של תרופות מקובלות.
ציטוט: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
מילות מפתח: מיקרוביוטת המעי, טיפול פרוביוטי, טרימתילאמינוריה, מידול מתמטי, ביותרפויטיקה חיה