Clear Sky Science · tr
İmzalandı, mühürlendi, teslim edildi: yaşayan biyoterapötik dozajlama ve metabolizma için genellenebilir bir model
Yararlı Mikropları İlaca Dönüştürmek
Birçok kişi bağırsaklarımızdaki mikropların sağlığı etkileyebileceğini bilir, ancak bu küçük yolcuları nasıl hassas ve güvenilir ilaçlara dönüştüreceğimizi anlamak çok daha zordur. Bu çalışma çok pratik bir sorunu ele alıyor: zararlı bir kimyasalı bağırsakta temizlemesi amacıyla yutulan genetik olarak tasarlanmış “iyi bakteri” kapsülünden ne kadar alınmalı ve ne zaman alınmalı? Yazarlar, yiyeceğin mide ve bağırsaklarda hareketi, yerleşik mikroplarımızın bununla ne yaptığı ve eklenen probiyotik suşun vücuda nasıl koruma sağlayabileceği arasındaki bağlantıyı kuran matematiksel bir çerçeve inşa ediyor.
Test Vakası Olarak Bir Vücut Kokusu Bozukluğu
Araştırmacılar trimetilaminuriyi, bazen “balık kokusu sendromu” olarak adlandırılan durumu incelemeye odaklanıyor. Bu durumda, karaciğer enzimindeki mutasyonlar nedeniyle güçlü kokulu bir bileşik olan trimetilamin (TMA) uygun şekilde nötralize edilemez ve terde, nefeste ve idrarda birikir. TMA çoğunlukla bağırsakta, bakterilerin yumurta ve et gibi yaygın gıdalardaki kolin gibi besinleri parçalaymasıyla oluşur. Mevcut tedaviler bu besinleri kısıtlamayı veya antibiyotiklerle bağırsak bakterilerini öldürmeyi deniyor; bunlar sürdürülemesi zor ve yan etkilere yol açabilecek stratejilerdir. Yazarlar farklı bir fikri araştırıyor: bağırsakta kan dolaşımına geçmeden önce TMA’yı zararsız, kokusuz forma dönüştürebilen bir enzimi taşıyan genetik olarak tasarlanmış bir bakteri — yani canlı bir biyoterapötik ürün — eklemek.
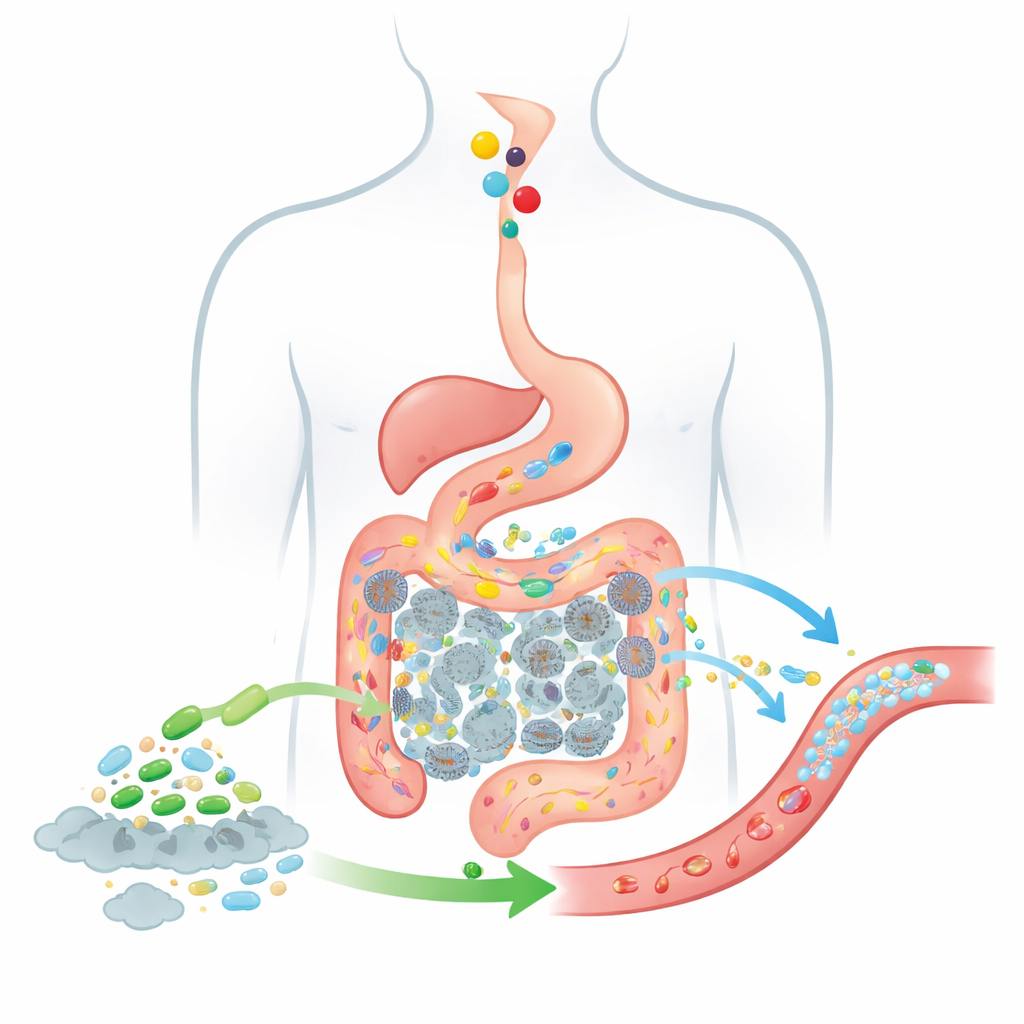
Yiyecek ve Bakterileri Bağırsaktan İzlemek
Böyle bir yaşayan terapinin ne kadar iyi çalışacağını tahmin etmek için yazarlar, yutulan maddelerin mideden ince bağırsak bölümleri ve kolon aracılığıyla nasıl hareket ettiğini izleyen klasik bir ilaç-emilim modeli olan CAT modelini genişletiyorlar. Güncellenmiş BCAT modelleri, bağırsak ve kolonun her birinin kendi sıvı hacmi, tipik bakteri sayıları ve emilim davranışı olan bir dizi bağlı “kutuya” bölünüyor. Yiyecek bir kutudan diğerine geçerken model, ne kadar kolin bulunduğunu, bağırsak bakterilerinin ne kadar TMA ürettiğini, bu TMA’nın ne kadarının kana geçtiğini ve eklenen probiyotik hücrelerin aynı güzergâh boyunca nasıl hareket edip davrandığını takip ediyor. Önceki modellere kıyasla bu model, probiyotik popülasyonu sabit bir arka plan yerine hareket eden, değişen bir hücre bulutu olarak ele alıyor ve TMA’nın büyük çoğunluğunun üretildiği kolonu açıkça içeriyor.
Modeli Gerçek Dünya Verileriyle Kontrol Etmek
Bir model, gerçeğe uyuyorsa ancak yararlıdır; bu yüzden ekip BCAT’i insan verilerine karşı test etti. Önce, modelin 1950’lerden 1990’lara kadar klasik beslenme çalışmalarını yeniden üretebilip üretemeyeceğini sordular; bu çalışmalarda gönüllüler ölçülmüş miktarda kolin aldı ve araştırmacılar daha sonra idrarda TMA ve nötralize edilmiş formunu topladı ve analiz etti. Birkaç doz düzeyinde ve bağımsız çalışmada, kolinin trimetilaminlere dönüşen fraksiyonu yaklaşık üçte iki civarında seyretti; BCAT bu deseni başarıyla yakaladı. Ardından çerçeve, kalıtsal fenilketonüri hastalığı için tasarlanmış SYNB1618 adlı farklı bir genetik probiyotik üzerinde uygulandı. Deneklerin idrarında görülen tanısal parçalanma ürün miktarına ilişkin klinik deneme verilerini kullanarak BCAT tahminleri yalnızca yaklaşık yüzde 5 farklılık gösterdi ve daha basit, düşük çözünürlüklü modelleri açıkça geride bıraktı.
Ne Kadar Probiyotik ve Ne Zaman Alınmalı?
Bu doğrulamanın ardından yazarlar BCAT’i trimetilaminuri üzerinde çalıştırdı. Sordukları soru şuydu: Sağlıklı bir karaciğer enziminin doğal temizleme gücüne yaklaşık olarak karşılık gelen, toplam kan TMA maruziyetini yüzde 95 azaltabilecek en küçük probiyotik dozu nedir? Probiyotik ve öğün birlikte alındığında model, tipik reçetesiz probiyotik kapsülde bulunan miktara benzer şekilde yaklaşık on milyar hücre civarında bir doz öneriyor. Ancak zamanlama önemli. Yerleşik bağırsak bakterileri kolonda zaten yayılmışken yutulan probiyotiklerin mide ve ince bağırsaktan geçip oraya ulaşması gerekir; bu nedenle terapinin doğru yerde olması biraz zaman alır. Simülasyonlar probiyotiğin kolona “erken ulaşmasını”, kolon boyunca yayılmasını ve TMA’yı daha etkili bir şekilde yakalamasını sağlamak için kolin açısından zengin bir öğünden yaklaşık üç-dört saat önce alınmasının uygun olduğunu gösteriyor. Bu takvime uyulduğunda gereken doz yaklaşık dört kat düşüyor; bu da çok yüksek mikrobiyel yüklerle ilgili güvenlik kaygılarını azaltabilir.
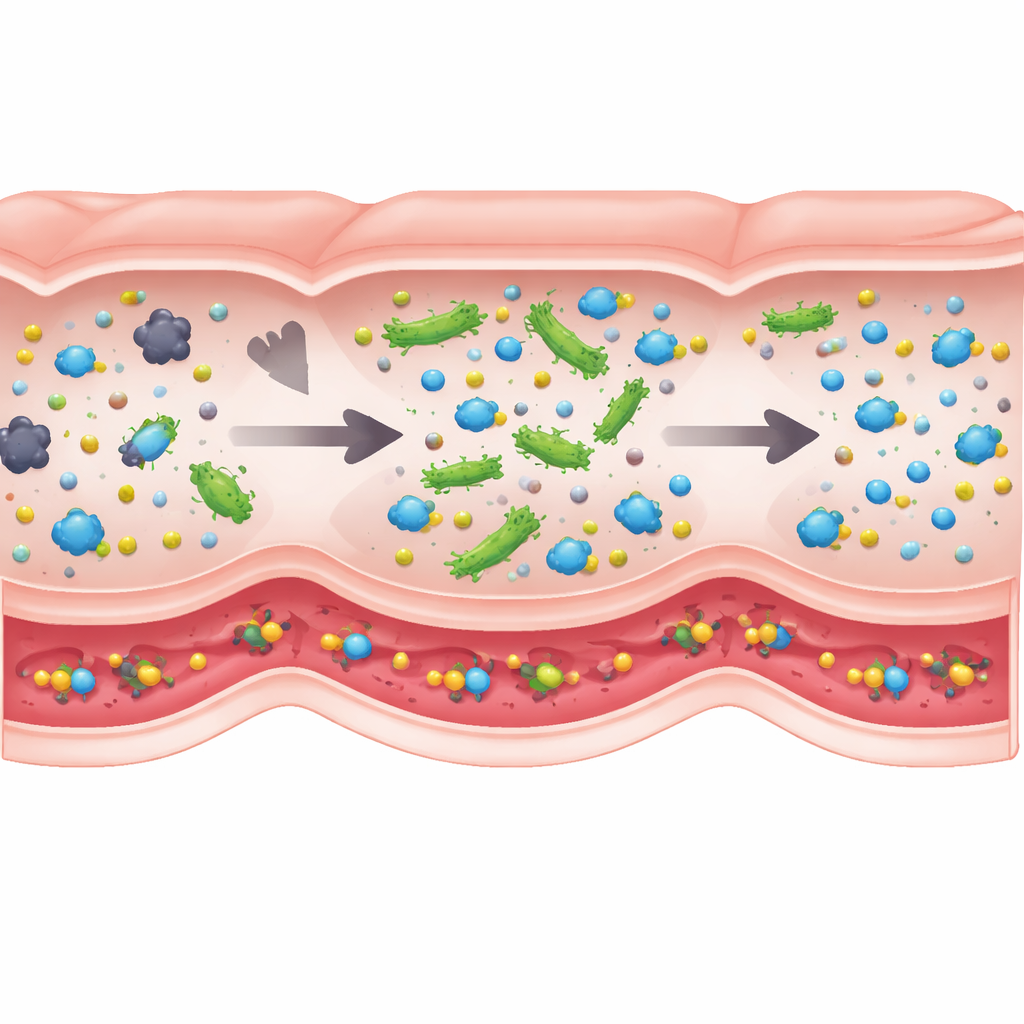
Kilit Noktada En Çok Ne Önemli?
Her biyolojik detay sonucun üzerinde eşit etkiye sahip değildir; bu nedenle yazarlar hangi model bileşenlerinin başarıyı gerçekten yönlendirdiğini görmek için bir tür küresel duyarlılık analizi kullandılar. Açık kazanan, her probiyotik hücrenin taşıyabileceği aktif enzim miktarıydı. Bağırsak geçiş sürelerindeki, emilim oranlarındaki veya hatta toplam bakteri yoğunluğundaki değişiklikler gerçekçi aralıklarda nispeten küçük etkiler gösterdi. Bu, bu tür canlı biyoterapotikler tasarlanırken, hücreleri anahtar enzimi daha fazla üretecek şekilde mühendislik etmenin, onların bağırsaktaki hareket hızını ince ayarlamaktan çok daha önemli olabileceğini gösteriyor. Ayrıca BCAT’in dozaj önerilerinin, sindirim hızları ve mikrobiyomları farklı olsa bile, farklı insanlar arasında nispeten dayanıklı olması gerektiğini düşündürüyor.
Bir Bozukluktan Birçokuna
Sonuç olarak bu çalışma yalnızca nadir ve sosyal açıdan bunaltıcı bir koku bozukluğu için rehberlik sunmuyor. Bağırsak mikrobiyomunun diyet veya vücut kaynaklı bileşikleri zararlı yan ürünlere dönüştürdüğü herhangi bir durumda canlı mikrobiyal terapileri planlamak ve optimize etmek için genel, uyarlanabilir bir çerçeve tanıtıyor. Bağırsak geçişi, yerli mikrobiyal kimya ve mühendislik ürünü enzimatik temizliği tek bir nicel resimde birleştirerek BCAT modeli, bir suş klinik denemelere ulaşmadan çok önce gerçekçi dozaj hedefleri ve zamanlama stratejileri önerebilir. Hastalar ve klinisyenler için bu, gelecekteki probiyotik ilaçların yalnızca dostça ve doğal görünen değil, aynı zamanda öngörülebilir, ayarlanabilir ve konvansiyonel ilaçlar için kullanılan aynı titiz planlamaya dayalı olacağı vaadini getiriyor.
Atıf: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
Anahtar kelimeler: bağırsak mikrobiyomu, probiyotik tedavi, trimetilaminuri, matematiksel modelleme, canlı biyoterapotikler